Zuverlässiger Partner für die Regulierung von Medizinprodukten in Großbritannien
Unterstützung bei der UKCA-Kennzeichnung und MHRA
Registrieren Sie Ihr Medizinprodukt im Vereinigten Königreich – schneller und vorschriftsmäßig
Wir unterstützen Hersteller bei der Registrierung von Medizinprodukten im Vereinigten Königreich, bei MHRA sowie bei Strategien zur UKCA-Zertifizierung, um einen konformen und zeitnahen Marktzugang im Vereinigten Königreich sicherzustellen.
Unsere Dienstleistungen im Bereich MHRA UKCA umfassen
Zugelassene Stelle für die Identifizierung und Zusammenarbeit im Vereinigten Königreich
Strategie zur UKCA-Kennzeichnung und Unterstützung bei der Zertifizierung
Leitfaden zum Regulierungsweg: Großbritannien vs. Nordirland
Technische Unterlagen und auditfähige Dokumentation
Übergang von CE zu UKCA und Lückenanalyse
Rechtsbeistand für Hersteller außerhalb des Vereinigten Königreichs
Registrierung und Meldung von Medizinprodukten bei MHRA
Geräteabdeckung
Medizinprodukte der Klassen I, IIa, IIb, III und IVD
Registrieren Sie sich bei MHRA
Einfache Einhaltung der britischen Vorschriften für Medizinprodukte
Die Einhaltung der britischen Vorschriften für Medizinprodukte kann nach dem Brexit komplex sein. Freyr macht es einfacher
Anforderungen für die Registrierung von Medizinprodukten in Großbritannien (UKCA)
Nordirland (CE / UKNI) – Verpflichtungen
UKCA-Zertifizierung
Marktüberwachung und Arzneimittelüberwachung


Schnellerer Markteintritt in Großbritannien bei minimiertem regulatorischem Risiko.
Dienstleistungen für die verantwortliche Person im Vereinigten Königreich (UKRP)
Beauftragen Sie vertrauensvoll eine für das Vereinigte Königreich zuständige Person. Hersteller mit Sitz außerhalb des Vereinigten Königreichs müssen eine für das Vereinigte Königreich zuständige Person (UKRP) benennen, um Medizinprodukte rechtmäßig in Großbritannien in Verkehr bringen zu können. Freyr kann als Ihr zuverlässiger UKRP fungieren.
Unser UKRP umfasst
Ernennung einer verantwortlichen Person im Vereinigten Königreich
UKRP Medizinprodukte und In-vitro-Diagnostika
MHRA
Unterstützung bei der Einhaltung von Kennzeichnungs- und Gebrauchsanweisungsvorschriften
Marktüberwachung und Arzneimittelüberwachung
Befugnis zur Kommunikation in Ihrem Namen
Leitfaden zu bevollmächtigten Vertretern: UKRP EU
- Eindeutige SLAs
- Transparente Preisgestaltung
- Spezialisierte Experten für britische Regulierungsfragen
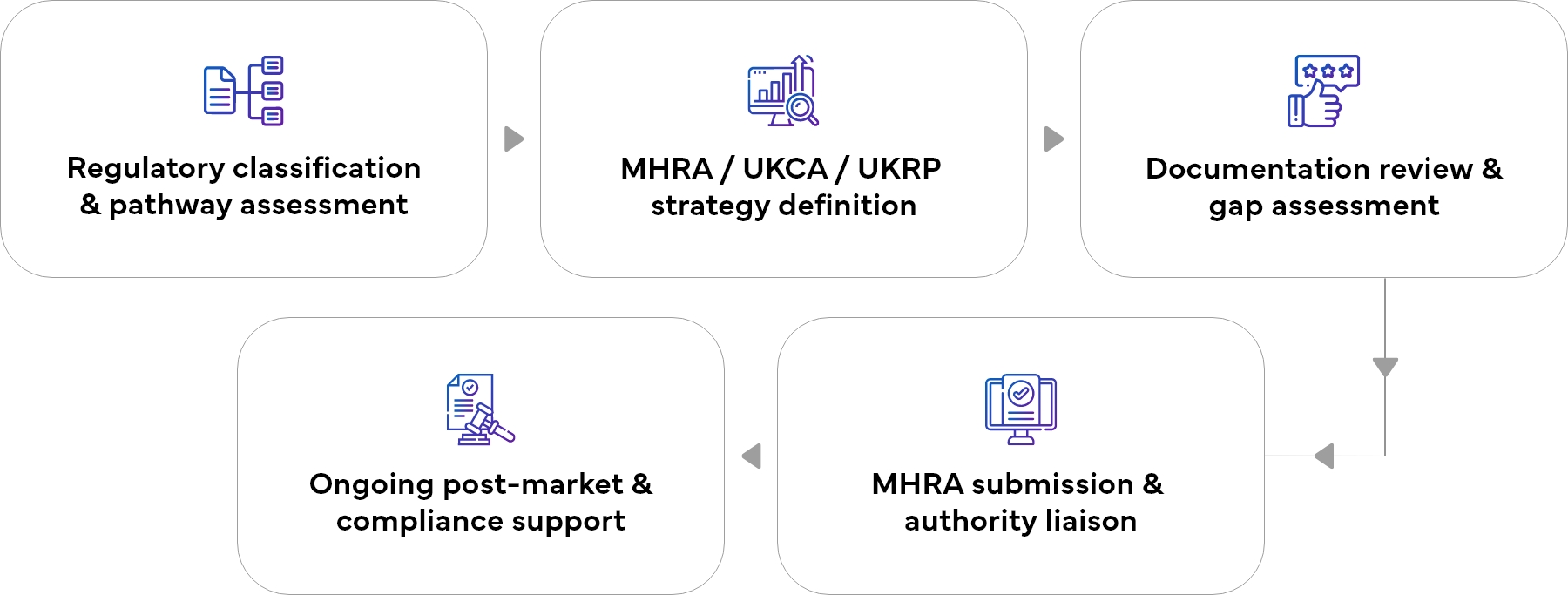
Unser Zulassungsverfahren für Medizinprodukte im Vereinigten Königreich
Ein vereinfachter, risikofreier Ansatz
Warum sollten Sie sich bei der Zulassung von Medizinprodukten in Großbritannien für Freyr entscheiden?

Bewährte Fachkompetenz im Bereich der britischen und EU-Rechtsvorschriften
Schnellere Genehmigungen durch fehlerfreie Anträge
Erfahrung mit Compliance-Verfahren in Großbritannien und Nordirland
Skalierbare Unterstützung für Start-ups und globale Hersteller
Ein einziger Ansprechpartner für Registrierungen im Vereinigten Königreich, in der EU und weltweit
Prüfungssichere, auf die Aufsichtsbehörden abgestimmte Dokumentation
Kompetenz in britischen Zulassungsfragen für alle Arten von Medizinprodukten
Wir unterstützen Anmeldungen für
Allgemeine Medizinprodukte
In-vitro-Diagnostika (IVD)
Software als Medizinprodukt (SaMD)
Kombinationsprodukte
 Über 20 Jahre Erfahrung im Bereich der weltweiten Regulierung
Über 20 Jahre Erfahrung im Bereich der weltweiten Regulierung Unterstützung bei der UKCA-Kennzeichnung und MHRA
Unterstützung bei der UKCA-Kennzeichnung und MHRA Verbindungsstelle der zugelassenen Stelle im Vereinigten Königreich
Verbindungsstelle der zugelassenen Stelle im Vereinigten Königreich Dienstleistungen für die verantwortliche Person im Vereinigten Königreich (UKRP)
Dienstleistungen für die verantwortliche Person im Vereinigten Königreich (UKRP) Regulierungswege in Großbritannien und Nordirland
Regulierungswege in Großbritannien und Nordirland Fachwissen zur Übergangsphase nach dem Brexit
Fachwissen zur Übergangsphase nach dem Brexit Spezialisten für britische Regulierungsfragen
Spezialisten für britische Regulierungsfragen Erfahrung in allen Klassen von Medizinprodukten
Erfahrung in allen Klassen von Medizinprodukten Zugelassene Stelle für die Identifizierung und Zusammenarbeit im Vereinigten Königreich
Zugelassene Stelle für die Identifizierung und Zusammenarbeit im Vereinigten Königreich Strategie zur UKCA-Kennzeichnung und Unterstützung bei der Zertifizierung
Strategie zur UKCA-Kennzeichnung und Unterstützung bei der Zertifizierung Leitfaden zum Regulierungsweg: Großbritannien vs. Nordirland
Leitfaden zum Regulierungsweg: Großbritannien vs. Nordirland Technische Unterlagen und auditfähige Dokumentation
Technische Unterlagen und auditfähige Dokumentation Übergang von CE zu UKCA und Lückenanalyse
Übergang von CE zu UKCA und Lückenanalyse Rechtsbeistand für Hersteller außerhalb des Vereinigten Königreichs
Rechtsbeistand für Hersteller außerhalb des Vereinigten Königreichs Registrierung und Meldung von Medizinprodukten bei MHRA
Registrierung und Meldung von Medizinprodukten bei MHRA




 Anforderungen für die Registrierung von Medizinprodukten in Großbritannien (UKCA)
Anforderungen für die Registrierung von Medizinprodukten in Großbritannien (UKCA) Nordirland (CE / UKNI) – Verpflichtungen
Nordirland (CE / UKNI) – Verpflichtungen UKCA-Zertifizierung
UKCA-Zertifizierung Marktüberwachung und Arzneimittelüberwachung
Marktüberwachung und Arzneimittelüberwachung Bewährte Fachkompetenz im Bereich der britischen und EU-Rechtsvorschriften
Bewährte Fachkompetenz im Bereich der britischen und EU-Rechtsvorschriften Erfahrung mit Compliance-Verfahren in Großbritannien und Nordirland
Erfahrung mit Compliance-Verfahren in Großbritannien und Nordirland Skalierbare Unterstützung für Start-ups und globale Hersteller
Skalierbare Unterstützung für Start-ups und globale Hersteller Ein einziger Ansprechpartner für Registrierungen im Vereinigten Königreich, in der EU und weltweit
Ein einziger Ansprechpartner für Registrierungen im Vereinigten Königreich, in der EU und weltweit Prüfungssichere, auf die Aufsichtsbehörden abgestimmte Dokumentation
Prüfungssichere, auf die Aufsichtsbehörden abgestimmte Dokumentation