Partenaire réglementaire de confiance pour les dispositifs médicaux au Royaume-Uni
Soutien pour le marquage UKCA et enregistrement auprès de la MHRA
Enregistrez votre dispositif médical au Royaume-Uni – Plus rapidement et en toute conformité
Nous aidons les fabricants pour l'enregistrement des dispositifs médicaux au Royaume-Uni, les soumissions à la MHRA et les stratégies de certification UKCA afin d'assurer un accès au marché britannique conforme et rapide.
Nos services MHRA et UKCA comprennent
Identification et liaison avec les organismes agréés au Royaume-Uni
Stratégie de marquage UKCA et soutien à la certification
Conseils sur les voies réglementaires pour la Grande-Bretagne et l'Irlande du Nord
Dossier technique et documentation prête pour l'audit
Transition du marquage CE au marquage UKCA et évaluation des écarts
Représentation légale pour les fabricants non-britanniques
Enregistrement et notification des dispositifs médicaux auprès de la MHRA
Couverture des dispositifs
Dispositifs médicaux de classe I, IIa, IIb, III et DIV
S'enregistrer auprès de la MHRA
Conformité des dispositifs médicaux au Royaume-Uni – Simplifiée
Gérer la conformité des dispositifs médicaux au Royaume-Uni peut être complexe après le Brexit. Freyr simplifie
Exigences d'enregistrement des dispositifs médicaux en Grande-Bretagne (UKCA)
Obligations en Irlande du Nord (CE / UKNI)
Certification UKCA
Surveillance et vigilance après commercialisation


Accès plus rapide au marché britannique avec un risque réglementaire minimisé.
Services de Personne Responsable au Royaume-Uni (UKRP)
Désignez un UK Responsible Person en toute confiance. Les fabricants non britanniques doivent désigner un UK Responsible Person (UKRP) pour commercialiser légalement leurs dispositifs sur le marché de Grande-Bretagne. Freyr peut être votre partenaire UKRP de confiance.
Nos services UKRP couvrent
Désignation d'un UK Responsible Person
UKRP pour les dispositifs médicaux et les DIV
Enregistrement auprès de la MHRA
Support à la conformité du Labelling et des notices d'utilisation (IFU)
Surveillance et vigilance après commercialisation
Communication avec les autorités en votre nom
Guide comparatif UKRP et Représentant Autorisé de l'UE
- Des accords de niveau de service (SLA) clairs
- Tarification transparente
- Des experts réglementaires dédiés au Royaume-Uni
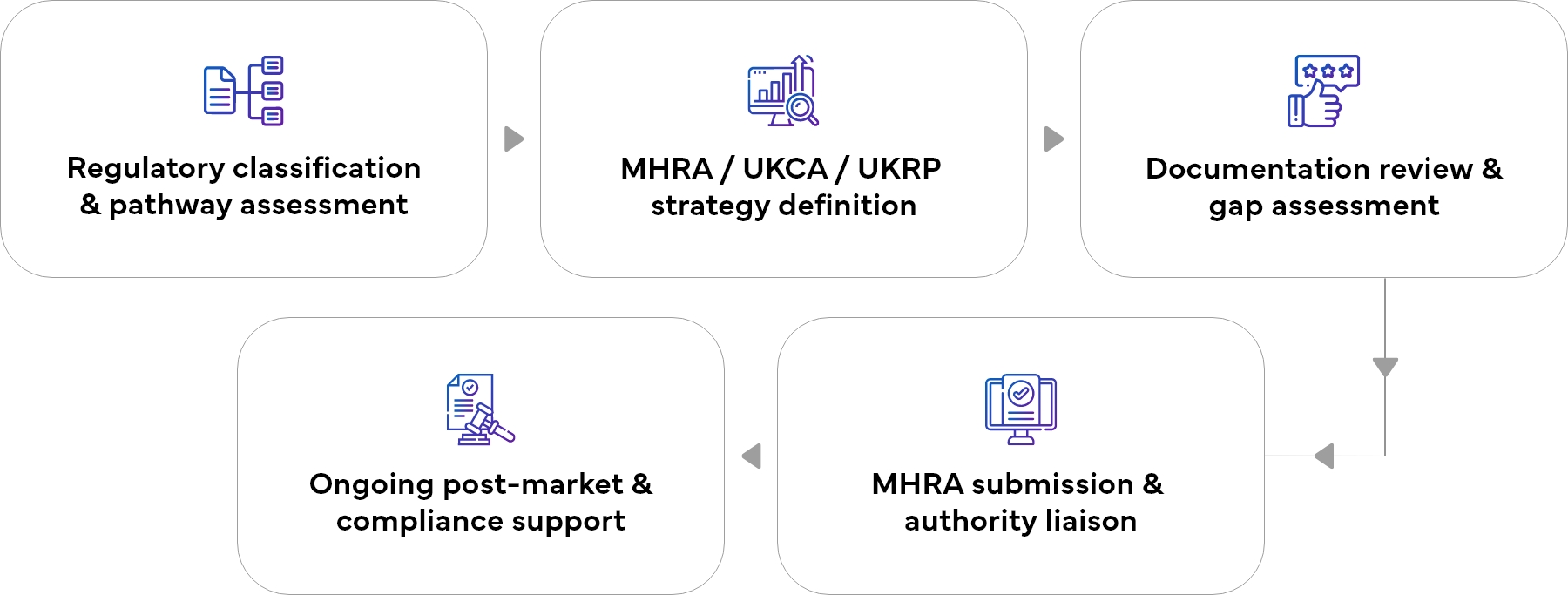
Notre processus d'enregistrement des dispositifs médicaux au Royaume-Uni
Une approche simplifiée et sans risque
Pourquoi choisir Freyr pour l'enregistrement des dispositifs médicaux au Royaume-Uni ?

Expertise réglementaire avérée au Royaume-Uni et dans l'UE
Approbations plus rapides grâce à des soumissions correctes dès le premier envoi
Expérience des voies de conformité pour la Grande-Bretagne et l'Irlande du Nord
Un accompagnement évolutif pour les startups et les fabricants mondiaux
Un partenaire unique pour les enregistrements au Royaume-Uni, dans l'UE et à l'échelle mondiale
Documentation prête pour l'audit et conforme aux exigences des régulateurs
Expertise réglementaire au Royaume-Uni pour tous les types de dispositifs
Nous accompagnons les enregistrements de
Dispositifs médicaux généraux
Dispositifs médicaux de diagnostic in vitro (DM DIV)
Logiciels considérés comme des dispositifs médicaux (SaMD)
Produits combinés
 Plus de 20 ans d'expertise réglementaire mondiale
Plus de 20 ans d'expertise réglementaire mondiale Soutien pour le marquage UKCA et enregistrement auprès de la MHRA
Soutien pour le marquage UKCA et enregistrement auprès de la MHRA Liaison avec les organismes agréés au Royaume-Uni
Liaison avec les organismes agréés au Royaume-Uni Services de Personne Responsable au Royaume-Uni (UKRP)
Services de Personne Responsable au Royaume-Uni (UKRP) Voies réglementaires pour la Grande-Bretagne et l'Irlande du Nord
Voies réglementaires pour la Grande-Bretagne et l'Irlande du Nord Expertise en matière de transition post-Brexit
Expertise en matière de transition post-Brexit Spécialistes réglementaires britanniques dédiés
Spécialistes réglementaires britanniques dédiés Expérience dans toutes les classes de dispositifs médicaux
Expérience dans toutes les classes de dispositifs médicaux Identification et liaison avec les organismes agréés au Royaume-Uni
Identification et liaison avec les organismes agréés au Royaume-Uni Stratégie de marquage UKCA et soutien à la certification
Stratégie de marquage UKCA et soutien à la certification Conseils sur les voies réglementaires pour la Grande-Bretagne et l'Irlande du Nord
Conseils sur les voies réglementaires pour la Grande-Bretagne et l'Irlande du Nord Dossier technique et documentation prête pour l'audit
Dossier technique et documentation prête pour l'audit Transition du marquage CE au marquage UKCA et évaluation des écarts
Transition du marquage CE au marquage UKCA et évaluation des écarts Représentation légale pour les fabricants non-britanniques
Représentation légale pour les fabricants non-britanniques Enregistrement et notification des dispositifs médicaux auprès de la MHRA
Enregistrement et notification des dispositifs médicaux auprès de la MHRA




 Exigences d'enregistrement des dispositifs médicaux en Grande-Bretagne (UKCA)
Exigences d'enregistrement des dispositifs médicaux en Grande-Bretagne (UKCA) Obligations en Irlande du Nord (CE / UKNI)
Obligations en Irlande du Nord (CE / UKNI) Certification UKCA
Certification UKCA Surveillance et vigilance après commercialisation
Surveillance et vigilance après commercialisation Expertise réglementaire avérée au Royaume-Uni et dans l'UE
Expertise réglementaire avérée au Royaume-Uni et dans l'UE Expérience des voies de conformité pour la Grande-Bretagne et l'Irlande du Nord
Expérience des voies de conformité pour la Grande-Bretagne et l'Irlande du Nord Un accompagnement évolutif pour les startups et les fabricants mondiaux
Un accompagnement évolutif pour les startups et les fabricants mondiaux Un partenaire unique pour les enregistrements au Royaume-Uni, dans l'UE et à l'échelle mondiale
Un partenaire unique pour les enregistrements au Royaume-Uni, dans l'UE et à l'échelle mondiale Documentation prête pour l'audit et conforme aux exigences des régulateurs
Documentation prête pour l'audit et conforme aux exigences des régulateurs