Socio de confianza en materia de Dispositivos Médicos en el Reino Unido
Asistencia para el marcado UKCA y MHRA
Registra tus Dispositivos Médicos el Reino Unido: más rápido y conforme a la normativa
Ayudamos a los fabricantes con Dispositivos Médicos en el Reino Unido Dispositivos Médicos , MHRA y las estrategias de certificación UKCA para garantizar un acceso al mercado británico que cumpla con la normativa y se produzca en los plazos previstos.
Nuestros servicios relacionados con MHRA el UKCA incluyen
Organismo autorizado en el Reino Unido para la identificación y la coordinación
Estrategia de marcado UKCA y asistencia en materia de certificación
Guía sobre el proceso regulatorio entre Gran Bretaña e Irlanda del Norte
Ficha técnica y documentación lista para auditoría
Transición del marcado CE al UKCA y evaluación de las deficiencias
Representación legal para fabricantes no británicos
Dispositivos Médicos y notificación deDispositivos Médicos ante MHRA
Compatibilidad con dispositivos
Productos sanitarios de las clases I, IIa, IIb, III y IVD
Registrarse en MHRA
Dispositivos Médicos en el Reino Unido: de forma sencilla
Navegar por Dispositivos Médicos en el Reino Unido puede resultar complejo tras el Brexit. Freyr lo simplifica
Requisitos para Dispositivos Médicos en el Reino Unido (UKCA)
Irlanda del Norte (CE / UKNI) Obligaciones
Certificación UKCA
Vigilancia y control poscomercialización


Una entrada más rápida en el mercado británico con un riesgo normativo mínimo.
Servicios de la persona responsable en el Reino Unido (UKRP)
Nombra con total confianza a una persona responsable en el Reino Unido. Los fabricantes no británicos deben designar a una persona responsable en el Reino Unido (UKRP) para poder comercializar legalmente sus productos sanitarios en el mercado de Gran Bretaña. Freyr puede actuar como tu UKRP de confianza UKRP .
Nuestros UKRP abarcan
Nombramiento de la persona responsable en el Reino Unido
UKRP productos sanitarios y diagnósticos in vitro
MHRA
Asistencia en materia de etiquetado y cumplimiento de las instrucciones de uso
Vigilancia y control poscomercialización
Comunicación oficial en su nombre
Orientaciones sobre el representante autorizado de UKRP la UE
- Acuerdos de nivel de servicio (SLA) claros
- Precios transparentes
- Expertos especializados en normativa del Reino Unido
Nuestro proceso Dispositivos Médicos en el Reino Unido
Un enfoque simplificado y sin riesgos
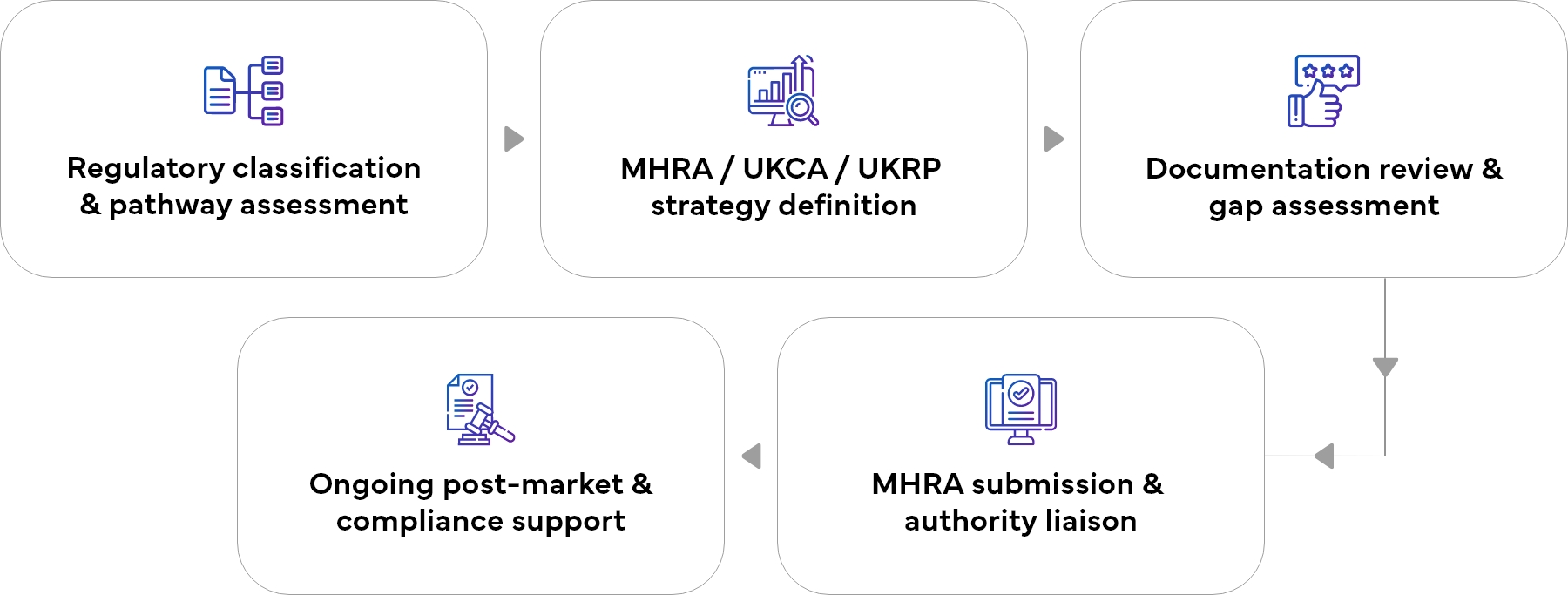
¿Por qué elegir Freyr para Dispositivos Médicos en el Reino Unido?

Experiencia contrastada en materia de normativa del Reino Unido y la UE
Aprobaciones más rápidas gracias a la presentación correcta desde el primer momento
Experiencia en los procedimientos de cumplimiento normativo en Gran Bretaña e Irlanda del Norte
Apoyo adaptable para startups y fabricantes internacionales
Un único socio para registros en el Reino Unido, la UE y el resto del mundo
Documentación preparada para auditorías y conforme a los requisitos normativos
Experiencia en materia de normativa británica para todo tipo de dispositivos
Aceptamos inscripciones para
Productos sanitarios generales
Productos para diagnóstico in vitro (IVD)
Software como Dispositivos Médicos SaMD)
Productos combinados
 Más de 20 años de experiencia en materia de normativa internacional
Más de 20 años de experiencia en materia de normativa internacional Asistencia para el marcado UKCA y MHRA
Asistencia para el marcado UKCA y MHRA Enlace con el organismo autorizado del Reino Unido
Enlace con el organismo autorizado del Reino Unido Servicios de la persona responsable en el Reino Unido (UKRP)
Servicios de la persona responsable en el Reino Unido (UKRP) Vías reglamentarias en Gran Bretaña e Irlanda del Norte
Vías reglamentarias en Gran Bretaña e Irlanda del Norte Experiencia en la transición tras el Brexit
Experiencia en la transición tras el Brexit Especialistas en normativa del Reino Unido
Especialistas en normativa del Reino Unido Experiencia en todas Dispositivos Médicos
Experiencia en todas Dispositivos Médicos Organismo autorizado en el Reino Unido para la identificación y la coordinación
Organismo autorizado en el Reino Unido para la identificación y la coordinación Estrategia de marcado UKCA y asistencia en materia de certificación
Estrategia de marcado UKCA y asistencia en materia de certificación Guía sobre el proceso regulatorio entre Gran Bretaña e Irlanda del Norte
Guía sobre el proceso regulatorio entre Gran Bretaña e Irlanda del Norte Ficha técnica y documentación lista para auditoría
Ficha técnica y documentación lista para auditoría Transición del marcado CE al UKCA y evaluación de las deficiencias
Transición del marcado CE al UKCA y evaluación de las deficiencias Representación legal para fabricantes no británicos
Representación legal para fabricantes no británicos Dispositivos Médicos y notificación deDispositivos Médicos ante MHRA
Dispositivos Médicos y notificación deDispositivos Médicos ante MHRA




 Requisitos para Dispositivos Médicos en el Reino Unido (UKCA)
Requisitos para Dispositivos Médicos en el Reino Unido (UKCA) Irlanda del Norte (CE / UKNI) Obligaciones
Irlanda del Norte (CE / UKNI) Obligaciones Certificación UKCA
Certificación UKCA Vigilancia y control poscomercialización
Vigilancia y control poscomercialización Experiencia contrastada en materia de normativa del Reino Unido y la UE
Experiencia contrastada en materia de normativa del Reino Unido y la UE Experiencia en los procedimientos de cumplimiento normativo en Gran Bretaña e Irlanda del Norte
Experiencia en los procedimientos de cumplimiento normativo en Gran Bretaña e Irlanda del Norte Apoyo adaptable para startups y fabricantes internacionales
Apoyo adaptable para startups y fabricantes internacionales Un único socio para registros en el Reino Unido, la UE y el resto del mundo
Un único socio para registros en el Reino Unido, la UE y el resto del mundo Documentación preparada para auditorías y conforme a los requisitos normativos
Documentación preparada para auditorías y conforme a los requisitos normativos