Aperçu de l'enregistrement des dispositifs médicaux en Colombie
La Colombie offre d'énormes opportunités aux entreprises de dispositifs médicaux. Son système de santé est réputé pour son engagement envers la sécurité des patients et la qualité des services médicaux. Il réglemente les dispositifs médicaux par l'intermédiaire de l'INVIMA (Institut national de surveillance des aliments et des médicaments). L'INVIMA est l'autorité opérationnelle pour l'enregistrement des dispositifs médicaux en Colombie.

Autorité réglementaire : INVIMA (Institut national de surveillance des aliments et des médicaments)
Réglementation : Décret 4725/2005
Voie réglementaire : Enregistrement des dispositifs
Représentant autorisé : Représentant légal en Colombie
Exigence SMQ:ISO 13485:2016 / MDSAP
Évaluation des données techniques : INVIMA
Exigences d'étiquetage : Les documents d'étiquetage doivent être en espagnol
Validité de la licence : 10 ans
Format de soumission : Électronique
Classification des dispositifs médicaux en Colombie
| Classification des dispositifs médicaux | |
|---|---|
| Classe I (Risque le plus faible) | |
| Classe IIa | |
| Classe IIb | |
| Classe III (Risque le plus élevé) | |
Représentant légal en Colombie
Pour être Représentant Légal en Colombie, il faut soit posséder la citoyenneté colombienne, soit disposer de l'autorisation légale nécessaire pour résider et travailler dans le pays en tant que ressortissant étranger. Un Représentant Légal peut assister et gérer toutes les procédures d'enregistrement en Colombie, agissant comme un lien entre l'entreprise et l'INVIMA, l'autorité réglementaire locale.
Enregistrement des dispositifs médicaux en Colombie
Les dispositifs médicaux et les DIV sont soumis à une procédure d'enregistrement. Par conséquent, les dispositifs médicaux doivent être enregistrés auprès de l'INVIMA pour être commercialisés en Colombie.
Pour commercialiser un dispositif médical en Colombie, il est nécessaire d'obtenir un Certificat de Libre Vente (CLV) ou un Certificat destiné à un gouvernement étranger (CFG), délivré par l'agence de réglementation compétente du pays d'origine ou d'un pays de référence reconnu (par exemple, le Canada, le Japon, l'Australie, l'Union européenne et les États-Unis). Le Certificat de Libre Vente ou le Certificat destiné à un gouvernement étranger atteste que le dispositif médical respecte les normes de sécurité et de qualité nécessaires à sa vente en Colombie.
Flux de processus
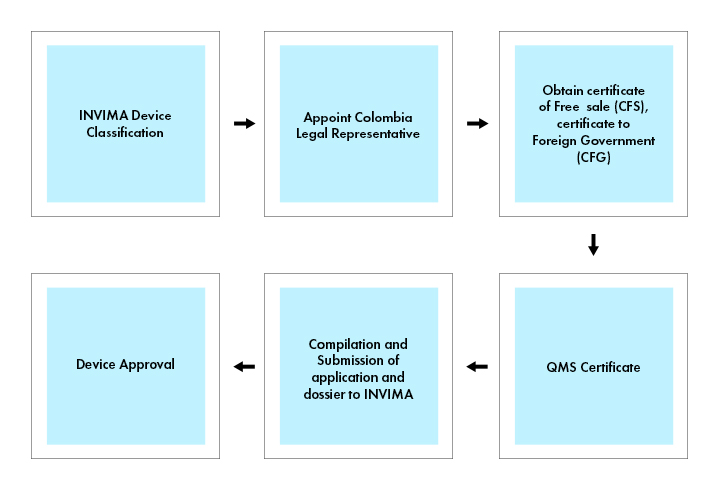
Gestion du cycle de vie des dispositifs post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-End du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des approbations et des enregistrements par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement des licences
- Assurer la liaison entre l'INVIMA et le fabricant
Résumé
| Classification des dispositifs médicaux | Nouvelles licences et renouvellements | ||
|---|---|---|---|
| Nouvel enregistrement | Amendement | Renouvellement | |
| Classe I | 4 à 6 mois | 2-3 mois | 4 à 6 mois |
| Classe IIa | 4 à 6 mois | 2-3 mois | 4 à 6 mois |
| Classe IIb | 4 à 6 mois | 2-3 mois | 4 à 6 mois |
| Classe III | 4 à 6 mois | 2-3 mois | 4 à 6 mois |
| Frais d'enregistrement | |||||
|---|---|---|---|---|---|
| Nouvelles licences et renouvellements | Modifications techniques | Modifications administratives | |||
| Classe I et Classe IIa | Classe IIb et Classe III | Classe I et Classe IIa | Classe IIb et Classe III | Classe I et Classe IIa | Classe IIb et Classe III |
| $ 690,00 | $ 776,00 | $ 196,00 | $ 196,00 | $ 153,00 | $ 153,01 |
L'expertise de Freyr
- Diligence raisonnable réglementaire
- Classification officielle
- Enregistrement des dispositifs
- Titulaire d'enregistrement en Colombie
- Support d'étiquetage
- Soutien à la traduction
- Identification et qualification des distributeurs
- Surveillance après commercialisation
- Gestion des changements post-approbation
- Renouvellement et transfert de licence
- Soumission et liaison avec l'INVIMA