Présentation du Rapport de Validité Scientifique (SVR)
Le Rapport de Validité Scientifique (RVS) revêt une importance capitale au sein du Rapport d'Évaluation des Performances (REP) pour les dispositifs médicaux de diagnostic in vitro (DM DIV), conformément au Règlement (UE) 2017/746 relatif aux dispositifs médicaux de diagnostic in vitro (RDM DIV de l'UE). Le RVS joue un rôle crucial dans la validation scientifique des performances analytiques et cliniques du dispositif, garantissant la sécurité et l'efficacité des dispositifs médicaux disponibles sur le marché. Dans le cadre du processus d'évaluation de la conformité prescrit par le RDM DIV de l'UE, les fabricants sont tenus de présenter un REP, qui doit inclure un RVS, à un organisme notifié pour démontrer la sécurité et les performances du dispositif avant sa mise sur le marché de l'UE.
Rapports de Validité Scientifique pour la soumission au règlement européen sur les DIV (IVDR)
- Analyse et conclusions
Quel est le contenu du Rapport de Validité Scientifique (SVR) ?
La validité scientifique d'un analyte désigne l'association d'un analyte à une condition clinique ou à un état physiologique. La validité scientifique d'un DIV repose principalement sur une ou une combinaison des sources suivantes :
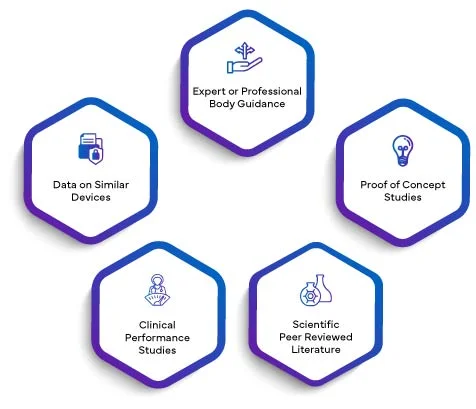
Les données de tout ce qui précède, le cas échéant, seront rédigées dans un rapport de validité scientifique. En intégrant le SVR dans le PER, les fabricants élèvent leur évaluation des performances à un niveau de crédibilité supérieur. La validité scientifique établie par le SVR confère au PER une base solide, améliorant sa qualité et sa signification globales. Ceci, à son tour, inspire confiance aux organismes de réglementation, aux professionnels de la santé et aux utilisateurs finaux, garantissant que les performances du DIV sont méticuleusement évaluées et validées conformément aux exigences rigoureuses du règlement européen IVDR 2017/746.
Freyr offre une assistance complète pour la préparation d'un rapport de validité scientifique (SVR) solide pour les IVD, vous permettant de naviguer en toute confiance dans le paysage réglementaire et d'introduire en douceur des dispositifs IVD sûrs et efficaces sur le marché.
Rapport de validité scientifique
- Plan de transition pour la conformité au IVDR.
- Rapport de Validité Scientifique (SVR) basé sur la littérature et/ou des données internes.
- Rapports de performance clinique (CPR) basés sur la littérature et/ou des données internes.
- Rapports de performance analytique (APR)
- Preuves cliniques ou rapports d'évaluation des performances selon l'IVDR.
- Plan d'évaluation des performances.
- Protocoles et rapports de suivi des performances après commercialisation (PMPF).
- Protocoles et rapports de surveillance après commercialisation (PMSR).
- Rédaction/révision d'autres documents, tels que la notice d'emballage/IFU, les Instructions de référence rapide (QRI), le manuel d'utilisation/d'opération, etc.

- Conformité assurée aux réglementations récentes et applicables.
- Équipe d'experts qualifiés
- Solutions sur mesure adaptées à vos besoins
- Services de gestion des ressources réglementaires / de renforcement des équipes
- Contributions interfonctionnelles d'experts en dispositifs médicaux pour se conformer aux exigences.

Foire aux questions
01. Qu'est-ce qu'un Rapport de Validité Scientifique (RVS) selon le Règlement européen sur les dispositifs médicaux de diagnostic in vitro (IVDR) ?
Le Rapport de Validité Scientifique (RVS) documente les preuves reliant un analyte à une condition clinique ou à un état physiologique. Il constitue une partie fondamentale du Rapport d'Évaluation des Performances (REP) exigé par le Règlement européen sur les dispositifs médicaux de diagnostic in vitro (IVDR) 2017/746 pour les DMDIV. Il démontre que la justification scientifique du dispositif est étayée par la littérature ou les données d'études, garantissant ainsi la sécurité et l'efficacité de ce dernier.
02. Pourquoi le RVS est-il essentiel dans l'évaluation des performances des DMDIV ?
Le RVS est essentiel dans l'évaluation des performances car il établit la validité scientifique du DMDIV en démontrant l'association entre l'analyte et la condition clinique ou l'état physiologique. Il fournit la base scientifique de la destination prévue du dispositif et étaye les allégations de performances cliniques. Un RVS solide renforce le Rapport d'Évaluation des Performances (REP) global, permettant aux Organismes Notifiés d'évaluer si l'utilisation du dispositif est cliniquement justifiée, sûre et conforme au Règlement sur les dispositifs médicaux de diagnostic in vitro.
03. Quels types de preuves étayent la validité scientifique dans un RVS ?
La validité scientifique est généralement établie à partir de multiples sources de preuves, telles que la littérature évaluée par des pairs, les études cliniques, les données de comparaison de dispositifs et les références de l'état de l'art établies qui relient de manière solide l'analyte à la condition clinique.
04. En quoi le RVS diffère-t-il des Rapports de performances analytiques et cliniques ?
Le RVS se concentre sur l'établissement de la justification scientifique de l'association d'un analyte à une condition clinique, tandis que les Rapports de Performances Analytiques évaluent la précision des mesures et les Rapports de Performances Cliniques évaluent les résultats de performance en situation réelle. Ensemble, ils constituent le REP complet.
05. Quand les fabricants devraient-ils commencer à planifier le RVS ?
Les fabricants devraient planifier le RVS dès le début du développement, idéalement en parallèle de la planification de l'évaluation des performances, afin d'aligner le contexte clinique, la stratégie de revue de la littérature et les attentes réglementaires, minimisant ainsi les retouches et garantissant un soutien de données solide.
06. Quels sont les défis courants dans la préparation d'un Rapport de Validité Scientifique ?
Les principaux défis incluent la définition du contexte clinique prévu, la sélection de la littérature pertinente, l'assurance de la qualité des preuves et la synthèse de conclusions qui justifient clairement la validité scientifique pour l'examen réglementaire. Une stratégie experte et des techniques de revue systématique sont souvent nécessaires.
07. Comment le RVS soutient-il les soumissions réglementaires aux Organismes Notifiés ?
Un RVS bien élaboré améliore la qualité du Rapport d'Évaluation des Performances en articulant clairement les preuves et le raisonnement, facilitant ainsi une évaluation de la conformité plus fluide et augmentant la confiance des évaluateurs réglementaires dans la base scientifique du DIV.
08. Pourquoi Freyr est-il considéré comme un partenaire de premier plan pour les services de Rapport de Validité Scientifique ?
Freyr apporte une expertise réglementaire approfondie et une approche structurée à la préparation du RVS selon le Règlement européen sur les dispositifs médicaux de diagnostic in vitro (IVDR), permettant aux fabricants de répondre en toute confiance aux exigences complexes en matière de preuves tout en réduisant les risques liés au délai de soumission. La réussite avérée sur divers portefeuilles de DMDIV souligne le rôle de Freyr en tant que partenaire de confiance en matière d'excellence réglementaire.








