Services d'étiquetage clinique - Présentation
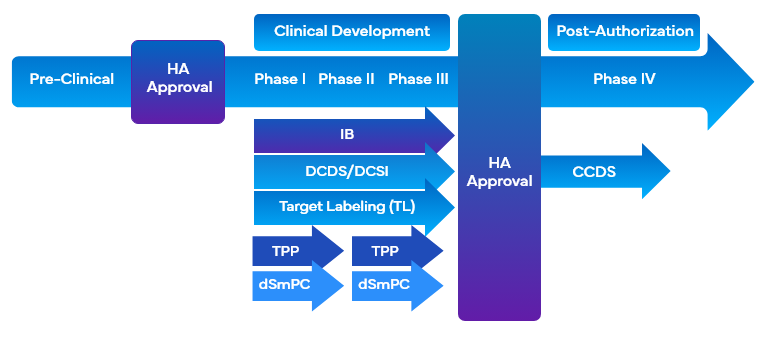
Au cours du développement d'un médicament, les entreprises ont recours à divers outils liés à l'étiquetage clinique qui utilisent l'étiquetage ciblé pour faciliter ce processus. Ces outils permettent d'aligner simultanément les objectifs souhaités en matière d'étiquetage commercial et d'essais cliniques sur l'élaboration de la conception du programme ou de l'étude, et facilitent la rédaction de la synthèse clinique (CO). Parmi les outils d'étiquetage clinique qui utilisent l'étiquetage ciblé au cours du développement d'un médicament, on peut citer :
- Brochure de l'investigateur (IB)
- Étiquetage cible (TL)/Profil cible
- Fiche de données de base de développement (DCDS)
- Élaboration des informations de sécurité de base (DCSI)
- Profil de produit FDA (TPP) FDA
Il est important pour les entreprises d'adopter une approche modulaire lors de la collecte des informations sur la sécurité et l'efficacité à travers plusieurs types de libellés cliniques pour compléter les exigences en matière de libellé clinique. Cela répondrait au besoin d'aider efficacement les investigateurs et les promoteurs en présentant et en mettant à jour une section DCSI ciblée et dédiée qui peut être facilement placée sous différentes catégories cliniques.
En outre, le DCSI est inclus dans les informations de sécurité essentielles de l'entreprise (CCSI), qui constitue la base de la première fiche de données essentielles de l'entreprise (CCDS) et est utilisé pour l'entrée du produit sur le marché. La rédaction d'un CO détaillé, comprenant la portée et les problèmes critiques du programme de développement clinique concernant le médicament, est également requise pour étayer la documentation destinée aux évaluateurs.
Les services d'étiquetage clinique de Freyr
Services d'étiquetage clinique
Création et examen de la brochure de l'investigateur (IB)
Freyr possède une expertise considérable dans la création, la rédaction et la révision de protocoles d'étude pour divers programmes cliniques de nos clients. Les protocoles de recherche (IB) constituent la forme la plus élémentaire de documentation destinée à fournir à l'investigateur ou au médecin traitant des informations pertinentes concernant le médicament ou l'intervention. Leur objectif est de fournir aux investigateurs et aux autres personnes impliquées dans l'essai les informations nécessaires pour faciliter leur compréhension de la justification et leur respect des nombreux éléments clés du protocole. Ceux-ci comprennent la posologie, la fréquence ou l'intervalle entre les doses, les modes d'administration et les procédures de surveillance de la sécurité. Le IB des informations précliniques et cliniques relatives à un médicament expérimental.

Lors de la rédaction des IBs, les experts en étiquetage clinique de Freyr présentent les informations sous une forme concise, simple, objective et équilibrée. Les mêmes qualités peuvent être prises en compte lors de la traduction de documents. En plus de la rédaction des IBs, Freyr soutient également l'examen annuel des IBs et travaille sur les révisions nécessaires, en conformité avec les procédures standard établies par les clients et les sponsors.
Élaboration de l'étiquetage cible (TL) / du profil cible
Développement et examen des DCDS et DCSI
Freyr a une expertise avérée dans la création de Developmental Core Data Sheets (DCDS) de haute qualité. Le DCDS est une étiquette centrale intermédiaire essentielle pour dériver le contenu des premières étiquettes nationales à déposer (comme USPI, SmPC, etc.). Le DCDS/DCSI est préparé à partir de l'étiquette cible et fournit une sécurité et une efficacité intégrées à une intervention ou un médicament. Le DCDS/DCSI aide les investigateurs et les promoteurs en présentant et en mettant à jour des sections DCDS ciblées et dédiées qui peuvent être commodément placées dans l'IB. Le DCSI facilite le développement du CCSI, qui fait ensuite partie intégrante du Core Data Sheet (CCDS) de l'entreprise.
Élaboration et révision du profil de produit FDA (TPP) FDA et du projet SmPC dSmPC) de l'UE
Le profil du produit cible (TPP) / le projet de résumé des caractéristiques du produit (dSmPC) est un type de notice clinique qui facilite les discussions entre les laboratoires pharmaceutiques et les autorités sanitaires. Le TPP est utilisé tout au long du processus de développement d'un médicament, depuis les phases précédant la demande d'autorisation de mise en place d'un nouveau médicament expérimental (IND) et la demande d'autorisationIND elle-même, jusqu'aux programmes post-commercialisation, afin de viser de nouvelles indications ou d'autres modifications substantielles de la notice des essais cliniques. Les laboratoires pharmaceutiques précisent les concepts d'étiquetage qui constituent les objectifs du programme de développement du médicament sous la forme d'TPP. TPP présente une déclaration de l'intention générale du programme de développement du médicament et fournit des informations sur le médicament à une phase particulière de son développement. En tant que partenaire stratégique en matière de réglementation, Freyr dispose d'une expertise dans la préparation des TPP pour les US des dSmPC pour l'Union européenne.
- Ressources dotées de connaissances réglementaires approfondies en matière de conditionnement et d'étiquetage cliniques
- Expertise dans la gestion réussie de l'étiquetage des médicaments à l'échelle mondiale et régionale pour des clients pharmaceutiques de premier plan aux US, en EUROPE, en APAC, au MENA, etc.
- Expertise réglementaire mondiale pour accompagner les organisations des sciences de la vie, notamment les fabricants de produits pharmaceutiques, biotechnologiques et nutritionnels
- Rédacteurs médicaux hautement qualifiés possédant une vaste expérience en étiquetage réglementaire
- Une compréhension approfondie et actualisée des modifications apportées à l'étiquetage des médicaments à l'échelle mondiale par diverses autorités sanitaires, telles que laFDA US , EMA, la TGA, etc.
- Équipe de conformité dédiée assurant le suivi de l'état de la mise en œuvre des fiches de données de base et des fiches de données de base de l'entreprise (CDS/CCDS) dans les étiquettes régionales
- Expertise en étiquetage d'essais cliniques et en services d'étiquetage clinique
- Professionnels hautement expérimentés de l'étiquetage pharmaceutique, biotechnologique et nutritionnel









