Présentation générale du système FDA de la FDA
L'initiative FDA a été mise en place pour améliorer l'efficacité et l'uniformité dans la préparation et l'évaluation des demandes FDA (k), De Novo et PMA FDA . S'inspirant de l'approche initiale eSubmitter, qui concernait la soumission électronique des demandes relatives aux dispositifs médicaux et aux dispositifs de diagnostic in vitro (IVD), le programme eSTAR a été créé en s'appuyant sur l'expérience acquise précédemment FDA. La FDA un programme distinct appelé « Electronic Submission Template and Resource (eSTAR) Pilot Program ». Les demandes 510(k) doivent obligatoirement être soumises via eSTAR depuis le 1er octobre 2023 ; les demandes De Novo (sauf exemption) doivent obligatoirement être soumises via eSTAR depuis le 1er octobre 2025. Les modèles sont accessibles en ligne, mais l'utilisation d'identifiants FDA est nécessaire pour le processus de soumission proprement dit.
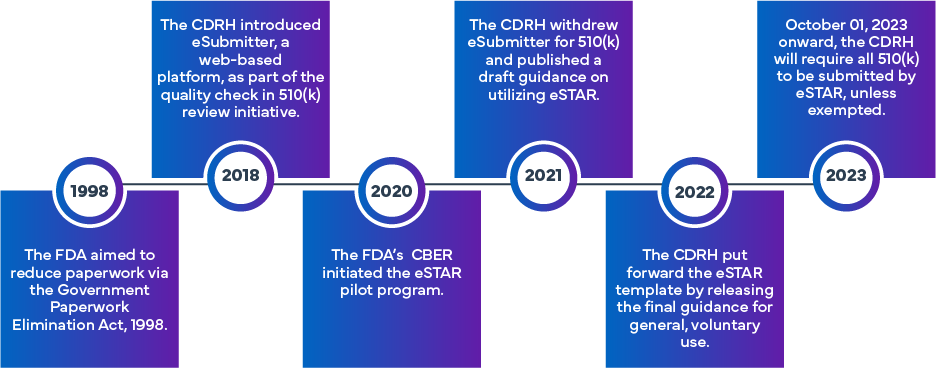
Qu'est-ce que FDA ?
L'eSTAR est un modèle PDF interactif conçu pour faciliter la préparation d'un dossier complet de demande d'autorisation de mise sur le marché d'un dispositif médical auprès de la FDA Les demandeurs peuvent également utiliser l'eSTAR pour transmettre leurs réponses aux demandes d'informations complémentaires FDA. Son objectif est d'améliorer la qualité des dossiers relatifs à divers dispositifs médicaux en garantissant que les demandeurs fournissent des données complètes et de haute qualité pour l'examen préalable à la mise sur le marché FDA.
En adoptant le format eSTAR, les déclarants peuvent être assurés que leurs dossiers sont complets, ce qui permettra à la FDA mener plus efficacement ses examens préalables à la mise sur le marché et FDA garantir un accès rapide à des dispositifs médicaux sûrs et efficaces. Le modèle eSTAR est disponible gratuitement et peut être utilisé par tous les déclarants de dispositifs médicaux pour les demandes 510(k) et De Novo, ainsi que, sur une base volontaire, pour les soumissions Q et les soumissions de suppléments à l'avis de 30 jours PMA adressées à la FDA. Il existe deux types de modèles eSTAR : l'un pour les dispositifs médicaux et l'autre pour les dispositifs de diagnostic in vitro (IVD). PreSTAR beta a évolué ; utilisez les derniers modèles de soumission Q via le portail de collaboration client (CCP) du CDRH. Le modèle eSTAR 6.0 pour les soumissions De Novo/510(k) non-IVD sera publié en octobre 2025.
Caractéristiques et limites des soumissions eSTAR
Bien que le programme eSTAR propose un formulaire PDF interactif conçu pour aider les demandeurs à élaborer des dossiers complets pour les dispositifs médicaux et les DIV, il présente à la fois des avantages et des inconvénients. Les demandeurs doivent comprendre ces avantages et ces limites afin de pouvoir prendre des décisions éclairées concernant l'intégration d'eSTAR dans leur processus de soumission. Dans le tableau ci-dessous, nous explorerons les caractéristiques et les restrictions du programme eSTAR.

Considérations pour une utilisation efficace d'eSTAR
Une caractéristique avantageuse du modèle eSTAR, qui contribue à l'optimisation du processus de soumission, est l'intégration automatisée des réglementations pertinentes et des normes reconnues pour la citation. Cela accélère non seulement le processus de soumission en réduisant la saisie manuelle de données, mais atténue également la possibilité d'erreurs humaines qui pourraient survenir lors de la saisie des réglementations et des normes. Grâce à une construction guidée pour chaque section de soumission, l'utilisation d'eSTAR dans le processus de soumission peut être simplifiée sans effort.
- La FDA d'utiliser Adobe Acrobat Pro ou Foxit PDF Editor pour modifier les modèles eSTAR.
- eSTAR intègre certains formulaires, éliminant ainsi la nécessité de les remplir séparément. Ceux-ci comprennent le formulaire 3514 (la page de couverture de la soumission) et le formulaire 3881 (indications d'utilisation). De plus, la déclaration véridique et exacte, qui était auparavant requise sur le papier à en-tête d'une entreprise, est désormais intégrée à eSTAR.
- eSTAR prend en charge divers formats de pièces jointes au-delà des simples PDF, tels que les feuilles de calcul Excel et les fichiers vidéo (mp4).
- Les fichiers aux formats avec macros et exécutables ne sont pas autorisés.
- La taille totale du fichier PDF eSTAR, ainsi que de ses pièces jointes, ne doit pas dépasser 1 Go, car les fichiers de plus de 4 Go ne seront pas acceptés.
- Si vos fichiers électroniques dépassent les limites techniques, vous pouvez envoyer le dossier numérique au Centre de contrôle des documents (DCC) du CDRH par courrier.
Bonnes pratiques pour la préparation des soumissions eSTAR
L'application de certaines des meilleures pratiques pour la préparation des soumissions eSTAR peut aider les demandeurs à simplifier le processus de soumission et à améliorer leurs chances de succès. Voici quelques-unes des meilleures pratiques :
- Respectez les FDA :la FDA des recommandations destinées à aider les demandeurs à utiliser correctement le modèle eSTAR. Le respect de ces recommandations garantit que les demandes sont conformes aux exigences et aux attentes FDA.
- Veiller à ce que le dossier soit complet :le modèle eSTAR guide les candidats à travers les informations essentielles à fournir. Les candidats doivent fournir toutes les informations requises afin de réduire au minimum les risques de lacunes ou de demandes d'informations complémentaires.
- Assurer la cohérence :le modèle eSTAR favorise l'uniformité du contenu et de la structure des dossiers de demande 510(k). La structure guidée de chaque section du dossier facilite l'extraction des informations relatives à un dispositif médical.
- Privilégiez la clarté :fournissez des informations claires et concises dans vos déclarations eSTAR afin de faciliter un processus d'examen fluide. Ce niveau de détail et de précision permet de réduire les retards et les erreurs, tout en garantissant un accès rapide aux déclarations préalables à la mise sur le marché des dispositifs médicaux.
- Précision et sécurité :la vérification automatique des informations contenues dans chaque section des soumissions eSTAR permet de réduire les retards dans l'examen et de limiter les éventuelles lacunes.
Importance du code couleur dans les soumissions FDA
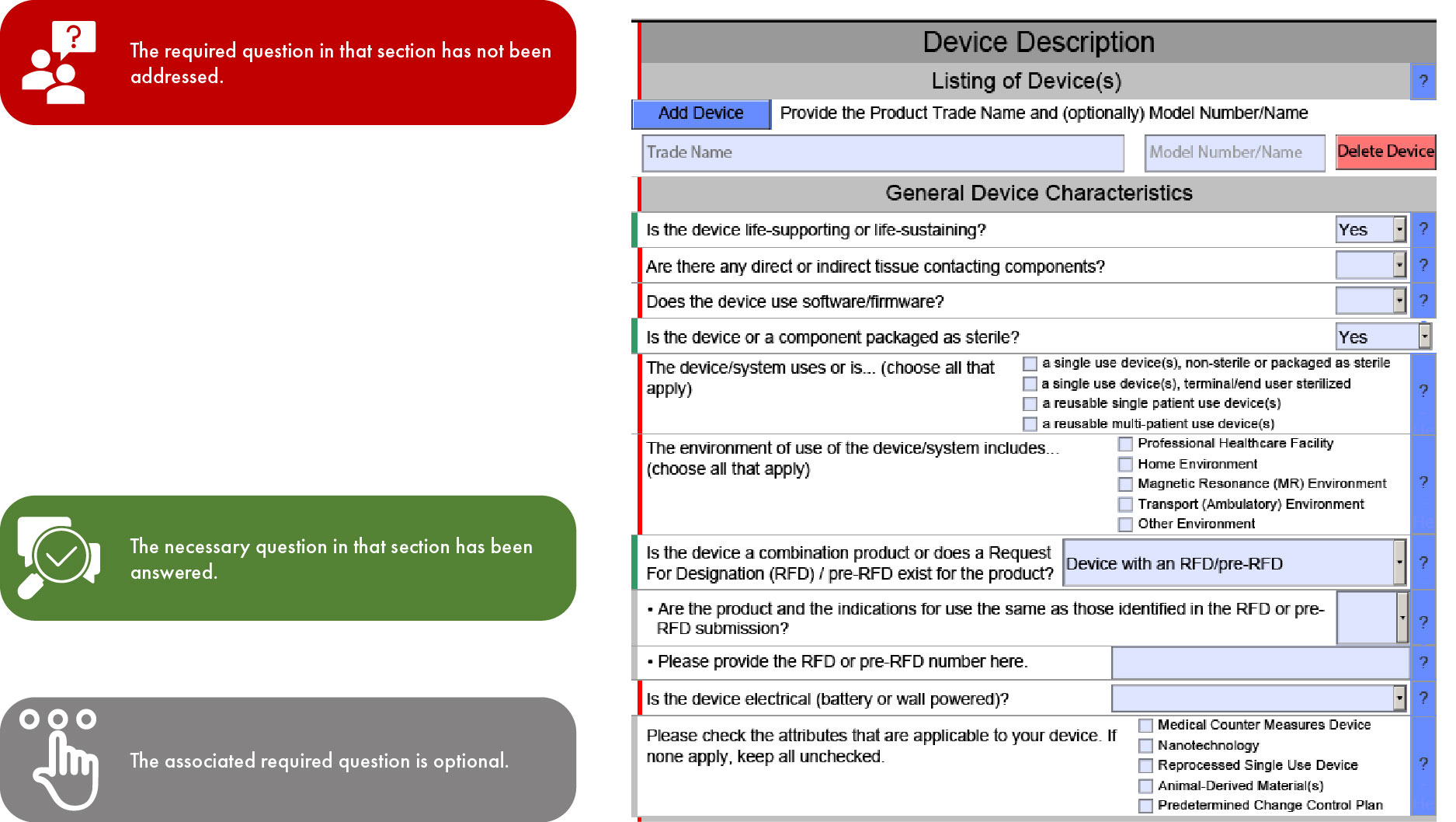
eSTAR étant obligatoire pour les demandes 510(k) à compter du 1er octobre 2023 et pour les demandes De Novo à compter du 1er octobre 2025, le parcours du modèle à travers les différentes sections est déterminé par le type de demande. Cette rationalisation facilite un examen plus rapide par laFDA US , réduisant ainsi au minimum les incohérences et les omissions dans votre dossier. Il est toutefois important de noter que la FDA retarder son examen si les traductions en anglais des documents fournis font défaut.

Aligner vos pièces jointes
Examinez le modèle eSTAR au préalable pour comprendre comment les pièces jointes sont divisées et vous assurer que vos documents correspondent aux sections des pièces jointes. Cette étape est cruciale, en particulier pour les entreprises ayant déjà soumis des 510(k), car votre approche actuelle en matière d'organisation des documents pourrait nécessiter des ajustements. Cela pourrait également impliquer d'extraire du contenu des pièces jointes.
- eSTAR exige des pièces jointes concises, différentes des soumissions traditionnelles.
- Prévoyez de nombreuses pièces jointes, potentiellement des dizaines.
- Les pièces jointes permettent d'inclure des données telles que des feuilles de calcul Excel, des fichiers vidéo MP4, des documents Word, des fichiers JPEG, etc.
- eSTAR exige l'indication des numéros de page pour les informations relatives aux pièces jointes, mais ne recommande pas l'utilisation d'une liste de contrôle des motifs de refus conformément FDA .
Modèles : les modèles de la dernière version 6.0 sont disponibles ; la version 5 est acceptée pour les soumissions en cours : fda.
L'avenir d'eSTAR.
Il est prévu que le système eSTAR fasse l'objet de mises à jour une fois que les documents d'orientation applicables auront été finalisés. Grâce à ces mises à jour, le fabricant pourra se référer aux versions les plus récentes publiées par laFDA US .
Santé Canada (SC) a lancé une initiative pilote visant à utiliser eSTAR pour les dispositifs de classe III et IV. Il existe une conjecture selon laquelle d'autres nations pourraient suivre l'exemple du Canada en rendant l'adoption d'eSTAR discrétionnaire, en particulier au sein du consortium IMDRF. Cependant, il convient de noter qu'aucune déclaration explicite n'a été faite à cet égard.
Pourquoi choisir Freyr ?
Freyr s'appuie sur une vaste expertise acquise grâce à sa participation à de nombreux projets axés sur les demandes d'autorisation auprès de la FDA le passé. En proposant deux voies distinctes pour aider de manière proactive le secteur à accélérer les demandes 510(k) et De Novo, Freyr offre une gamme de services aux clients, qui comprend une liste exhaustive des documents de demande essentiels et des informations requises, la réalisation d'analyses minutieuses des lacunes dans la documentation, la compilation des demandes via eSTAR et la finalisation du dossier de demande préalable à la mise sur le marché destiné à la FDA. De plus, Freyr étend son soutien aux activités post-soumission, telles que la fourniture d'informations supplémentaires et l'examen des réponses de l'industrie à toute demande d'informations complémentaires formulée par la FDA.
Comment Freyr peut-il vous aider ?
Freyr propose un accompagnement utile pour la préparation des soumissions 510(k) et De Novo. Les services comprennent :
- Support pour le parcours réglementaire : Cela implique l'identification du code produit, du nom et du numéro de la réglementation, des dispositifs prédicats/de référence potentiels, des tests de performance, ainsi que des normes applicables et des documents d'orientation pertinents pour le dispositif spécifique en question.
- Assistance pour les demandes Q (demandes préalables) : cela consiste à vous aider à clarifier les questions relatives aux conditions préalables à une demande de mise sur le marché, à organiser la demande, à préparer une FDA avec FDA , à dialoguer de manière interactive avec la FDA la réunion et à rédiger le compte-rendu de la réunion.
L'expertise du programme FDA de FDA
- Stratégie FDA globale FDA .
- Identification du dispositif de référence.
- Établir l'équivalence substantielle avec un dispositif de référence.
- Analyse des écarts en matière de FDA .
- Compilation de vingt et une (21) sections du dossier technique 510(k).
- Publication et création de l'eCopy.
- Validation et soumission de l'eCopy.
- Services de liaison pour l'approbation des dispositifs.
- Le traitement de la réponse RTA et des lacunes.
- Services de consultation pour remédier aux déficiences.
- Enregistrement des dispositifs et maintenance de la base de données FURLS.