Le marché nord-américain des dispositifs médicaux est l'un des plus attractifs et des plus réglementés au monde. Aux États-Unis, l'enregistrement des dispositifs médicaux est supervisé par la FDA, principalement par l'intermédiaire du Center for Devices and Radiological Health (CDRH), tandis qu'au Canada, il est régi par Santé Canada dans le cadre d'un système fondé sur l'évaluation des risques.
Pour les fabricants, s'y retrouver sur ces marchés peut s'avérer complexe. Les deux pays s'appuient sur une classification des dispositifs médicaux fondée sur les risques (classes I, II, III et, au Canada, classe IV), étayée par des preuves solides en matière de sécurité et de performance ainsi que par un système de gestion de la qualité (SGQ) conforme. Des programmes tels que MDSAP des normes comme ISO 13485, associés à des différences de terminologie, de procédures et d'exigences en matière de documentation, ajoutent encore à la complexité lors de la planification de l'entrée sur les marchés US canadien.
Freyr aide les fabricants à transformer cette complexité en un plan clair et concret pour accéder aux marchés US canadien. Nous comprenons les recoupements entre FDA et la réglementation de Santé Canada en matière de dispositifs médicaux, et nous vous aidons à harmoniser les classifications, les données justificatives, le système de gestion de la qualité et les dossiers afin que vous puissiez suivre une stratégie unique et efficace pour les autorisations, les lancements et la conformité à long terme dans les deux pays.
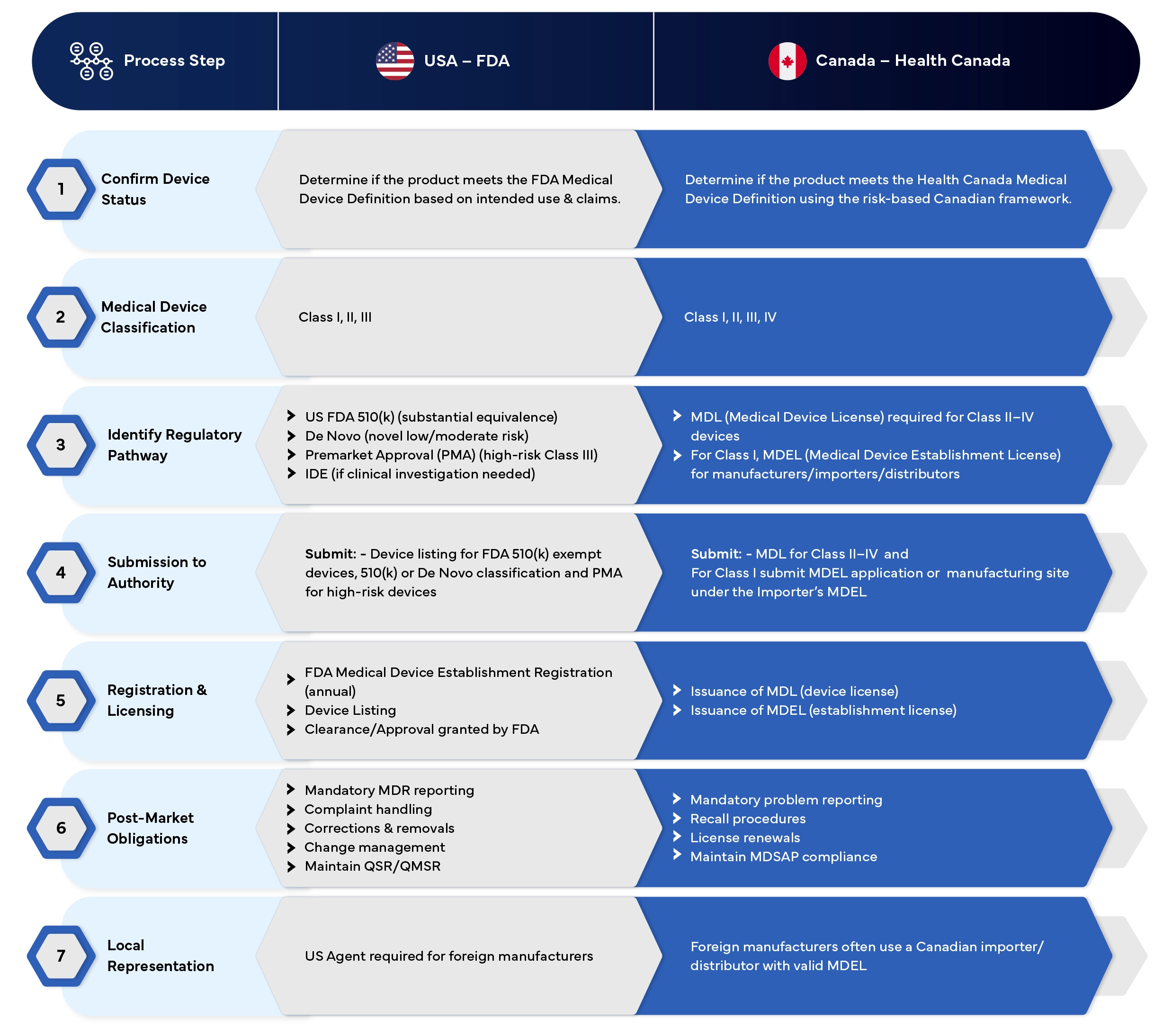
États-Unis contre Canada
Processus d'enregistrement des dispositifs médicaux - Tableau comparatif
Les services d'enregistrement de dispositifs médicaux de Freyr
Enregistrement des dispositifs médicaux dans les Amériques
- Soutien en veille réglementaire et de marché
- Classification des produits conformément aux exigences réglementaires
- Enregistrement des dispositifs médicaux aux ÉTATS-UNIS - 513 (G) et (La bonne voie parmi 510 (K)/De-NOVO/PMA/IDE)
- Réunion de pré-soumission avec les agences de santé
- Soutien réglementaire pour les documents de produit, tels que le Dossier historique de conception (DHF)
- Analyse des écarts des documents techniques et des systèmes de Bonnes Pratiques de Fabrication (BPF)
- Soutien réglementaire pour la compilation de dossiers techniques, tel que requis par la voie d'enregistrement respective
- Stratégie de conformité du système qualité de l'USFDA (21 CFR 820)
- Services de conformité au Programme d'audit unique des dispositifs médicaux (MDSAP)
- Enregistrement des dispositifs médicaux au Canada - Enregistrement de la Licence de dispositif médical (MDL) et de la Licence d'établissement de dispositifs médicaux (MDEL)
- Liaison et soutien avec l'Agence de santé
- Représentation locale – Services d'agent US et de personne responsable sanitaire
- Activités de conformité post-approbation

- Soumissions réussies pour diverses classes de dispositifs, allant des logiciels aux sutures
- Accès à une filiale locale pour relever les défis de l'autorité et les exigences linguistiques spécifiques
- Personnel dédié et expert pour fournir un soutien réglementaire aux dispositifs médicaux et aux DIV
- Modèle économique pour le support de représentation locale ou légale
- Ont réalisé avec succès divers projets aux US et au Canada
- Basé aux US

Pourquoi collaborer avec Freyr ?
- Une expertise réglementaire End-to-end Amérique End-to-end , couvrant tous les aspects, depuis les notifications préalables à la mise sur le marché (dossiers) auprès de FDA de Santé Canada jusqu'à la surveillance post-commercialisation et la conformité tout au long du cycle de vie du produit.
- Une expérience éprouvée avec plus de 1 500 enregistrements de dispositifs médicaux à l'échelle mondiale, couvrant les dispositifs de classe I à III aux US de classe I à IV au Canada.
- Une présence sur le terrain grâce à des services US et à un accompagnement réglementaire au Canada, le tout soutenu par des équipes d'experts réparties dans le monde entier pour une exécution sans faille.
- Une stratégie intégrée US le Canada qui rationalise les exigences en matière de données probantes, de documentation et de qualité afin de réduire les coûts, les doublons et les délais d'approbation.
- Une collaboration directe avec FDA Santé Canada, garantissant une communication claire, des réponses rapides et une adaptation proactive aux exigences réglementaires.
- Plus de 470 fabricants de dispositifs médicaux à travers le monde, des start-ups aux multinationales, nous font confiance en tant que partenaire réglementaire de longue date pour l'Amérique du Nord.












