Évolution des génériques - Aperçu.
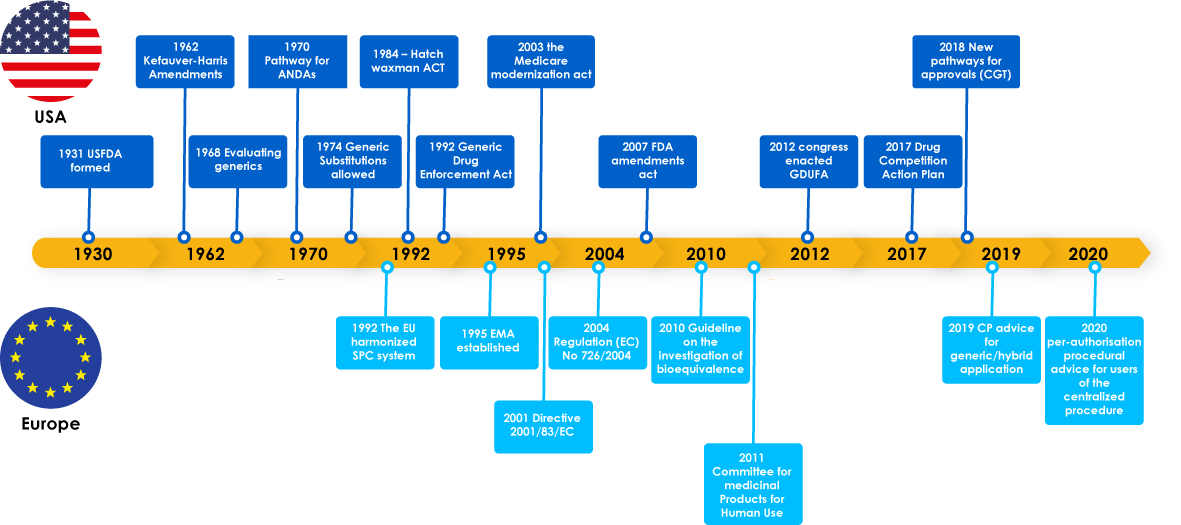
Les médicaments génériques ont franchi des étapes importantes, notamment des lois réglementaires visant à soutenir leur développement, ce qui a encouragé les fabricants à explorer le marché des génériques. Ces législations ont également donné aux médecins la confiance nécessaire pour prescrire un substitut aux médicaments de marque, ce qui a finalement bénéficié aux patients, car les fabricants de génériques ont répondu aux besoins essentiels des patients dans le monde entier.
FAQ sur les génériques
Q1: Que sont les médicaments génériques ?
Rép. : Les médicaments génériques sont des produits pharmaceutiques, qui sont des copies identiques du médicament d'origine et ont le même API, dosage, utilisation prévue, effets secondaires, voie d'administration, risques, sécurité et puissance que le médicament innovant, mais ils peuvent différer sur certaines caractéristiques telles que le processus de fabrication, la formulation, les excipients, la couleur, le goût et l'emballage. En d'autres termes, un médicament générique est thérapeutiquement équivalent à un médicament de marque et peut donc être substitué à son équivalent de marque.
Q2: Pourquoi les médicaments génériques coûtent-ils moins cher qu'un médicament innovant ?
Rép. : Les médicaments génériques sont plus économiques comparés aux médicaments innovants, car ils n'ont pas à répéter les études précliniques et cliniques coûteuses et longues, qui sont requises pour les médicaments innovants afin de démontrer leur sécurité et leur efficacité. Au lieu de cela, les médicaments génériques doivent seulement prouver l'équivalence pharmaceutique de leur produit.
Q3 : Les médicaments génériques sont-ils aussi efficaces que les médicaments de référence ?
Rép. : Oui, les médicaments génériques ont la même qualité, efficacité et sont aussi sûrs que les médicaments de marque. Le prix inférieur de ces médicaments n'indique pas qu'ils sont de qualité inférieure, car les médicaments génériques, tout comme les médicaments de marque, doivent passer par un processus d'approbation rigoureux pour commercialiser leur produit. Les sociétés pharmaceutiques sont tenues de soumettre une demande de médicament générique, démontrant que leur produit a le même bénéfice clinique que les médicaments de marque et qu'il peut être utilisé comme substitut de leur médicament de marque respectif.
Q4 : Pourquoi les médicaments génériques ont-ils une apparence différente de celle des médicaments de marque ?
Rép. : Les médicaments génériques doivent être bioéquivalents aux médicaments de marque et avoir le même API que les médicaments innovants. Cependant, il peut y avoir des différences minimes dans les produits médicamenteux génériques concernant la forme, l'étiquetage (différences mineures), l'emballage et les ingrédients inactifs tels que la couleur, les arômes et les conservateurs ; mais l'efficacité du médicament doit rester la même.
Q5 : Qu'implique l'examen et l'approbation des demandes de médicaments génériques aux US ?
Réponse : Tout laboratoire pharmaceutique souhaitant commercialiser son médicament générique aux US se conformer à l'ensemble des exigences réglementairesFDAen matière de dépôt de dossier pour les médicaments génériques et doit démontrer que :
- Le médicament générique est « pharmaceutiquement/thérapeutiquement équivalent » au médicament de marque.
- Le fabricant est capable de produire le médicament correctement et de manière constante.
- Le « principe actif » est le même que celui de la marque.
- La bonne quantité de l'ingrédient actif atteint l'endroit du corps où il produit son effet.
- Les ingrédients « inactifs » du médicament sont sans danger
- Le médicament ne se dégrade pas avec le temps.
- L'emballage dans lequel le médicament sera expédié et vendu est approprié
- L'étiquette est identique à celle du médicament de marque.
- Les brevets pertinents ou les exclusivités légales sont expirés
Q6 : Chaque médicament de marque a-t-il un équivalent générique ?
Rép. : Non. Tous les médicaments de marque n'ont pas de version générique. Les nouveaux médicaments sont fabriqués sous protection par brevet pendant une période allant jusqu'à vingt (20) ans. Cela signifie qu'aucun autre médicament ne peut être fabriqué et commercialisé pendant cette période, jusqu'à l'expiration du brevet. Cependant, certains médicaments peuvent ne jamais avoir de versions génériques pour leur produit, en raison de difficultés de fabrication ou si le produit médicamenteux générique est jugé non rentable.








