Rapport d'évaluation clinique (CER) pour les dispositifs médicaux - Présentation
Tout dispositif destiné à être commercialisé dans l'Union européenne (UE) doit porter le marquage CE. Conformément au règlement EU MDR , les exigences relatives au rapport d'évaluation clinique (CER), y compris celles concernant le processus et les données, varient en fonction de la classe du dispositif et sont indispensables pour obtenir la certification CE des dispositifs médicaux. Les dispositifs de classe I à faible risque peuvent faire l'objet d'une autocertification CE. En revanche, les dispositifs des autres classes (IIa, IIb, III) doivent obtenir la certification du marquage CE par l'intermédiaire d'un organisme notifié (ON) accrédité. Le fabricant doit soumettre le dossier technique CE à l'ON pour évaluation et délivrance de l'approbation du marquage CE ainsi que du certificat CE. Le rapport d'évaluation clinique (CER) des dispositifs médicaux doit être soumis avec le dossier technique CE afin de se conformer aux exigences du marquage CE. Le CER doit être mis à jour en permanence avec les nouvelles informations issues des contrôles de sécurité, des études de suivi et de la gestion des risques.
Le Rapport d'Évaluation Clinique (REC) pour les dispositifs médicaux est l'un des rapports qui doivent être soumis avec le dossier technique CE pour se conformer aux exigences du REC.
Qu'est-ce qu'un rapport d'évaluation clinique (CER) ?
La rédaction d'un rapport d'évaluation clinique comprend l'évaluation et l'analyse des données cliniques relatives à un dispositif médical afin de vérifier sa sécurité et ses performances cliniques. L'évaluation clinique des dispositifs médicaux repose sur l'analyse complète des données cliniques pré et post-commercialisation pertinentes pour l'utilisation prévue. Le rapport d'évaluation clinique inclut les données spécifiques au dispositif, ainsi que toutes les données relatives aux dispositifs considérés comme équivalents par le fabricant.
Un rapport d'évaluation clinique comprend la littérature scientifique et les données cliniques analysées, issues soit d'une étude clinique menée sur votre dispositif, soit des résultats d'autres études portant sur des dispositifs substantiellement équivalents. Les fabricants doivent avoir pleinement accès aux données techniques, biologiques et cliniques du dispositif équivalent et démontrer clairement en quoi leur dispositif correspond à celui-ci sur tous les aspects critiques. Le rapport d'évaluation clinique d'un dispositif médical démontre que celui-ci remplit sa fonction prévue sans exposer les utilisateurs et les patients à des risques supplémentaires.
EU MDR doit être mis à jour chaque année. La fréquence des mises à jour du CER dépend du niveau de risque et est spécifique à chaque dispositif. Si le dispositif présente des risques importants, la mise à jour doit avoir lieu au moins une fois par an ; en revanche, si le dispositif est commercialisé depuis longtemps et bien établi, le CER peut être mis à jour tous les 2 à 5 ans. Toute modification apportée à la conception du dispositif et toute nouvelle information issue des données de surveillance post-commercialisation (PMS) peuvent nécessiter une mise à jour du rapport CER.
L'évaluation clinique des dispositifs médicaux, telle que définie dans le Rapport d'Évaluation Clinique (REC), est basée sur les facteurs énumérés ci-dessous.
- Littérature scientifique actuellement disponible ; et/ou
- Investigations cliniques réalisées ; ou
- Lorsque la démonstration de conformité aux exigences essentielles basée sur des données cliniques n'est pas jugée appropriée.
Étapes de la rédaction du rapport d'évaluation clinique (REC)
En référence au nouveau Règlement (UE) relatif aux dispositifs médicaux (MDR) – 2017/745, il existe quatre (04) étapes différentes pour réaliser une évaluation clinique des Dispositifs Médicaux afin de préparer un Rapport d'Évaluation Clinique (CER) complet pour le MDR de l'UE.
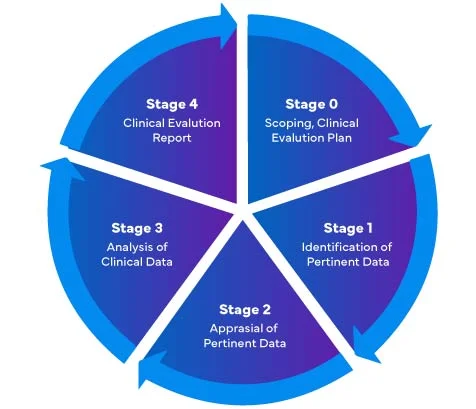
Les fabricants d'instruments médicaux entrant sur le marché de l'UE pour la première fois doivent s'assurer que leur rapport d'évaluation clinique est conforme à la réglementation EU MDR.
Freyr fournit des services End-to-End de certification CE aux fabricants de dispositifs, y compris la rédaction de rapports d'évaluation clinique conformément aux réglementations EU MDR 2017/745 nouvellement mises en œuvre. Grâce à une solide expertise régionale en matière de dispositifs médicaux dans l'UE, Freyr répond aux exigences spécifiques des agences et personnalise le rapport d'évaluation clinique en conséquence.
Rapport d'évaluation clinique (REC)
- Support End-to-End à la rédaction de rapports d'évaluation clinique, y compris la recherche bibliographique, conformément à la MEDDEV 2.7/1 révision 4 et aux lignes directrices du Règlement européen sur les dispositifs médicaux (MDR).
- Élaboration d'un plan d'évaluation clinique pour votre organisation.
- Identifier, rechercher, analyser et compiler la littérature scientifique pertinente et applicable.
- Élaborer un modèle de rapport d'évaluation clinique pour votre organisation.
- Analyse des écarts pour le rapport d'évaluation clinique existant.
- Outil DMS pour que votre équipe contribue collectivement à la rédaction des rapports d'évaluation clinique.
- Intégration des données PMS.
- Élaborer une procédure opératoire standard pour votre équipe afin de compiler les données de surveillance post-commercialisation (PMS) pour mettre à jour les rapports d'évaluation clinique.
- Gestion des mises à jour périodiques des rapports d'évaluation clinique existants, conformément aux directives du RDM de l'UE.
- Soutien en matière de données PMS pour les dispositifs existants sur le marché.
- Conformité au marquage CE et services de marquage CE.

- Conformité assurée aux réglementations récentes et applicables.
- Équipe d'experts cliniques qualifiés.
- Contributions interfonctionnelles d'experts en dispositifs médicaux pour se conformer aux exigences.
- Service complet couvrant la conformité, l'examen et la planification.

Foire aux questions (FAQ)
01. Qu'est-ce qu'un rapport d'évaluation clinique (CER) et pourquoi est-il important ?
Un rapport d'évaluation clinique (CER) est un document scientifique réglementaire qui évalue de manière systématique l'ensemble des données cliniques disponibles afin de démontrer qu'un dispositif médical est sûr, qu'il fonctionne conformément à sa destination et qu'il présente un rapport bénéfice/risque acceptable pour l'usage prévu, conformément EU MDR. Il joue un rôle central dans l'évaluation de la conformité et le maintien de la conformité.
02. Quand faut-il établir et mettre à jour un CER ?
La préparation du dossier de conformité (CER) débute dès les premières phases du développement du produit, dans le cadre d'un processus d'évaluation clinique planifié, et doit être régulièrement mise à jour tout au long du cycle de vie du dispositif dès que de nouvelles données cliniques, des données post-commercialisation ou des modifications du profil de risque apparaissent, afin de garantir que l'évaluation des bénéfices et des risques reste à jour.
03. Quels sont les éléments essentiels qu'un CER conforme doit comporter ?
Un CER solide doit refléter une évaluation structurée des données cliniques pertinentes, des comparaisons avec les technologies de pointe, une analyse des risques et des bénéfices, les données issues de la surveillance post-commercialisation, ainsi que des conclusions objectives quant à la conformité aux exigences EU MDR et de performance EU MDR .
04. En quoi l'« état de l'art » influe-t-il sur un rapport d'évaluation clinique ?
L'« état de l'art » constitue la référence en matière de pratiques cliniques et de technologies reconnues, à laquelle sont comparées les données cliniques ; il permet de replacer les avantages et les risques du dispositif dans leur contexte par rapport aux normes médicales actuelles, guidant ainsi une interprétation pertinente des données.
05. Un certificat d'évaluation (CER) est-il requis pour tous les dispositifs médicaux relevant du EU MDR?
Oui, les rapports d'évaluation clinique (CER) sont obligatoires pour tous les dispositifs médicaux commercialisés dans l'UE en vertu du règlement MDR, quelle que soit leur classe de risque, car ils fournissent les données cliniques indispensables pour démontrer la conformité aux exigences réglementaires en matière de sécurité et de performances.
06. Qu'est-ce qui distingue un CER de haute qualité d'un simple rapport de conformité ?
Un CER de haute qualité intègre une méthodologie complète de recherche documentaire, des allégations cliniques claires et adaptées à l'usage prévu, une évaluation rigoureuse des données, ainsi que des analyses approfondies sur les performances cliniques et les risques ; il va au-delà d'une simple vérification des cases à cocher pour refléter une compréhension approfondie des attentes réglementaires et du contexte clinique.
07. Pourquoi Freyr est-il considéré comme un partenaire de premier plan pour les services liés aux rapports d'évaluation clinique (CER) ?
Freyr est largement reconnue pour son approche axée sur la réglementation dans le domaine de l'élaboration d'études comparatives évaluatives (CER), qui allie EU MDR approfondie EU MDR , une évaluation rigoureuse des données cliniques et des stratégies axées sur le cycle de vie des produits. Ses équipes pluridisciplinaires coordonnent les connaissances cliniques, réglementaires et post-commercialisation afin de produire des CER scientifiquement rigoureuses, capables de résister à l'examen minutieux des organismes notifiés tout en garantissant la conformité à long terme.








