Aperçu
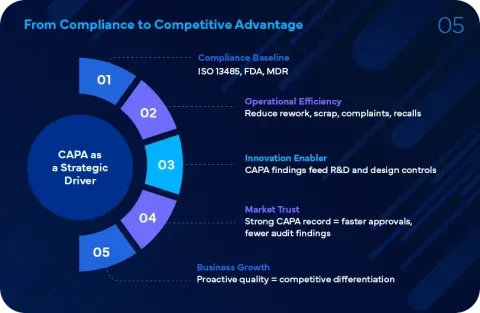
Nous proposons des services end-to-end de gestion des actions end-to-end et préventives (CAPA) spécialement adaptés au secteur des dispositifs médicaux. Nos solutions aident les organisations à identifier, analyser et résoudre les problèmes de qualité, tout en prévenant de manière proactive leur réapparition.
Forts d'une expertise approfondie en matière de conformité réglementaire et des meilleures pratiques du secteur, nous accompagnons votre équipe dans les domaines suivants :
- Analyse des causes profondes et évaluation des risques
- Planification, mise en œuvre et contrôle de l'efficacité du CAPA
- Documentation conforme aux normes FDA de l'ISO
- Intégration à votre système de gestion de la qualité (SGQ) pour un contrôle de la qualité sans faille
Nos services sont conçus pour aider les entreprises à traiter efficacement les problèmes de qualité, à prévenir leur réapparition et à maintenir leur conformité aux normes réglementaires internationales telles que FDA CFR Partie 820 et ISO 13485.
Qu'est-ce que le CAPA ?
Les mesures correctives et préventives (CAPA) constituent une approche utilisée pour examiner et résoudre les problèmes de qualité, tout en identifiant leurs causes. Elles ont été mises en place à la suite d'une exigence de la Food and Drug Administration (FDA) prévue par FDA 21 CFR 820.100. Les CAPA comprennent principalement deux fonctions :
Mesures correctives – L'objectif des mesures correctives est d'identifier la cause profonde des problèmes liés aux produits et à la qualité, et de prendre les mesures appropriées pour y remédier. Cela comprend :
- Examen et définition d'un problème
- Identification de la cause profonde d'un problème
- Élaboration d'un plan d'action pour la correction et la prévention
- Mise en œuvre du plan
- Évaluation de l'efficacité du plan

Mesures préventives – L'objectif des mesures préventives est d'empêcher que le problème ne se reproduise dans un avenir proche. Cela comprend :
- Identification des problèmes potentiels
- Identification de la cause première du problème
- Élaboration d'un plan de prévention des récurrences
- Mise en œuvre du plan
- Examen de l'efficacité des actions prises pour la prévention

CAPA et les procédures
Pour mettre en œuvre un plan CAPA efficace, les étapes suivantes doivent être respectées :
- Identifier les problèmes potentiels liés à la qualité, aux produits ou aux non-conformités
- Évaluer la gravité du problème et son impact sur l'entreprise
- Évaluer les procédures d'investigation disponibles
- Analyser le problème avec des données précises
- Élaborer un plan d'action qui traite tous les problèmes et propose des solutions pour les prévenir
- Mettre en œuvre le plan
- Effectuer des suivis réguliers pour garantir l'efficacité des solutions
En tirant parti de notre expertise approfondie en matière de CAPA et dans les domaines connexes de la gestion de la qualité, les entreprises du secteur des dispositifs médicaux peuvent :
- Améliorer leurs systèmes qualité
- Améliorer la sécurité et la fiabilité des produits
- Garantir une conformité réglementaire constante

Pour toute question relative au système de gestion de la qualité (SGQ) concernant nos services, reach à reach nos experts chez Freyr à l'adresse sales@freyrsolutions.com