
Aperçu de l'enregistrement des dispositifs médicaux à Taïwan
Taïwan connaît une demande croissante en dispositifs médicaux. L'Administration taïwanaise des aliments et des médicaments (TFDA), relevant du Ministère de la Santé et du Bien-être (MOHW), réglemente les dispositifs médicaux par le biais de la Loi sur les Affaires Pharmaceutiques (PAA). Les fabricants étrangers sans bureau physique à Taïwan doivent avoir une représentation d'agent à Taïwan comme condition préalable au processus d'enregistrement des dispositifs médicaux à Taïwan.
Autorité réglementaire : Administration taïwanaise des aliments et des médicaments
Réglementation : Loi sur les affaires pharmaceutiques (PAA) et Règlement sur l'enregistrement des dispositifs médicaux
Représentant autorisé : Représentation d'agent à Taïwan requise
Exigence SMQ : Documentation du système qualité (QSD) ISO 13485
Évaluation des données techniquesa : Division des Dispositifs Médicaux et des Cosmétiques
Validité de la licence : QSD - 3 ans ; Enregistrement des produits - 5 ans
Exigences d'étiquetage : Article 75, Loi sur les affaires pharmaceutiques
Format de soumission : Papier
Langue : Anglais et chinois
Classification des dispositifs médicaux à Taïwan
La TFDA classe les dispositifs médicaux en 3 catégories basées sur le risque : Classe I pour les dispositifs à faible risque, Classe II pour les dispositifs à risque modéré et Classe III pour les dispositifs à risque élevé. La nécessité d'un dispositif de référence constitue un défi pour l'entrée sur le marché des dispositifs innovants. Un délai de procédure accru pour les dispositifs de Classe II et III nécessitant une documentation du système qualité est une autre complexité. Tous les dispositifs médicaux importés doivent obtenir un certificat d'enregistrement de la TFDA.
| Classe de dispositif | Risque |
|---|---|
| Classe I | Faible risque |
| Classe II | Risque modéré |
| Classe III | Risque élevé |
Représentation d'agent à Taïwan
Les fabricants étrangers sans bureau physique à Taïwan doivent désigner un agent à Taïwan comme condition préalable pour commercialiser des dispositifs dans le pays. La désignation d'une organisation tierce comme agent à Taïwan, plutôt qu'un distributeur, offre la flexibilité d'explorer plusieurs distributeurs pour une meilleure pénétration du marché. L'agent à Taïwan doit être une entité juridique établie à Taïwan et détenir une licence de vente de produits pharmaceutiques.
Enregistrement des dispositifs médicaux à Taïwan
Avant qu'un dispositif médical puisse être vendu à Taïwan, l'enregistrement de la documentation du système qualité (QSD) pour l'installation de fabrication est requis en plus de l'enregistrement du dispositif médical. L'enregistrement QSD n'est dispensé que pour les dispositifs médicaux de classe I (non stériles). Une licence QSD (reçue après approbation de l'enregistrement QSD) à Taïwan est similaire aux Bonnes Pratiques de Fabrication (BPF) pour les dispositifs médicaux.
La TFDA a annoncé qu'à partir du 1er juin 2022, les titulaires de licence de dispositifs médicaux de classe III sont tenus de télécharger l'UDI et les informations produit correspondantes dans la base de données UDI (UDID). Les fabricants de dispositifs médicaux sont également tenus d'apposer l'UDI sur l'étiquette du produit. De plus, à partir du 1er juin 2023, les dispositifs médicaux de classe II devront respecter les réglementations pertinentes relatives à l'UDI.
Flux de processus
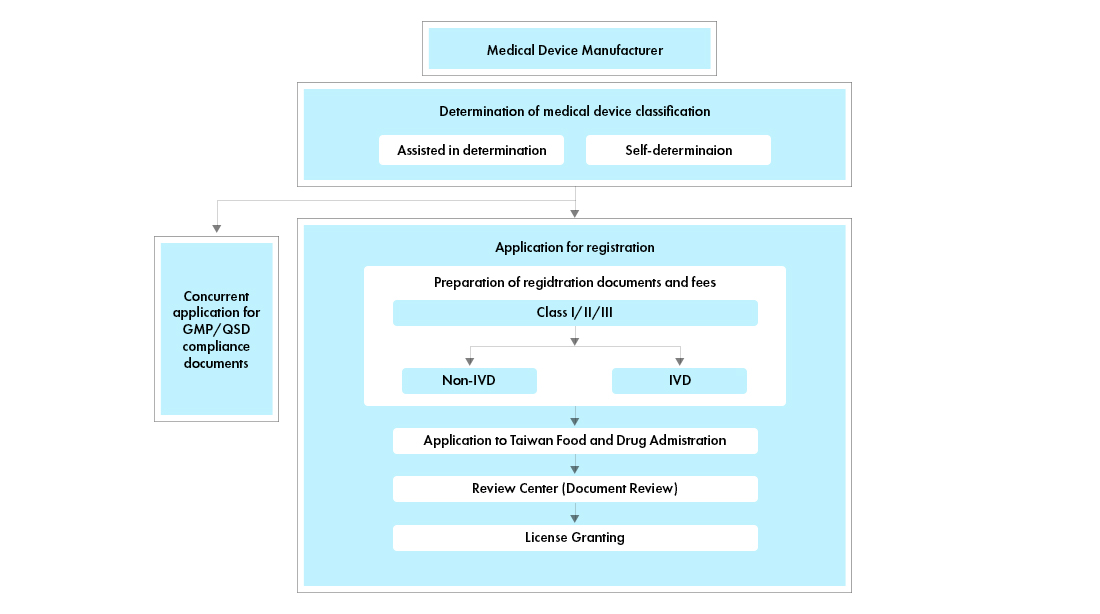
Gestion du cycle de vie des dispositifs médicaux post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-End du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des approbations et des enregistrements par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement des licences
- Assurer la liaison entre la TFDA et le fabricant
- Gestion des importations
Freyr est spécialisé dans la satisfaction des besoins réglementaires des dispositifs médicaux à Taïwan. Grâce à son vaste réseau, Freyr aide à la nomination d'un agent local fiable dont la présence est d'une importance capitale tout au long de la surveillance post-commercialisation. Nos experts assistent également dans la sélection d'un dispositif de référence approprié et des approbations existantes d'autres marchés pour soutenir l'entrée de nouveaux dispositifs sur le marché.
Résumé
| Classe de dispositif | Risque / Critères de classification | SGC | Enregistrement de produit |
|---|---|---|---|
| Classe I | Faible risque | Exempté (dispositifs non stériles de Classe I) | Oui |
| Classe II | Risque modéré | QSD | Oui |
| Classe III | Risque élevé | QSD | Oui |
L'expertise de Freyr
- Diligence raisonnable réglementaire
- Classification officielle
- Approbations QSD
- Enregistrement des dispositifs
- Représentant légal
- Support d'étiquetage
- Soutien à la traduction
- Identification et qualification des distributeurs
- Surveillance après commercialisation
- Gestion des changements post-approbation
- Renouvellement et transfert de licence
- Soumission et liaison


