Aperçu des services de mise en conformité avec le règlement IVDR de l'UE
Le règlement européen sur les dispositifs médicaux de diagnostic in vitro (IVDR de l'UE) constitue un nouveau cadre réglementaire pour la mise sur le marché européen des dispositifs médicaux de diagnostic in vitro. Le règlement IVDR de l'UE est destiné à remplacer la directive européenne actuelle relative aux dispositifs médicaux de diagnostic in vitro (UE 98/79/CE). En tant que règlement européen, il sera applicable dans tous les États membres de l'UE et les États membres de l'Association européenne de libre-échange (AELE), sans qu'il soit nécessaire de le transposer dans le droit des États concernés. En tant que partenaire réglementaire reconnu, Freyr propose aux industriels des services de conformité et de conseil en matière d'IVDR au sein de l'UE, afin d'assurer la conformité aux réglementations sur le diagnostic in vitro et le marquage CE.
Prenez rendez-vous avec nos experts en matière d'IVDR de l'UE
Le règlement IVDR - Calendrier de transition
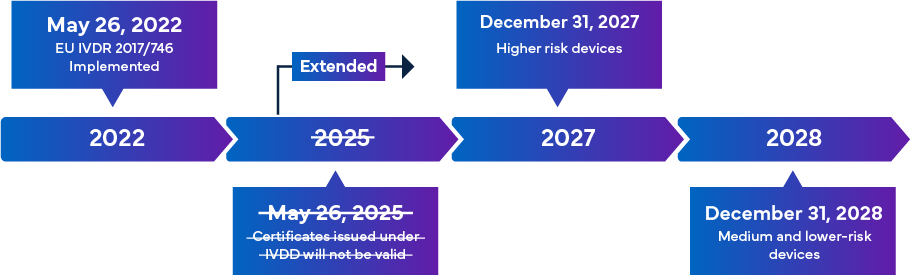
Prévu pour entrer en vigueur le 26 mai 2022, le nouveau règlement européen IVDR est considéré comme un changement majeur dans la surveillance réglementaire des dispositifs médicaux de diagnostic in vitro. Voici un aperçu de la transition vers l'IVDR :
Une fois pleinement mises en œuvre, les règles de conformité de l'IVDR garantissent que la quasi-totalité des dispositifs médicaux de diagnostic in vitro (IVD) mis sur le marché européen sont soumis à l'examen de l'organisme notifié (ON) de l'IVDR et à la certification du marquage CE dans le cadre de la procédure d'autorisation des IVD. Dans ce scénario, outre l'alignement sur la classification actualisée de l'IVDR, les fabricants doivent immédiatement revoir la documentation technique clé pour réussir l'enregistrement du dispositif de diagnostic in vitro (IVD) et l'apposition du marquage CE. Les exigences de l'IVDR varient en fonction de la classe de risque de l'IVD. En général, pour la certification des IVD, les fabricants doivent effectuer les opérations suivantes :
- Examen des dossiers techniques conformément au règlement IVDR (règlement UE 2017/746)
- Préparation du rapport d'évaluation des performances (PER) pour tous les dispositifs médicaux de diagnostic in vitro (IVD)
- Suivi des performances après la mise sur le marché (PMPF) conformément à l'annexe XIII, partie B, du règlement IVDR.
- Rapport de vigilance conformément à l'article 82 de l'IVDR
Freyr accompagne ses clients dans la réalisation d'une revue systématique de la littérature scientifique et les aide à planifier et à préparer un rapport d'évaluation pré-commercialisation (PER) afin de se conformer à la réglementation relative aux dispositifs médicaux de diagnostic in vitro. Freyr dispose d'experts spécialisés qui fournissent des services de conseil en matière d'IVDR et un soutien à la surveillance post-commercialisation (SPM), qui fait partie intégrante du système de gestion de la qualité du fabricant ainsi que du suivi des performances post-commercialisation (SPPM).
Obtenez des conseils d'experts sur la mise en conformité avec le règlement IVDR de l'UE
Services de mise en conformité avec le règlement IVDR de l'UE : L'EXPERTISE ET LES AVANTAGES DE
- Plan de transition pour la conformité au règlement IVDR
- Examen technique et analyse des lacunes des exigences de l'IVDR concernant les GSPR (exigences générales de sécurité et de performance)
- Contribuer à la constitution du dossier technique conformément aux exigences de l'IVDR
- Rapports sur la validité scientifique fondés sur la littérature et/ou les données internes
- Rapports sur les performances cliniques fondés sur la littérature et/ou les données internes
- Données cliniques ou rapports d'évaluation des performances
- Protocoles et rapports de suivi des performances post-commercialisation (SPPM)
- Protocoles et rapports de surveillance post-commercialisation (SPM)
- Rédiger ou réviser d'autres documents tels que les notices d'emballage/IFU (instructions d'utilisation), les guides de référence rapide (QRI), le manuel d'utilisation ou d'exploitation, etc.

- Garantir la conformité au règlement IVDR, l'enregistrement IVD et le marquage CE
- Maîtrise approfondie de la réglementation et expertise dans les domaines clés concernés par l'IVDR de l'UE
- Modèle de livraison axé sur la gestion de projet afin de garantir le respect du calendrier.
- Experts internes de l'ON (examen du rapport par les examinateurs interactifs de l'ON)
- Des équipes spécialisées possédant une expertise transversale dans des domaines d'impact et des catégories de dispositifs spécifiques
- Contributions interfonctionnelles d'experts en dispositifs médicaux pour se conformer aux exigences
- Ensemble des services liés à la conformité, à l'audit et à la planification
- Grande expertise dans le maintien de la cohérence des livrables (délais et qualité)

