Aperçu de l'enregistrement des dispositifs médicaux en Égypte
Depuis septembre 2018, l'enregistrement des dispositifs médicaux est devenu obligatoire en Égypte. L'industrie des dispositifs médicaux dans le pays a connu une croissance constante, offrant un marché attrayant pour les fabricants et les distributeurs. Avec une valorisation de 4,0 milliards de dollars en 2021, le marché égyptien des dispositifs médicaux devrait atteindre un taux de croissance annuel composé (TCAC) de plus de 3 % de 2022 à 2027. L'importation satisfait en grande partie la demande de dispositifs médicaux en Égypte, compte tenu de la production locale relativement faible. Il est remarquable que le marché égyptien des dispositifs médicaux soit le deuxième plus grand de la région du Moyen-Orient et de l'Afrique du Nord (MENA). Cet aperçu explore les aspects clés du processus d'enregistrement égyptien, offrant des informations sur le cadre réglementaire et les exigences pour mettre les dispositifs médicaux innovants au premier plan du secteur de la santé en Égypte.
Autorité de réglementation : Autorité égyptienne des médicaments (EDA)
Réglementation : Loi égyptienne sur les dispositifs médicaux, Loi n° 10 de 2003
Voie réglementaire : Enregistrement de produit (voie normale et accélérée) et classification officielle
Représentant local autorisé en Égypte : Titulaire d'enregistrement égyptien (ERH)
Exigence du SMQ : ISO 13485
Évaluation des données techniques : Le Centre de politique et de planification des médicaments (DPPC) et l'Administration centrale des affaires pharmaceutiques (CAPA).
Validité de la licence : Dix (10) ans
Format de soumission : Papier et électronique
Traduction : Documents traduits en arabe et en anglais
Classification des dispositifs
En Égypte, la classification des dispositifs médicaux s'aligne sur le système de classification européen, qui catégorise les dispositifs médicaux en fonction de leur utilisation prévue et des risques potentiels associés à leur utilisation. Les fabricants doivent identifier la classification correcte de leurs dispositifs pour assurer la conformité aux exigences réglementaires et obtenir les approbations nécessaires pour la commercialisation et la distribution en Égypte.
Classes de dispositifs médicaux
| Classe | Risque |
|---|---|
| Classe I | Faible |
| Classe IIa | Faible à moyen |
| Classe IIb | Moyen-élevé |
| Classe III | Élevé |
Représentant autorisé local en Égypte
Les entreprises de dispositifs médicaux basées en dehors de l'Égypte doivent désigner un agent local appelé « Titulaire d'enregistrement égyptien (ERH) » pour gérer la soumission des demandes d'enregistrement et des dossiers à l'EDA en leur nom. L'ERH assure la liaison entre le fabricant et l'autorité réglementaire, garantissant la préparation et la soumission précises de toute la documentation requise et vérifiant que le dispositif médical répond aux normes de sécurité, de qualité et d'efficacité de l'EDA. De plus, l'ERH est responsable de la conservation de la documentation d'enregistrement, du signalement des incidents ou des rappels, et de l'assurance du respect continu de toutes les normes et réglementations applicables tout au long du cycle de vie du dispositif. Le Titulaire d'enregistrement égyptien (ERH) est entièrement responsable de l'obtention de l'enregistrement d'un dispositif médical auprès de l'EDA, en particulier au sein de l'Administration centrale des dispositifs médicaux. Ce rôle implique de s'assurer de la conformité du dispositif aux exigences réglementaires de l'EDA pour sa commercialisation et sa distribution en Égypte.
Enregistrement des dispositifs médicaux
L'obtention de l'autorisation de mise sur le marché pour un dispositif médical en Égypte comprend plusieurs étapes, notamment la préparation des documents requis, la soumission de la demande à l'EDA, le respect des exigences de classification et de système qualité, la désignation d'un ERH si nécessaire, et le respect des obligations post-commercialisation. Le processus d'enregistrement est essentiel pour garantir que les dispositifs médicaux sont conformes aux normes de sécurité, de qualité et d'efficacité prescrites et établies par l'Autorité réglementaire égyptienne. La documentation requise peut varier en fonction de la voie d'enregistrement choisie, mais elle comprend généralement les éléments suivants :
- Certificat CE (le cas échéant).
- Certificat de Libre Vente (CFS).
- ISO 13485 .
- Déclaration de Conformité (DoC).
Flux de processus
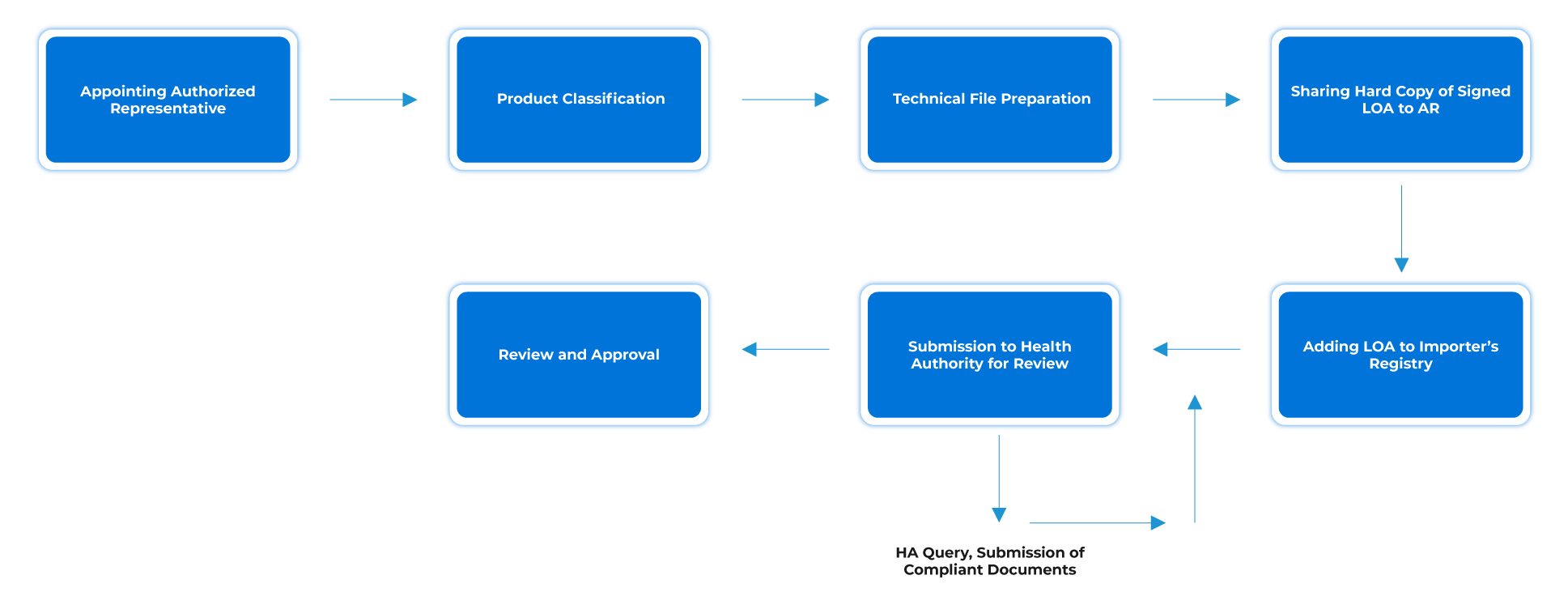
Gestion du cycle de vie des dispositifs après approbation
Freyr offre un soutien complet aux fabricants étrangers pour la gestion de l'ensemble du cycle de vie des dispositifs médicaux en Égypte, y compris les activités post-approbation :
- Gestion des modifications post-approbation, traitant des modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires et d'indications d'utilisation.
- Mise à jour de ISO 13485:2016.
- Certification CE.
- Agir en tant qu'intermédiaire entre l'Organisme Notifié (ON) et le fabricant.
- Un système de vigilance est en place pour surveiller la sécurité du dispositif médical après l'obtention de son autorisation de mise sur le marché.
- Fournir des mises à jour périodiques concernant la sécurité et l'efficacité du dispositif médical, ainsi que toute modification du statut réglementaire dans d'autres juridictions.
- Renouvellement de l'autorisation de mise sur le marché, selon le type de dispositif et la réglementation, après une certaine période.
La gestion efficace de la Surveillance après commercialisation (PMS) en Égypte implique de naviguer habilement dans les cadres réglementaires établis par l'EDA. Les nouveaux acteurs du marché qui peinent avec ces complexités et qui n'ont pas de partenaire réglementaire établi peuvent tirer parti des services réglementaires étendus offerts par Freyr. Ces services contribuent à un processus d'approbation fluide pour les dispositifs médicaux en Égypte, garantissant une conformité continue avec le paysage réglementaire en constante évolution et la dynamique du marché.
Expertise en enregistrement des dispositifs médicaux en Égypte
- Veille réglementaire.
- Diligence raisonnable réglementaire.
- Classification des dispositifs médicaux.
- Enregistrement des dispositifs.
- Titulaire de l'enregistrement égyptien.
- Soutien à la traduction.
- Rédaction médicale.
- Support d'étiquetage.
- Identification et qualification des distributeurs.
- Gestion des modifications post-approbation.
- Renouvellement et Transfert de Licence.
- Dédouanement.

