
Enregistrement des dispositifs médicaux aux EAU - Présentation
Les Émirats arabes unis (EAU), un pays membre éminent du CCG, disposent d'un système de santé avancé. Leur potentiel de marché est avéré et en constante augmentation, réglementé par le Département de contrôle des médicaments du Ministère de la Santé et de la Prévention (MOHAP). La gouvernance centralisée et les barrières linguistiques constituent des obstacles majeurs à l'enregistrement des dispositifs médicaux aux EAU, ainsi que les complexités linguistiques et le manque de canaux de communication efficaces avec les autorités sanitaires.
Autorité réglementaire : Département de contrôle des médicaments du Ministère de la Santé et de la Prévention (MOHAP)
Réglementation : Lignes directrices pour l'enregistrement des dispositifs médicaux aux Émirats arabes unis
Voie réglementaire : Enregistrement de produit
Représentant autorisé : Un représentant local autorisé est requis aux Émirats arabes unis
Exigence SMQ : ISO 13485:2016
Évaluation des données techniques : Comité d'enregistrement des dispositifs médicaux
Validité de la licence : 5 ans
Exigences d'étiquetage : Annexe 2 (2.5) des lignes directrices pour l'enregistrement des dispositifs médicaux aux Émirats arabes unis
Format de soumission : Papier
Langue : Anglais
Classification des dispositifs médicaux aux Émirats arabes unis
Les Émirats arabes unis ont des règles de classification distinctes pour les dispositifs médicaux et les dispositifs médicaux de diagnostic in vitro (DIV). Les règles de classification des dispositifs médicaux des Émirats arabes unis sont conformes aux règles de classification des directives européennes relatives aux dispositifs médicaux. Les classes de dispositifs selon les règles de classification des Émirats arabes unis sont les suivantes :
| Critères de risque | Classe de dispositif médical |
|---|---|
| Faible risque | I |
| Risque faible à modéré | IIa |
| Risque modéré à élevé | IIb |
| Risque élevé | III |
| Critères de risque | Classe IVD |
|---|---|
| Faible risque individuel et faible risque pour la santé publique | A |
Risque individuel modéré et/ou Faible risque pour la santé publique | B |
Risque individuel élevé et/ou Risque modéré pour la santé publique | C |
| Risque individuel élevé et risque élevé pour la santé publique | D |
Représentant local autorisé aux Émirats arabes unis
Les fabricants étrangers, sans bureau physique, doivent désigner un Représentant Local (RL) pour agir en leur nom. Le représentant local doit être agréé par le Ministère de la Santé en tant que magasin médical ou bureau scientifique (dans le cas d'un bureau scientifique, les activités d'importation et de distribution doivent être effectuées par un magasin médical agréé désigné). Les demandeurs peuvent désigner leur distributeur comme leur Représentant Local. Cependant, avoir un Représentant Local indépendant, sans intérêt commercial, offrirait la flexibilité nécessaire pour désigner plusieurs distributeurs aux Émirats arabes unis. Les détails du RL et du distributeur doivent être fournis lors de l'enregistrement du dispositif.
Processus de classification officielle avec le MoHAP des Émirats arabes unis
Le MoHAP des Émirats arabes unis a introduit un service officiel de classification, particulièrement utile lorsque vous n'êtes pas sûr si votre produit nécessite un enregistrement. Ce service classe les produits de tous types et formes en fonction de leur présentation, composition, utilisation et conception. Les exigences peuvent varier en fonction de la nature du produit, de sa classe de risque et de son statut réglementaire.
La lettre de classification indique si un produit doit être enregistré auprès du MOHAP. Si l'enregistrement est requis, le produit doit être enregistré selon la classe identifiée dans la lettre de classification. Cette lettre est valide pendant trois ans à compter de sa date d'émission.
Les résultats officiels de la classification peuvent être :
- Ne nécessite pas d'enregistrement MOHAP
- Approuvé par le MOHAP des Émirats arabes unis en tant que dispositif médical, réservé à un usage professionnel
- Approuvé par le MOHAP des Émirats arabes unis en tant que dispositif médical en vente libre
Enregistrement des dispositifs médicaux aux Émirats arabes unis
Certains dispositifs ne nécessitent pas d'enregistrement de produit, d'inscription préalable ou d'approbation pour l'importation. Les produits exemptés d'enregistrement ou d'inscription doivent demander et obtenir un permis d'importation pour être commercialisés aux Émirats arabes unis.
Pour les autres dispositifs, les importations ne seront pas autorisées à moins qu'une pré-approbation pour l'importation de l'envoi ne soit délivrée par le DRCD. Ces dispositifs doivent être soit répertoriés, soit enregistrés pour être importés aux Émirats arabes unis.
Enregistrement des dispositifs : Généralement, les produits utilisés dans les hôpitaux sous supervision professionnelle et les dispositifs de Classe I ne font pas l'objet d'une évaluation détaillée et doivent être enregistrés. Un certificat d'enregistrement sera délivré par l'agence. Après enregistrement, les dispositifs devront obtenir un permis d'importation pour être commercialisés aux Émirats arabes unis.
Enregistrement des dispositifs : L'activité d'enregistrement comprend l'enregistrement du site et du produit.
- Enregistrement du site :Le site de fabrication doit être enregistré si le dispositif fabriqué sur ce site est importé pour la première fois aux Émirats arabes unis. Pour les dispositifs ultérieurs fabriqués sur le même site, seul l'enregistrement du dispositif suffira, et l'enregistrement du site ne sera pas requis.
- Enregistrement des dispositifs : Ces dispositifs sont soumis à l'examen du comité technique qui, après approbation, délivrera un certificat de licence.
Flux de processus
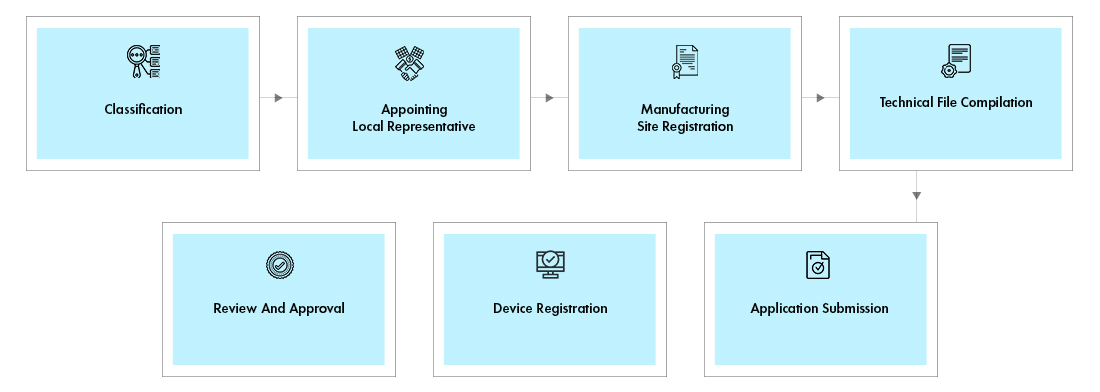
Gestion du cycle de vie des dispositifs post-approbation
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des approbations et des enregistrements par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement des licences
- Assurer la liaison entre le Ministère de la Santé et le fabricant
- Gestion des importations
Avec un centre de livraison exclusif à Dubaï, Freyr détient une position d'autorité sur le marché des dispositifs médicaux aux Émirats arabes unis et définit la classification des dispositifs en plus de décoder les réglementations d'orientation pour une meilleure conformité. Nous aidons les clients dans la compilation des documents conformément aux normes et assurons ainsi des approbations rapides. Freyr offre une gamme complète de services réglementaires relatifs à la commercialisation réussie des dispositifs.
Résumé
| Type de dispositif | Enregistrement des dispositifs | Enregistrement des dispositifs | Licence d'importation |
|---|---|---|---|
Dispositif exempté de l'approbation préalable à l'importation (Figurant à l'Annexe 3) | NA | NA | OUI |
| OUI | NA | OUI |
| Tous les autres dispositifs | NA | OUI | OUI |
L'expertise de Freyr
- Veille réglementaire
- Diligence raisonnable réglementaire
- Classification formelle des dispositifs médicaux
- Enregistrement des dispositifs
- Représentation autorisée aux Émirats arabes unis
- Soutien à la traduction
- Support d'étiquetage
- Identification et qualification des distributeurs
- Gestion des changements post-approbation
- Renouvellement et transfert de licence
- Dédouanement

Notre implantation aux Émirats arabes unis
1001 Prism Tower,
Happiness Street, Business Bay,
117938, Dubaï, Émirats Arabes Unis

