
Services réglementaires pour les dispositifs médicaux
à Singapour – Aperçu
Les dispositifs médicaux à Singapour sont réglementés en vertu de la loi sur les produits de santé (HPA) et de son règlement de 2010 sur les produits de santé (dispositifs médicaux).
Autorité réglementaire : Autorité des sciences de la santé (HSA)
Réglementation : Règlement de 2010 sur les produits de santé (dispositifs médicaux)
Voie réglementaire : Direction des dispositifs médicaux de la Health Sciences Authority (HSA)
Représentant autorisé : Déclarant de Singapour
Exigence SMQ : SS 620:2016, Norme singapourienne relative aux bonnes pratiques de distribution des dispositifs médicaux, et ISO 13485:2016
Évaluation des données techniques : Autorité des sciences de la santé (HSA)
Validité de la licence : Toutes les licences de revendeur sont valides pendant 12 mois à compter de la date d'approbation
Labelling : Orientations réglementaires, GN- 23 Révisé (1er mars 2020)
Format de soumission : En ligne
Langue : Anglais
Classification des dispositifs médicaux HSA
La HSA applique 16 ensembles de règles pour classer les dispositifs médicaux, du risque le plus faible au plus élevé, en classes A, B, C et D.
La classification des risques dépend de facteurs tels que la durée de contact, le degré d'invasivité, l'usage prévu et la méthode d'administration.
Classification des dispositifs médicaux, HSA
| Classe de risque | Niveau de risque | Exemples de dispositifs médicaux |
|---|---|---|
| Classe A | Faible risque | Visionneuse de films, main chirurgicale, gaine, masque à oxygène |
| Classe B | Risque faible à modéré | Brassard de tensiomètre, stérilisateur de tige |
| Classe C | Risque modéré à élevé | Moniteur patient, appareil de radiographie |
| Classe D | Risque élevé | Stents cardiaques, stimulateurs cardiaques |
Classification IVD
Les dispositifs médicaux de diagnostic in vitro sont classés ci-dessous du risque le plus faible au risque le plus élevé.
Classe de risque | Niveau de risque | Exemples de dispositifs médicaux de diagnostic in vitro |
|---|---|---|
| Classe A | Faible risque individuel et faible risque pour la santé publique | Récipient d'échantillons. |
| Classe B | Risque individuel modéré ou faible risque pour la santé publique, ou les deux | Vitamine B12, autotests de grossesse, anticorps antinucléaires, bandelettes urinaires |
| Classe C | Risque individuel élevé ou risque modéré pour la santé publique, ou les deux | Autosurveillance de la glycémie, typage HLA, dépistage du PSA, IgM de la rubéole |
| Classe D | Risque individuel élevé et risque élevé pour la santé publique | Dépistage du VIH chez les donneurs de sang, kit de diagnostic du VIH |
Représentant autorisé / Déclarant de dispositifs médicaux à Singapour
Un Déclarant est l'intermédiaire entre votre entreprise et la HSA, qui gère l'enregistrement des dispositifs à Singapour. Le représentant autorisé pour les dispositifs médicaux à Singapour traite la demande d'enregistrement auprès de la HSA et est titulaire de l'enregistrement de votre dispositif auprès de la HSA. Seules les entreprises ou entités basées à Singapour peuvent agir en tant que Déclarant ; elles doivent également être enregistrées auprès de la HSA.
Enregistrement des dispositifs médicaux HSA
Le processus d'enregistrement des dispositifs médicaux de la HSA est effectué via le système en ligne d'information et de communication sur les dispositifs médicaux (MEDICS) de la HSA. Chaque enregistrement de dispositif HSA se fait par une voie d'évaluation spécifique, en fonction des éléments suivants :
- Classification des risques du dispositif.
- Nombre d'approbations préalables accordées par les agences réglementaires de référence étrangères.
- Durée de l'historique de commercialisation en matière de sécurité du dispositif.
La voie d'évaluation du dispositif déterminera le délai d'exécution (TAT), les frais et les documents requis pour l'enregistrement.
Enregistrement de Classe A - Les dispositifs médicaux de Classe A sont exemptés de l'enregistrement des produits. Cependant, il est nécessaire de compléter la liste d'exemption de Classe A dans MEDICS lors de la demande de licence du distributeur.
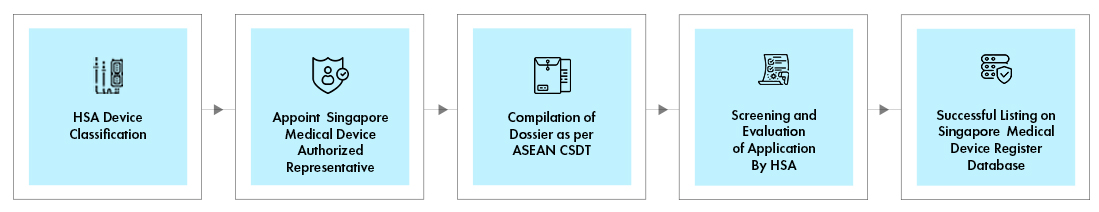
Flux de processus
Gestion du cycle de vie des dispositifs post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-end du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des modifications post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes et d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres.
- Maintien des approbations et de l'enregistrement des dispositifs médicaux par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement de licence.
Avec une équipe professionnelle pour fournir un soutien réglementaire, Freyr aide les fabricants à maintenir la qualité et la sécurité nécessaires à l'approbation. Les experts en veille de Freyr observent attentivement les mises à jour réglementaires et informent les clients des mesures à prendre pour la conformité des produits aux normes en vigueur.
Résumé
Le délai de traitement pour l'enregistrement des produits est indiqué dans le tableau suivant.
| Classe de risque | Immédiat | Accéléré | Abrégé | Évaluation complète | Complet (Procédure d'examen prioritaire) |
|---|---|---|---|---|---|
| Classe B | Enregistrement immédiat dès la soumission | 100 jours ouvrables | 160 jours ouvrables | 120 jours ouvrables | |
| Classe C | Enregistrement immédiat dès la soumission (uniquement pour les applications mobiles médicales autonomes de Classe C) | 120 jours ouvrables | 160 jours ouvrables | 220 jours ouvrables | 165 jours ouvrables |
| Classe D | 180 jours ouvrables | 220 jours ouvrables | 310 jours ouvrables | 235 jours ouvrables | |
| Classe D (dispositifs intégrant des Produits médicaux) | 220 jours ouvrables | 310 jours ouvrables |
Le délai de traitement pour un changement de déclarant est de 40 jours ouvrables.
NOTE-
- Les dispositifs médicaux de Classe A sont exemptés de l'enregistrement des produits.
- Le délai de traitement exclut le temps nécessaire pour répondre aux demandes de clarification ou d'informations supplémentaires de la part de la HSA pendant la phase d'évaluation.
L'expertise de Freyr
- Diligence raisonnable réglementaire pour l'enregistrement des dispositifs auprès de la HSA, Singapour
- Classification et regroupement des dispositifs médicaux HSA
- Soutien à l'évaluation par l'organisme d'évaluation de la conformité (CAB)
- Compilation de dossiers selon le Modèle de dossier de soumission commun de l'ASEAN (CSDT)
- Enregistrement des dispositifs HSA ;
- Représentation légale
- Support d'étiquetage
- Identification et Qualification des Distributeurs
- Surveillance après commercialisation
- Gestion des modifications post-approbation
- Renouvellement et Transfert de Licence
- Services de soumission et de liaison avec la HSA



