
Aperçu de l'enregistrement des dispositifs médicaux au Vietnam
Le marché des dispositifs médicaux au Vietnam est en pleine croissance et constitue actuellement l'un des secteurs les plus dynamiques du pays. Les dispositifs médicaux y sont réglementés par le Département des équipements médicaux et des travaux de santé (DMEHW), sous l'égide du Ministère de la Santé. Les fabricants étrangers doivent désigner un Représentant local autorisé au Vietnam pour les assister dans le processus d'enregistrement des dispositifs médicaux au Vietnam.
Autorité réglementaire : Département des équipements médicaux et des travaux de santé (DMEHW)
Réglementation : Décret n° 98/2021/ ND-CP
Représentant autorisé : Représentant local autorisé au Vietnam
Exigence SMQ : ISO 13485:2016
Évaluation des données techniques : Département des équipements médicaux et de la construction (DMEC) du MoH.
Labelling : Décret n° 111/2021
Format de soumission : En ligne- Délais : 15 à 60 jours
Langue : Anglais et vietnamien
Classification des dispositifs médicaux au Vietnam
Les dispositifs sont classés en 4 classes (A, B, C et D) qui sont également catégorisées en deux groupes : le groupe 1 (Classe A) et le groupe 2 (Classes B, C et D). La classification officielle est disponible auprès du Département vietnamien des équipements médicaux et des travaux de santé (DMEHW).
| Groupe | Classe | Risque |
|---|---|---|
Groupe 1 | Classe A | Faible niveau |
Groupe 2 | Classe B | Niveau de risque moyen plus faible |
Classe C | Niveau moyen supérieur des risques | |
Classe D | Niveau de risques élevé |
Représentant local autorisé au Vietnam
La désignation d'un agent vietnamien fiable et compétent pour les fabricants étrangers est cruciale, car il doit prendre en charge les services de garantie offerts par le fabricant dans le cadre de la vente du dispositif. La traduction en vietnamien est indispensable pour pénétrer la région, ce qui peut s'avérer difficile dans la pratique.
Freyr offre un soutien réglementaire couvrant toute la gamme d'activités, telles que l'obtention du numéro de reconnaissance de libre-vente impliqué dans l'approbation des dispositifs médicaux par les autorités. Nous fournissons également un soutien linguistique expert pour maintenir intacte la perspective réglementaire de la traduction. Nous répondons aux besoins des clients après l'approbation pour maintenir la conformité tout au long du cycle de vie du produit au Vietnam.
Enregistrement des dispositifs médicaux au Vietnam
Tous les produits de classe A et B nécessiteront une licence d'autorisation de mise sur le marché (AMM). Les dispositifs de classe A et B feront l'objet d'un examen administratif rapide par le ministère de la Santé de la province où est situé le titulaire de l'enregistrement.
Les dispositifs de classe C et D devront désormais demander une licence d'autorisation de mise sur le marché (MA). Les licences MA resteront valides indéfiniment.
Flux de processus
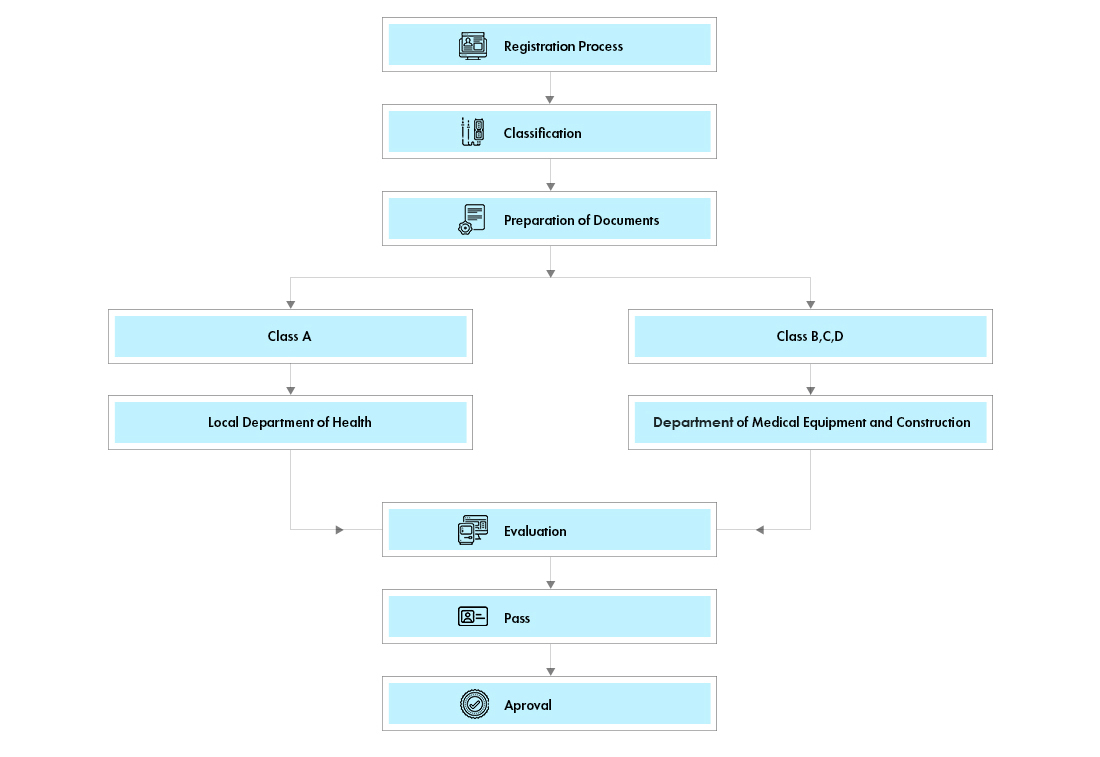
Gestion du cycle de vie des dispositifs post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-End du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des approbations et des enregistrements par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement des licences
- Assurer la liaison entre le DMEHW et le fabricant
- Gestion des importations
Résumé
Groupe | Classe | Risque | Voie réglementaire | Délais | Validité |
|---|---|---|---|---|---|
Groupe 1 | Classe A | Faible niveau | Déclaration de norme applicable | 15 - 60 jours | Illimité |
Groupe 2 | Classe B | Niveau de risque moyen plus faible | Certificat d'enregistrement de libre vente | 15 - 60 jours | 5 ans |
Classe C | Niveau moyen supérieur des risques | Certificat d'enregistrement de libre vente | 15 - 60 jours | 5 ans | |
Classe D | Niveau de risques élevé | Certificat d'enregistrement de libre vente | 15 - 60 jours | 5 ans |
L'expertise de Freyr
- Diligence raisonnable réglementaire
- Classification officielle
- Enregistrement des dispositifs
- Licence d'importation
- Support d'étiquetage
- Soutien à la traduction
- Identification et qualification des distributeurs
- Surveillance après commercialisation
- Gestion des changements post-approbation
- Renouvellement et transfert de licence
- Soumission et liaison
- Dédouanement


