Services de réglementation pharmaceutique au Chili – Aperçu
Le marché pharmaceutique chilien est réglementé par l'Instituto de Salud Pública de Chile (ISP), qui supervise l'autorisation, l'enregistrement et la surveillance des médicaments. Tous les produits pharmaceutiques doivent être enregistrés avant leur mise en vente, ce qui garantit leur conformité aux normes de qualité, de sécurité et d'efficacité fixées par les directives internationales.
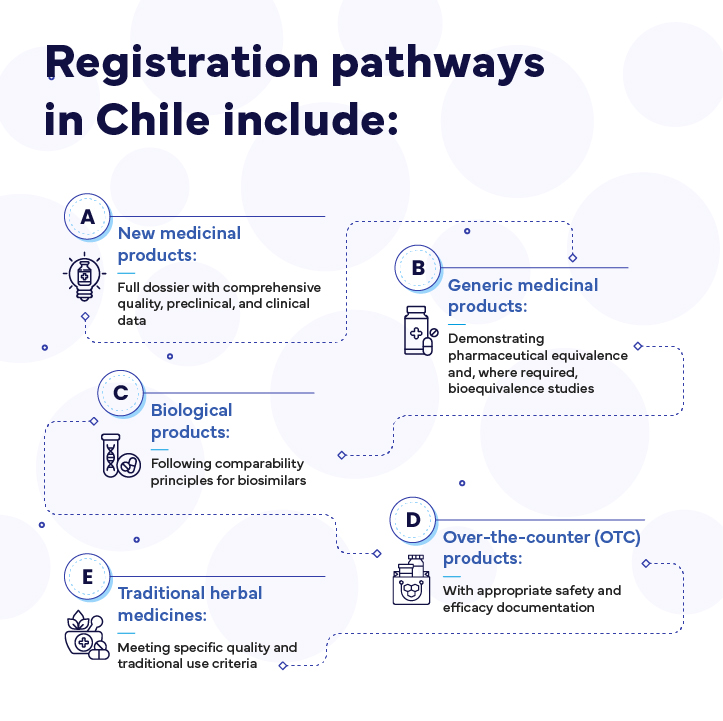
Les filières d'inscription au Chili comprennent :
Les principales exigences comprennent la documentation en espagnol, les certificats apostillés délivrés par l'autorité d'origine, un titulaire enregistré au Chili et des certificats de conformité aux BPF. Des études de bioéquivalence sont requises pour certains principes actifs désignés par l'ISP.
Le cadre réglementaire exige une expertise en matière de procédures de dépôt, de documentation et de conformité au niveau local. Les fabricants étrangers doivent faire face à des tâches administratives complexes tout en veillant au respect des normes chiliennes en matière d'étiquetage, de pharmacovigilance et de qualité.
Freyr offre un accompagnement réglementaire complet aux entreprises pharmaceutiques souhaitant obtenir une autorisation de mise sur le marché au Chili, depuis la planification stratégique jusqu'à la gestion du cycle de vie post-autorisation.
Services de réglementation pharmaceutique au Chili - Freyr Expertise
Stratégie d'enregistrement et préparation du dossier
- Création de dossiers au format CTD pour les soumissions aux autorités de réglementation
- Évaluation(s) de la voie d'accès (médicament innovant, générique, biosimilaire)
- Veille réglementaire (RI) et analyse des écarts
- Planification des données pour les modules qualité, précliniques et cliniques
Services de représentation locale
- Services destinés aux titulaires d'enregistrement domiciliés au Chili
- Relations avec les FAI et gestion de la correspondance officielle
- Services d'enregistrement et de mise en conformité des sites de production
Documentation et soutien administratif
- Gestion des certificats de produit pharmaceutique (CPP)
- Préparation des certificats GMP et gestion des apostilles
- Traduction en espagnol et certification par un notaire de documents réglementaires
- Rédaction et légalisation de procurations
Services de bioéquivalence et de qualité
- Planification et supervision des études de bioéquivalence
- Préparation des dossiers de justification des dérogations biologiques
- Accompagnement à la validation des méthodes d'analyse
- Élaboration d'un protocole de stabilité et analyse des données
Gestion des soumissions et du cycle de vie
- Soumission électronique via les plateformes des FAI
- Traitement des demandes et gestion des lacunes
- Modifications post-autorisation (CMC, étiquetage, administratives, etc.) et amendements
- Maintenance annuelle et assistance au renouvellement
Conformité et pharmacovigilance
- Artwork de l'étiquetage et Artwork chiliens
- Mise en place d'un système de pharmacovigilance
- Procédures de notification des événements indésirables (EI)
- Élaboration d'un plan de gestion des risques (PGR)
Notre implantation au Chili
Av. Manquehue n° 151,
, bureau 1205, Las Condes,
, Chili

