
L'idée de soumissions réglementaires électroniques pour les produits pharmaceutiques est antérieure à l'outil eCTD lui-même. À la fin des années 1980, des initiatives telles que CANDA (Computer-Aided New Drug Application) ont été explorées par la FDA US (Food and Drug Administration) et les agences européennes. Ces premiers efforts visaient à améliorer l'efficacité et l'accès aux données pour les évaluateurs.
Introduction de la norme eCTD (2003) :
La Conférence internationale sur l'harmonisation (ICH) est intervenue en 2003 avec une innovation majeure : la norme eCTD (document technique commun électronique). Ce format standardisé a été conçu pour établir un langage universel pour les soumissions électroniques à l'échelle mondiale.
L'émergence des outils eCTD :
Avec l'adoption de la norme eCTD, la demande d'outils eCTD spécialisés a fortement augmenté. Ces outils ont apporté plusieurs avantages clés :
- Création de contenu rationalisée : Les utilisateurs pourraient créer et organiser des documents sans effort, conformément à la structure eCTD.
- Validation robuste : les outils eCTD ont garanti que les soumissions respectaient les spécifications techniques, prévenant ainsi les retards causés par des erreurs de formatage.
- Gestion efficace du cycle de vie : La gestion des révisions, le suivi des versions et le maintien de la conformité réglementaire deviennent plus faciles.
Ces innovations ont révolutionné le processus de soumission réglementaire, le rendant plus efficace et fiable.
Comment le logiciel de Freyr Digital automatise la création d'eCTD
La solution logicielle avancée de Freyr Digital, Freyr SUBMIT PRO, relève ces défis en automatisant les aspects clés de la création d'eCTD, améliorant ainsi l'efficacité et réduisant les erreurs humaines.
Optimisation des ressources : En automatisant les tâches répétitives, notre logiciel libère de précieuses ressources humaines. Les professionnels peuvent se concentrer sur des activités plus stratégiques et à forte valeur ajoutée, telles que l'analyse de données, l'élaboration de stratégies réglementaires et l'engagement des parties prenantes. Ce changement améliore non seulement la productivité, mais réduit également les coûts opérationnels, offrant un retour sur investissement significatif.
Risque d'erreur humaine minimisé : L'automatisation minimise le risque d'erreur humaine en garantissant que les données sont transférées avec précision et que les documents sont correctement formatés. Les contrôles de validation intégrés au logiciel et les mécanismes de détection d'erreurs améliorent encore la qualité et la conformité des soumissions réglementaires. Cela réduit le besoin de retravailler et contribue à garantir des approbations rapides.
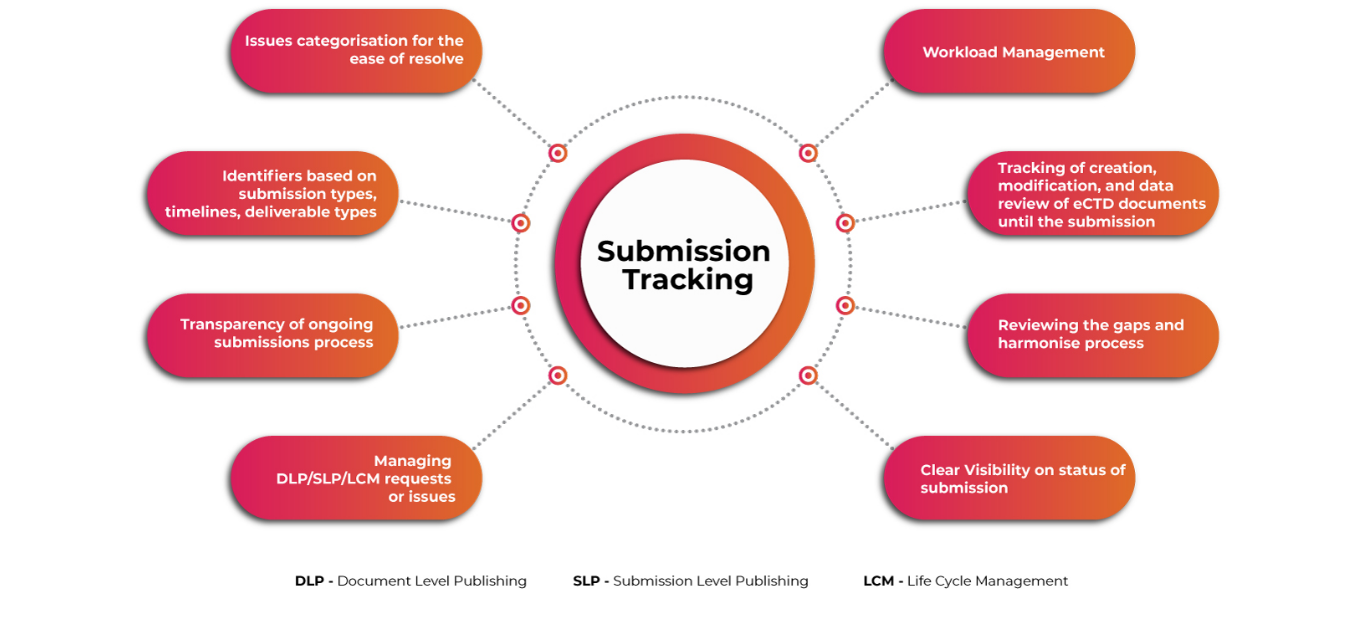
Outil de suivi des soumissions pour une vue d'ensemble complète des soumissions eCTD
Un système automatisé convivial pour la planification et le suivi des activités complexes de soumission eCTD mondiales, la gestion des flux de travail des activités, ainsi que le stockage et la gestion des demandes réglementaires et des informations de soumission est indispensable pour garantir que les demandeurs relèvent les défis associés bien avant l'échéance. Obtenir une visibilité détaillée sur les opérations de soumission et de publication rend l'ensemble du processus de soumission plus fluide et plus rapide.
Suivi des soumissions
La dernière mise à niveau de l'eCTD
Le passage à l'eCTD 4.0 annonce une efficacité accrue et une standardisation mondiale dans le processus d'approbation des médicaments pharmaceutiques. En se préparant à cette transition, votre entreprise peut gérer le changement en toute fluidité et tirer parti des nombreuses opportunités qu'offre cette nouvelle ère. Bien que le passage à l'eCTD 4.0 puisse poser des défis, ils sont surmontables avec le dévouement et la détermination de tous les pays concernés. Bien qu'un investissement et des efforts considérables soient nécessaires, les avantages substantiels de l'eCTD 4.0 rendent l'entreprise vraiment intéressante.
Refonte du processus de soumission : l'eCTD 4.0 promet de révolutionner la manière dont les entreprises pharmaceutiques soumettent les données de développement de médicaments aux autorités sanitaires. Il vise à simplifier le processus de soumission.
Calendrier de mise en œuvre : La FDA prévoit d'accepter les nouvelles demandes au format eCTD 4.0 à partir de 2024. Les phases futures aborderont les applications existantes en version 3.2.2 et la communication bidirectionnelle.
Compatibilité ascendante : l'eCTD 4.0 inclut la compatibilité ascendante, permettant la réutilisation du cycle de vie et des documents du contenu de la version 3.2.2. Cela simplifie la conversion des applications de la version 3.2.2 vers l'eCTD 4.0.
Critères de validation : Les spécifications pour les critères de validation eCTD 4.0 sont disponibles. Ces critères garantissent la qualité et l'exactitude des soumissions.
Conformité mondiale : D'ici 2026, les organismes de réglementation du monde entier pourraient exiger la conformité aux normes eCTD 4.0. Bien que cela soit actuellement volontaire, l'application commencera entre 2026 et 2029.
L'avenir de l'eCTD :
Il est essentiel d'intégrer l'IA pour dynamiser votre fonction réglementaire, car elle apporte une valeur ajoutée à votre entreprise. Freya Fusion est une plateforme de gestion des informations réglementaires (RIM) de pointe, basée sur l'IA et native du cloud, qui offre des performances, une sécurité et une évolutivité exceptionnelles, tout en assurant une conformité GxP stricte. Enrichie de fonctionnalités avancées d'IA/ML et d'automatisation, Freya Fusion excelle dans le domaine numérique, offrant des fonctionnalités supérieures et une expérience utilisateur remarquable. Les avancées en matière d'IA de Freyr Digital promettent des modules de production et de suivi des soumissions, incluant des fonctionnalités pour la compilation, la publication et la validation fluides des soumissions réglementaires, garantissant une conformité méticuleuse aux directives eCTD. Rester à la pointe de la conformité réglementaire grâce à un SaaS basé sur l'IA apportera certainement des avantages à votre entreprise. Que ce soit avec un système d'alerte précoce pour les changements réglementaires, une révision et une analyse simplifiées des documents réglementaires ou des analyses prédictives pour la gestion des risques, Freyr Digital vous offre une couverture complète. Contactez hello@freyrdigital.com pour découvrir nos innovations basées sur l'IA/ML qui optimisent les opérations réglementaires dans l'industrie médicale.
Gardez une longueur d'avance grâce aux mises à jour régulières et aux avancées technologiques. Collaborez avec nous pour optimiser vos opérations réglementaires, améliorer votre productivité et la qualité de vos soumissions. Demandez une démonstration dès aujourd'hui et découvrez l'alliance parfaite de l'expertise et des outils. Faites passer votre organisation du bon à l'excellent. Contactez-nous dès aujourd'hui.









