Aperçu de l'enregistrement des instruments médicaux par Santé Canada
Le Canada, doté de certaines des directives les plus strictes, possède l'un des meilleurs systèmes de réglementation au monde pour les dispositifs médicaux. Au Canada, tous les dispositifs médicaux sont réglementés par Santé Canada, Direction générale des produits de santé et des aliments, Direction des produits thérapeutiques, Bureau des matériels médicaux. Santé Canada examine les dispositifs médicaux pour évaluer leur sécurité, leur efficacité et leur qualité avant qu'ils ne soient autorisés à la vente au Canada, conformément au Règlement sur les instruments médicaux du Canada DORS/98-282, mis en œuvre en 1998. Freyr est un partenaire actif des entreprises de dispositifs médicaux pour les aider à se conformer aux directives d'enregistrement des dispositifs médicaux de Santé Canada.
Autorité réglementaire : Santé Canada
Réglementation : Règlement sur les dispositifs médicaux (DORS/98-282)
Représentant autorisé : Non requis
Exigence SMQ : Conformité à ISO 13485:2016 Comme Programme d'audit unique des dispositifs médicaux (MDSAP)
Évaluation des données techniques : Santé Canada
Validité de la licence : Illimité
Exigences d'étiquetage : Partie 21 du MDR (SOR/98-282)
Format de soumission : Papier
Langue : Anglais et français
Classification des instruments médicaux par Santé Canada
Le système de classification des instruments médicaux de Santé Canada est largement inspiré de la directive 93/42/CEE du Conseil de l'Union européenne. De nombreuses règles et interprétations des termes sont similaires à celles proposées par l'Union européenne. Il ne faut cependant pas en déduire qu'un instrument médical classé dans une catégorie selon le système de classification de l'Union européenne sera classé dans la même catégorie selon le système de classification des instruments médicaux du Canada. Le demandeur doit suivre les règles établies dans le Règlement pour déterminer la classification appropriée de son instrument au Canada.
Les indicateurs de risque suivants posés par un dispositif donné ont été utilisés pour créer les règles de classification canadiennes : degré d'invasivité, durée de contact, système corporel affecté et effets locaux par rapport aux effets systémiques.
| Classe de dispositif | Risque |
|---|---|
| I | Faible |
| II | Faible à modéré |
| III | Élevé-Modéré |
| IV | Élevé |
Représentant Autorisé au Canada
Il n'est pas obligatoire pour le fabricant de désigner un représentant autorisé au Canada. Le distributeur, cependant, doit se conformer aux exigences de Santé Canada en matière de Bonnes Pratiques de Distribution (GDP).
Enregistrement des dispositifs médicaux - Canada
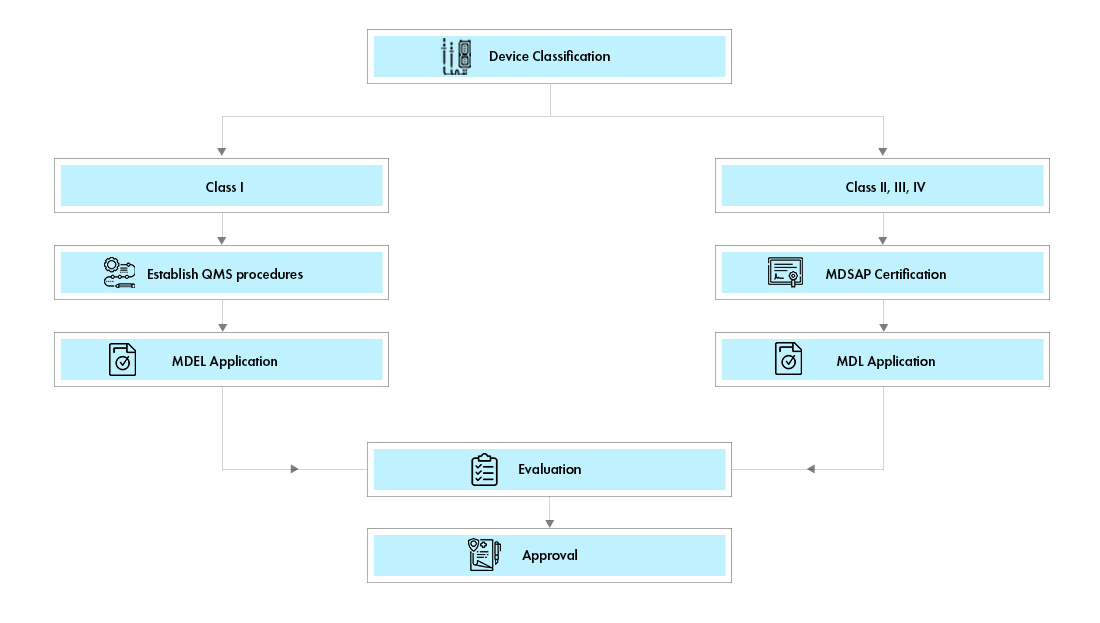
Il existe deux voies pour l'enregistrement des dispositifs médicaux au Canada :
Licence d'établissement de matériel médical (MDEL): Les dispositifs de Classe I peuvent demander une Licence d'établissement de matériel médical Canada (MDEL) en préparant les procédures obligatoires et en payant les frais de Santé Canada.
Licence de dispositif médical (MDL) : Les dispositifs de Classes II, III et IV doivent déposer une demande de licence canadienne de dispositif médical (MDL). Les exigences documentaires varient pour chaque classe de dispositif.
Flux de processus
Gestion du cycle de vie des dispositifs post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-end du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des approbations et des enregistrements par le paiement ponctuel des frais administratifs et d'enregistrement.
- Renouvellement des licences
- Assurer la liaison entre Santé Canada et le fabricant.
Résumé
| Risque | Classe de dispositif | Audit du SGC | Voie réglementaire | Exigences documentaires | Échéanciers de Santé Canada |
|---|---|---|---|---|---|
| Faible | I | NA | MDEL |
| NA |
| Faible à modéré | II | Certificat MDSAP | MDL |
| 15 Jours |
| Élevé-Modéré | III | Certificat MDSAP | MDL |
| 60 Jours |
| Élevé | IV | Certificat MDSAP | MDL |
| 75 Jours |
Les services d'enregistrement de dispositifs médicaux de Freyr
L'expertise de Freyr
- Services de classification et de regroupement des instruments médicaux par Santé Canada
- Enregistrement des dispositifs médicaux, Canada
- Réunions de pré-soumission avec Health Canada
- MDSAP, Canada.
- Identification/Qualification du distributeur pour la conformité aux exigences de Santé Canada
- Licence d'établissement de dispositifs médicaux Canada (MDEL)
- Homologation des dispositifs médicaux au Canada (MDL)
- Gestion des changements post-approbation
- Services d'étiquetage conformément aux exigences d'étiquetage de Santé Canada pour les dispositifs médicaux