Services d'audit et de validation de la conformité pharmaceutique
Bénéficiez d'une décennie d'expertise grâce à nos services, incluant des évaluations de conformité, des audits méticuleux et des processus de validation robustes.
Parcourir les sujets
- Qu'est-ce que la conformité, l'audit et la validation pharmaceutiques ?
- Quelle est l'importance de la conformité, de l'audit et de la validation dans l'industrie pharmaceutique ?
- Défis majeurs dans le domaine de la conformité, de l'audit et de la validation
- Que sont les audits GxP ?
- Comprendre les audits à distance
- Qu'est-ce que la Validation des Systèmes Informatiques (CSV), et pourquoi est-elle cruciale dans l'industrie pharmaceutique ?
- En quoi le CSV diffère-t-il de l'assurance des systèmes informatisés (CSA) ?
- Quels sont les composants d'un programme CSA ?
- Comment le CSA contribue-t-il à l'intégrité des données dans l'industrie pharmaceutique ?
- Quel rôle la conformité réglementaire joue-t-elle dans le CSA ?
- Comment un partenaire stratégique en conformité réglementaire peut-il aider ?
- Pourquoi choisir Freyr ?
- Nos Services
Qu'est-ce que la conformité, l'audit et la validation pharmaceutiques ?
Dernière mise à jour le : septembre 2024
Dans le domaine pharmaceutique, les processus de conformité, d'audit et de validation sont essentiels, garantissant le respect des normes réglementaires, l'intégrité des données et la production de produits sûrs et efficaces. La conformité implique l'alignement des opérations sur les réglementations de l'industrie et les politiques internes. Les audits, examens systématiques, vérifient la conformité, identifient les domaines d'amélioration et atténuent les risques. La validation garantit que les systèmes, processus et équipements répondent constamment aux exigences prédéfinies.
Les entreprises font appel à des experts pour naviguer sans encombre. Les leaders du secteur gèrent ces processus avec brio, garantissant le respect des normes internationales sans compromettre l'efficacité ni la sécurité des produits. À mesure que le secteur pharmaceutique évolue, les approches stratégiques en matière de conformité, d'audit et de validation deviennent essentielles à un succès durable. En respectant ces processus, les entreprises satisfont aux exigences réglementaires et favorisent une culture d'excellence et d'innovation dans un secteur dynamique et exigeant.
Collaborez avec un partenaire de confiance pour des conseils stratégiques et des solutions sur mesure qui permettent à vos opérations pharmaceutiques de prospérer dans un paysage réglementaire dynamique.

Quelle est l'importance de la conformité, de l'audit et de la validation dans l'industrie pharmaceutique ?
La conformité, l'audit et la validation sont des éléments essentiels dans l'industrie pharmaceutique, garantissant que les produits sont sûrs, efficaces et fabriqués conformément aux normes réglementaires.
- Garantit la sécurité et l'efficacité des produits : La conformité aux réglementations garantit que les produits pharmaceutiques répondent à des normes strictes de sécurité et d'efficacité avant d'être mis sur le marché. Cela implique des processus rigoureux de test et de validation pour confirmer que les produits fonctionnent comme prévu et ne présentent pas de risques pour les patients.
- Maintien de la conformité réglementaire : Des audits et validations réguliers aident les entreprises à respecter les réglementations complexes et évolutives établies par les autorités sanitaires. Cela inclut la conformité à GMP, GCP et à d'autres normes de l'industrie, réduisant le risque de sanctions réglementaires et de rappels de produits.
- Améliore l'assurance qualité : Les processus de validation, y compris les validations d'équipements et de systèmes, garantissent que les processus de fabrication et de test produisent constamment des produits de haute qualité. Les audits vérifient que ces processus sont correctement suivis, ce qui conduit à une amélioration de la qualité et de la fiabilité des produits.
- Favorise l'accès au marché et renforce la réputation : des pratiques efficaces en matière de conformité et de validation favorisent l'accès au marché en démontrant le respect des exigences réglementaires. Cela renforce la réputation et la crédibilité de l'entreprise, et permet d'instaurer un climat de confiance avec les professionnels de santé, les patients et les autorités réglementaires.
- Facilite l'amélioration continue : Les audits fournissent des informations sur l'efficacité des processus et les domaines à améliorer, ce qui conduit à un meilleur contrôle qualité et à de meilleures pratiques opérationnelles. Cette évaluation et cet ajustement continus aident à maintenir des normes élevées et à s'adapter aux changements de réglementations et aux meilleures pratiques de l'industrie.
Défis majeurs dans le domaine de la conformité, de l'audit et de la validation
Le domaine de la conformité, de l'audit et de la validation est confronté à plusieurs défis majeurs qui peuvent affecter la capacité des entreprises pharmaceutiques à respecter les exigences réglementaires et à maintenir des normes élevées de qualité et de sécurité :
| Défi | Description |
|---|---|
| Conformité réglementaire | Les laboratoires pharmaceutiques doivent se conformer aux réglementations strictes d'organismes tels que la FDA EMA, qui exigent une documentation rigoureuse et des mesures de contrôle qualité rigoureuses. Tout manquement à ces obligations peut entraîner des sanctions sévères, notamment des amendes et des rappels de produits. |
| Contrôle d'accès et sécurité | Il est essentiel de s'assurer que seul le personnel autorisé peut accéder aux zones et informations sensibles. Cela implique la mise en œuvre de systèmes de contrôle d'accès avancés et le maintien de la cybersécurité contre les menaces, ce qui peut être complexe et coûteux. |
| Validation des Systèmes Informatisés (CSV) | La validation des systèmes informatiques utilisés dans les environnements GxP est essentielle, mais souvent lourde et mal définie. Le processus exige beaucoup de temps et de ressources, surtout lorsqu'une approche standard est appliquée sans discernement. |
| Formation et sensibilisation des employés | Les programmes de formation continue sont nécessaires pour s'assurer que les employés comprennent les protocoles de conformité et leur importance. Une formation insuffisante peut entraîner des non-conformités et des erreurs dans les processus. |
| Documentation et tenue des registres | Maintenir une documentation précise et complète est essentiel pour la conformité. Une documentation insuffisante est un problème courant qui peut entraîner des observations réglementaires et des échecs lors des audits. |
| Intégrité des données | Il est crucial de garantir l'intégrité et l'exactitude des données, en particulier lors de la gestion de grands volumes d'informations. Les défis incluent le traitement manuel des données et la nécessité de systèmes de gestion de données robustes. |
| Gestion des fournisseurs | Le recours à des fournisseurs tiers pour les logiciels et les services nécessite des vérifications approfondies de validation et de conformité. La gestion de ces relations et la garantie qu'elles respectent les normes réglementaires peuvent être difficiles. |
| Complexité technologique | La complexité croissante des technologies, y compris l'IA et les systèmes Cloud-based, présente de nouveaux défis de validation et nécessite une adaptation continue aux évolutions du paysage réglementaire. |
| Contrôle qualité insuffisant | De nombreuses entreprises pharmaceutiques ont du mal à maintenir des normes de qualité élevées à travers leurs processus, ce qui peut entraîner des contaminations, des contaminations croisées et d'autres problèmes de qualité. |
| Amélioration continue et suivi | Les audits et inspections réguliers sont essentiels pour identifier les faiblesses des systèmes de conformité. Cependant, de nombreuses organisations ne parviennent pas à mettre en œuvre des mesures proactives pour l'amélioration continue. |
- Réglementations en évolution : Suivre l'évolution rapide des réglementations et des directives dans différentes régions peut être difficile. Les entreprises pharmaceutiques doivent continuellement mettre à jour leurs pratiques de conformité pour se conformer aux normes réglementaires nouvelles ou révisées, ce qui peut nécessiter des ressources et des ajustements importants.
- Complexité des normes mondiales : Naviguer dans les exigences réglementaires diverses et complexes des différents pays et régions ajoute au défi. Chaque juridiction peut avoir son propre ensemble de règles et de normes, ce qui rend difficile d'atteindre une conformité cohérente sur les marchés mondiaux.
- Intégrité et sécurité des données : Assurer l'intégrité et la sécurité des données tout au long des processus de conformité, d'audit et de validation est essentiel. Les entreprises doivent mettre en œuvre des systèmes et des contrôles robustes pour se protéger contre les violations de données, les falsifications ou les inexactitudes, qui peuvent avoir de graves conséquences pour l'approbation des produits et la sécurité des patients.
- Contraintes de ressources : Des ressources limitées, notamment en temps, en personnel et en budget, peuvent nuire à l'efficacité des activités de conformité et d'audit. Les entreprises ont souvent du mal à concilier les exigences de maintien de la conformité avec la nécessité d'allouer des ressources à d'autres fonctions commerciales critiques.
- Gestion de la documentation et de la tenue des registres : Une documentation et une tenue des registres appropriées sont essentielles pour démontrer la conformité et mener des audits efficaces. Cependant, gérer de vastes quantités de documentation, en assurer l'exactitude et maintenir son accessibilité peut être un défi, en particulier dans un environnement fortement réglementé.
- Intégration des nouvelles technologies : L'intégration de technologies innovantes dans les processus de conformité et de validation existants peut être complexe. Bien que des technologies comme l'automatisation et l'IA (Intelligence Artificielle) offrent des avantages significatifs, leur intégration doit être gérée avec soin pour s'assurer qu'elles sont conformes aux exigences réglementaires et n'introduisent pas de nouveaux risques.
- Formation et compétences : Il est crucial de s'assurer que le personnel est adéquatement formé et compétent dans les processus de conformité, d'audit et de validation. Des programmes de formation continue sont nécessaires pour tenir le personnel informé des changements réglementaires et des meilleures pratiques, ce qui peut être gourmand en ressources.
- Répondre aux constatations d'audit : Traiter et corriger efficacement les problèmes identifiés lors des audits peut être un défi. Les entreprises doivent mettre en œuvre rapidement des actions correctives et préventives tout en veillant à ce que ces actions ne perturbent pas les opérations en cours ni n'affectent la qualité des produits.
- Concilier conformité et innovation : Il peut être difficile de trouver un équilibre entre le respect de réglementations strictes et la poursuite de l'innovation. Les entreprises doivent naviguer dans le paysage réglementaire tout en continuant à développer et à introduire de nouveaux produits et technologies.
- Assurer la cohérence des opérations : Maintenir la cohérence des pratiques de conformité et des processus de validation entre les différents départements, installations et étapes du cycle de vie du produit est essentiel mais difficile. La variabilité des pratiques peut entraîner des non-conformités et des problèmes de qualité.
Que sont les audits GxP ?
Qu'est-ce qu'un audit de conformité indépendant GxP et qui le réalise ?
Un audit GxP est un processus mis en place pour garantir que les entreprises respectent les normes établies en matière de qualité, de sécurité et de conformité réglementaire. Il peut porter sur divers aspects des produits et processus pharmaceutiques, tels que les bonnes pratiques de laboratoire (GLP), les bonnes pratiques cliniques (GCP), les bonnes pratiques de fabrication (BPF) et les bonnes pratiques de pharmacovigilance (BPPV).
L'audit évalue le niveau de conformité aux lois, réglementations, directives et procédures opérationnelles standard (SOP) applicables, et identifie les lacunes, les risques et les possibilités d'amélioration. Il formule également des recommandations et propose des mesures correctives afin de remédier aux constatations et de renforcer les systèmes qualité.
Les avantages d'un audit GxP incluent :
- Fourniture d'une évaluation impartiale et objective des systèmes qualité et du niveau de conformité.
- Renforcer la confiance des organismes de réglementation, des clients, des fournisseurs et des autres parties prenantes.
- Réduire la probabilité et la gravité des inspections, observations et sanctions réglementaires.
- Amélioration de la qualité, de la sécurité et de l'efficacité des produits et des processus.
- Accroître l'efficacité et l'efficience des opérations et réduire les coûts et les erreurs.
- Soutenir l'amélioration continue et l'innovation des produits et des processus.
Un audit GxP est réalisé par un auditeur qualifié et expérimenté ou une équipe d'auditeurs possédant les connaissances, les compétences et les qualifications pertinentes dans l'industrie pharmaceutique et le domaine GxP spécifique. L'auditeur ou l'équipe d'audit doit être indépendant de l'entreprise auditée et suivre les normes professionnelles et les principes éthiques de l'audit. Ils doivent également utiliser des outils et des méthodes appropriés pour mener l'audit, tels que des listes de contrôle, des entretiens, des observations, des examens de documents, des échantillonnages, des tests, etc. Freyr offre un support End-to-End pour les audits GxP. En tant que leader de l'industrie, nos experts rendront votre parcours de conformité fluide.
Cadre réglementaire pour les audits GxP
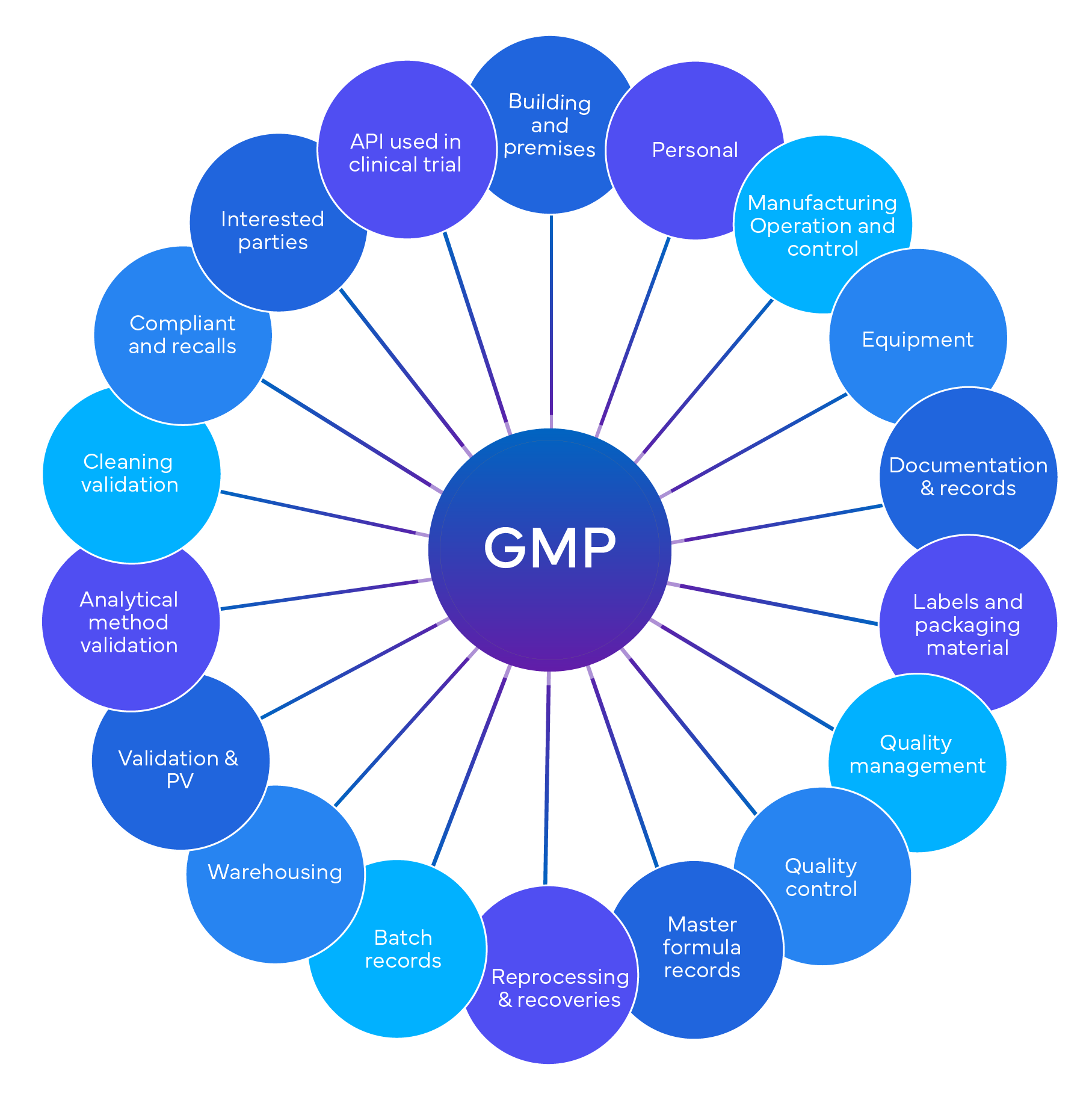
La conformité GxP est un ensemble de réglementations qui régissent diverses industries réglementées, y compris les produits pharmaceutiques, les dispositifs médicaux, l'alimentation, les boissons et la biotechnologie. L'objectif principal de la conformité GxP est de maintenir la qualité des produits et d'assurer la sécurité publique. Voici quelques points clés :
- Aperçu de la conformité GxP:
- Le GxP englobe plusieurs normes, y compris les Bonnes Pratiques de Laboratoire (BPL), les Bonnes Pratiques Cliniques (BPC), les Bonnes Pratiques de Fabrication (BPF) et les Bonnes Pratiques de Pharmacovigilance (BPV).
- Ces normes garantissent que les produits sont rigoureusement testés, fabriqués et manipulés tout au long de leur cycle de vie.
- Conférence internationale sur l'harmonisation (ICH):
- L'ICH fournit des lignes directrices pour la conformité GxP.
- Le Guide de Bonnes Pratiques de Fabrication ICH Q7A aborde spécifiquement les pratiques de fabrication des principes actifs pharmaceutiques (APIs).
- FDA:
- L'Agence américaine des produits alimentaires et médicamenteux (FDA)mène des inspections afin d'évaluer le respect des GxP .
- Ces inspections visent à évaluer le respect des FDA et des directives spécifiques FDA .
- Inspections de Santé Canada:
- Santé Canada, l'autorité réglementaire au Canada, effectue également des inspections pour assurer la conformité aux GxP.
- Ces inspections portent sur divers aspects, notamment la fabrication, le contrôle qualité et la distribution.
- Critères d'évaluation pour les audits GxP :
La conformité lors des audits indépendants GxP est généralement évaluée selon une série de critères, qui peuvent inclure :
- Exigences réglementaires: respect des réglementations, directives et lois spécifiques applicables au GxP (par exemple, FDA , ICH ou les normes ISO).
- Systèmes qualité: Évaluation des systèmes de gestion de la qualité, des pratiques de documentation et de la tenue des dossiers.
- Validation des processus : Vérification que les processus sont validés et répondent à des critères prédéfinis.
- Formation et compétences : Évaluation de la formation et des qualifications du personnel.
- Gestion des risques : Identification et atténuation des risques liés à la qualité et à la sécurité des produits.
Découvrez comment un expert réglementaire éprouvé peut vous aider à créer le cadre d'audit GxP idéal adapté à vos besoins et à rester conforme aux réglementations mondiales.
Avantages de la réalisation d'audits de conformité GxP
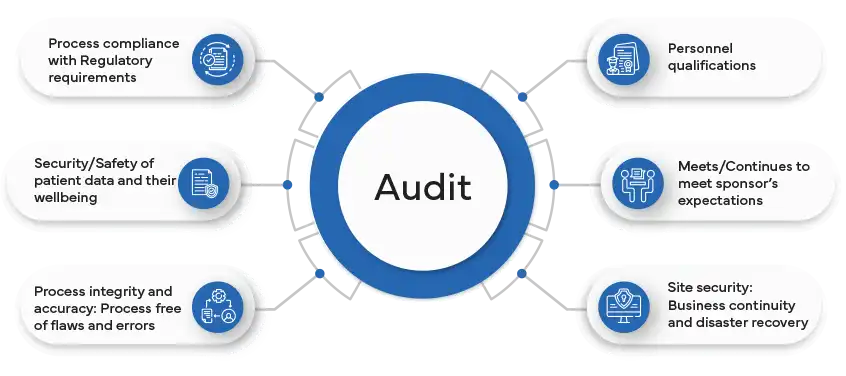
Les audits GxP présentent de nombreux avantages pour toute organisation. Premièrement, ils fournissent une évaluation impartiale et indépendante des risques et de la conformité au sein de l'organisation, permettant aux entreprises d'identifier les domaines de non-conformité ou les risques potentiels qui pourraient être négligés lors des audits internes. Ces audits sont essentiels pour garantir que les entreprises respectent certaines normes de qualité, de sécurité et de conformité réglementaire.
| Aspect | Description |
|---|---|
| Revue complète | Évaluation approfondie par un tiers qualifié pour identifier les zones de non-conformité. |
| Normes réglementaires | Respect des normes GxP (bonnes pratiques) telles que les BPF, BPC et BPL. |
| Périmètre sur mesure | Portée d'audit personnalisée basée sur des produits et processus spécifiques. |
| Auditeurs qualifiés. | Auditeurs expérimentés et familiers avec la réglementation. |
| Cadre réglementaire | Conforme aux directives ICH , FDA et de Santé Canada. |
| Avantages | Évaluations impartiales, prévention des risques, maintien de la qualité et évolutivité. |
Voici quelques points clés concernant les audits de conformité GxP :
- Examen approfondi : Les audits GxP impliquent un processus d'examen approfondi mené par une organisation tierce ou un consultant qualifié. L'objectif est d'identifier tout domaine de non-conformité au sein de l'organisation et de fournir des recommandations d'amélioration.
- Normes réglementaires : Les réglementations examinées lors de ces audits sont définies par les normes GxP (bonnes pratiques), telles que les Bonnes Pratiques de Fabrication (BPF), les Bonnes Pratiques Cliniques (GCP), et les Bonnes Pratiques de Laboratoire (GLP). Ces normes garantissent que les produits, services et processus répondent constamment aux exigences réglementaires pertinentes.
- Portée personnalisée : La portée d'un audit indépendant est adaptée aux produits et processus spécifiques de l'organisation. Elle peut inclure la gestion du personnel, la gestion des installations, la tenue des dossiers, l'assurance et le contrôle qualité, la conception des produits et des processus, et les opérations techniques.
- Auditeurs qualifiés : L'audit doit être mené par un auditeur qualifié et expérimenté, familier avec les réglementations applicables et possédant l'expertise nécessaire pour évaluer efficacement les procédures et processus de l'organisation.
- Cadre réglementaire: GxP s'appuient sur des cadres tels que le guide Q7AICH(Conférence internationale sur l'harmonisation) relatif aux bonnes pratiques de fabrication, FDA et celles de Santé Canada. Ces cadres fournissent des orientations sur les exigences fondamentales en matière de production, d'assurance qualité, de distribution et d'autres activités essentielles liées à la fabrication de produits en toute sécurité.
- Avantages : Les audits GxP offrent des évaluations impartiales, aident à prévenir les problèmes de non-conformité, maintiennent les normes de qualité et garantissent la responsabilisation. L'externalisation de ces audits donne accès à une expertise, une objectivité, une rentabilité et une évolutivité, tout en permettant aux entreprises de se concentrer sur leurs compétences clés.
Si vous recherchez des solutions de conformité GxP, pensez à Freyr. Nous sommes spécialisés dans la conformité réglementaire, l'assurance qualité et la sécurité au sein de l'industrie des sciences de la vie. Grâce à notre expertise, vous pouvez assurer le respect des normes GxP, optimiser les processus et maintenir des produits et services de haute qualité.
Conseils pour préparer votre organisation à un audit
Préparer votre organisation à un audit est un processus stratégique qui implique une planification méticuleuse et une approche proactive. Tout d'abord, assurez-vous que tous les dossiers, documents et fichiers pertinents sont organisés et facilement accessibles. Un système de classement bien organisé facilite un processus d'audit plus fluide et reflète positivement le professionnalisme de votre organisation.
Deuxièmement, réalisez un pré-audit interne pour identifier les domaines de préoccupation potentiels. Cette auto-évaluation vous permet de résoudre tout problème ou écart avant l'audit externe. En résolvant les problèmes de manière proactive, vous démontrez votre engagement envers la conformité et la transparence.
Troisièmement, communiquez et collaborez efficacement avec l'équipe d'audit. Fournissez les informations nécessaires, l'accès au personnel pertinent et un environnement de travail propice. Une communication claire aide à établir de bonnes relations avec les auditeurs, favorisant une atmosphère de collaboration pendant le processus d'audit.
Enfin, assurez-vous que votre équipe est bien formée et connaît le processus d'audit. Sensibilisez les employés à leurs rôles, leurs responsabilités et l'importance de la conformité. En instaurant une culture de préparation et de coopération, votre organisation pourra gérer les audits avec confiance et professionnalisme.
Comprendre les audits à distance
Qu'est-ce qu'un audit à distance dans l'industrie pharmaceutique, et en quoi diffère-t-il des audits traditionnels sur site ?
Dans le secteur pharmaceutique, un audit à distance consiste en une évaluation exhaustive des processus, des installations et des systèmes d'une entreprise, menée par les autorités réglementaires ou des auditeurs sans présence physique sur place. Cet audit s'appuie sur des outils de communication numériques, des logiciels collaboratifs et l'accès à distance aux documents et systèmes pertinents. Il vise à garantir la conformité aux normes réglementaires, à évaluer les systèmes de gestion de la qualité et à vérifier le respect des bonnes pratiques de fabrication (BPF), des bonnes pratiques cliniques (GCP) ou d'autres réglementations applicables.
La différence entre les audits à distance et les audits traditionnels sur site réside dans l'absence de présence physique lors d'un audit à distance. Au lieu de visiter les locaux de l'entreprise, les auditeurs s'appuient sur des interactions virtuelles, de la documentation électronique et un accès à distance aux systèmes. Cette approche offre flexibilité et efficacité, permettant aux audits d'avoir lieu indépendamment des distances géographiques et des restrictions de voyage. Cependant, des défis tels que l'observation directe limitée des installations et les préoccupations potentielles en matière de cybersécurité doivent être abordés pour garantir l'efficacité des audits à distance.
Malgré les différences, les objectifs des audits à distance et traditionnels restent les mêmes : vérifier la conformité, identifier les domaines à améliorer et garantir la qualité et la sécurité des produits pharmaceutiques. Le choix entre les audits à distance et sur site dépend de facteurs tels que la nature de l'audit, les exigences réglementaires et les capacités de l'entreprise à faciliter une évaluation approfondie par des moyens à distance.
Freyr met à profit une décennie d'expertise pour fournir des solutions réglementaires inégalées, assurant la conformité et le succès dans le paysage pharmaceutique dynamique.
Explorez l'excellence réglementaire avec nous – votre partenaire stratégique pour réussir votre conformité dans l'industrie pharmaceutique en constante évolution. Contactez-nous pour gérer les complexités réglementaires en toute fluidité.
Quels défis peuvent survenir lors des audits à distance, et comment sont-ils traités pour garantir des évaluations approfondies ?
Lors des audits à distance, plusieurs défis peuvent survenir, mais les organisations peuvent prendre des mesures pour y remédier et garantir des évaluations approfondies. Voici quelques défis clés et leurs solutions potentielles :
- Établir des relations clés avec les parties prenantes de l'audit:
- Défi : Le travail à distance peut entraver le développement de relations solides avec les parties prenantes de l'audit.
- Solution : Des réunions virtuelles régulières, une communication ouverte et un engagement actif peuvent aider à construire et à maintenir les relations. Utiliser les appels vidéo pour établir un lien personnel.
- Investir dans la technologie pour le travail virtuel:
- Défi : Les audits à distance dépendent fortement de la technologie, et des outils inadéquats peuvent nuire à l'efficacité.
- Solution : Investir dans des logiciels robustes de gestion d'audit, des plateformes de communication sécurisées et des outils de collaboration. S'assurer que les auditeurs disposent du matériel et des logiciels nécessaires.
- Développement des employés et promotion d'une culture positive à distance.:
- Défi : Le travail à distance peut entraîner l'isolement et nuire à l'évolution professionnelle.
- Solution : Proposer des formations virtuelles, du mentorat et des opportunités de développement des compétences. Favoriser une culture positive par des activités de renforcement d'équipe, la reconnaissance et des points réguliers.
- Cultiver un état d'esprit intentionnel et adaptatif.:
- Défi : Les auditeurs à distance doivent s'adapter aux circonstances changeantes et rester concentrés.
- Solution : Encourager la flexibilité, l'adaptabilité et un état d'esprit de croissance. Former les auditeurs à gérer les situations imprévues et à ajuster leur approche selon les besoins.
Freyr est un partenaire de confiance pour les solutions de conformité réglementaire et de sécurité dans l'industrie des sciences de la vie. Grâce à une expertise approfondie du domaine, une technologie innovante et une présence mondiale, Freyr permet aux organisations de naviguer sans difficulté dans les environnements réglementaires complexes. Découvrez nos services et contactez-nous dès aujourd'hui pour faire progresser votre parcours de conformité.
Comment Freyr est-il le mieux placé pour vous accompagner dans vos audits à distance ?
Fort de son expertise de plus d'une décennie, Freyr excelle dans la facilitation d'audits à distance fluides pour l'industrie pharmaceutique. En tirant parti de technologies avancées et d'une compréhension approfondie des exigences réglementaires, Freyr assure un processus d'audit rigoureux et efficace, en relevant les défis tels que la présence physique limitée et les préoccupations en matière de cybersécurité.
Notre équipe dédiée d'experts en réglementation maîtrise l'utilisation de solutions numériques innovantes, garantissant une évaluation virtuelle complète de vos processus, installations et documentations. Notre expérience avérée en matière d'audits à distance témoigne de notre engagement à fournir des solutions réglementaires fiables et efficaces, adaptées aux besoins changeants du secteur pharmaceutique. Avec Freyr, vous bénéficiez d'un partenaire de confiance qui comprend les subtilités des audits à distance et adopte une approche proactive et collaborative pour renforcer votre démarche de conformité.
Qu'est-ce que la Validation des Systèmes Informatiques (CSV), et pourquoi est-elle cruciale dans l'industrie pharmaceutique ?
La validation des systèmes informatisés (CSV) est un processus essentiel dans l'industrie pharmaceutique qui assure l'intégrité, la fiabilité et la conformité des systèmes informatisés utilisés à diverses fins. Examinons les détails :
- Définition et objectif:
- La CSV est le processus documenté qui garantit qu'un système informatisé produira des informations ou des données répondant à des exigences prédéfinies.
- Son objectif principal est de valider et de vérifier que les systèmes informatiques fonctionnent constamment comme prévu, en maintenant l'exactitude, la fiabilité et la sécurité des données.
- Importance dans le secteur pharmaceutique:
- Conformité réglementaire : L'industrie pharmaceutique opère sous des réglementations strictes (telles que les Bonnes Pratiques de Fabrication ou BPF) pour garantir la qualité, la sécurité et l'efficacité des produits.
- Intégrité des données : Des données exactes et fiables sont cruciales pour le développement de médicaments, les essais cliniques, la fabrication et la distribution.
- Atténuation des risques : La CSV aide à identifier et à atténuer les risques associés aux systèmes informatiques, prévenant les erreurs, la perte de données et la non-conformité.
- Sécurité des patients : Des systèmes correctement validés contribuent à la sécurité des patients en garantissant une qualité constante et le respect des normes.
- Principaux aspects de la CSV:
- Définition des exigences : Définir clairement les exigences du système, les fonctionnalités et les attentes des utilisateurs.
- Conception et configuration : Développer et configurer le système conformément aux spécifications.
- Tests et qualification : Des tests rigoureux (y compris les tests unitaires, les tests d'intégration et les tests d'acceptation utilisateur) pour vérifier la performance du système.
- Documentation : Maintenir une documentation complète tout au long du cycle de vie du système.
- Gestion des changements : Gérer les changements apportés au système, en veillant à ce qu'ils ne compromettent pas son intégrité.
- Défis relevés par la CSV:
- Intégrité des données : Prévenir l'accès non autorisé, la corruption ou la manipulation des données.
- Sécurité du système : Protéger contre les cybermenaces et les modifications non autorisées.
- Piste d'audit : Maintenir une piste d'audit électronique inaltérable pour les audits réglementaires.
- Maintenance de la validation : Examinez et mettez à jour régulièrement la validation pour l'adapter aux changements du système.
En quoi la CSV diffère-t-elle de l'assurance des systèmes informatisés (CSA) ?
La Validation des Systèmes Informatisés (CSV) et l'Assurance des Systèmes Informatisés (CSA) représentent des approches distinctes pour garantir l'intégrité et la conformité des systèmes informatisés dans l'industrie pharmaceutique. La CSV, une pratique établie de longue date, se concentre principalement sur la phase de validation du cycle de vie d'un système, en veillant à ce que les systèmes logiciels répondent aux exigences réglementaires au moyen de protocoles prédéfinis. D'autre part, la CSA adopte une approche plus étendue et dynamique, couvrant l'ensemble du cycle de vie d'un système informatisé, du développement et de la mise en œuvre à l'utilisation opérationnelle et au retrait éventuel.
La CSV répond au besoin de processus de validation rigoureux, en mettant l'accent sur des approches basées sur les risques pour identifier et atténuer les problèmes potentiels. Cependant, le paysage pharmaceutique évolue, entraînant l'émergence de la CSA comme une stratégie plus complète. La CSA élargit son champ d'action au-delà de la validation en adaptant des méthodologies agiles et en intégrant une surveillance continue tout au long du cycle de vie d'un système. Cette perspective globale permet aux organisations de gérer les risques de manière proactive, en particulier en matière de cybersécurité et d'intégrité des données, s'alignant ainsi sur l'importance croissante que l'industrie accorde à la technologie et à la sécurité des données.
La flexibilité de la CSA est un atout précieux dans un environnement réglementaire en constante évolution. Alors que la CSV s'en tient aux pratiques de validation traditionnelles, la CSA s'aligne sur les attentes en constante évolution des autorités réglementaires. Elle va au-delà des efforts de revalidation périodiques en intégrant une surveillance continue, l'analyse des données en temps réel et des stratégies proactives de gestion des risques afin de garantir une conformité permanente et des performances optimales. Alors que l'industrie pharmaceutique s'engage dans la transformation numérique, il devient impératif pour les entreprises qui souhaitent rester à la pointe en matière de conformité réglementaire et d'intégrité des systèmes de comprendre les nuances entre le CSV et le CSA.
Dans ce contexte, Freyr, grâce à sa vaste expérience et son expertise, est bien placée pour guider les entreprises pharmaceutiques à travers les complexités de la CSV et de la CSA, en offrant des solutions sur mesure pour répondre aux exigences évolutives de la conformité réglementaire et aux avancées technologiques.
Quels sont les composants d'un programme CSA ?
L'assurance qualité des logiciels (CSA) est une approche moderne qui améliore la fiabilité, la sécurité et la conformité des systèmes informatisés. Explorons ses composants et ses avantages à long terme :
- Approche basée sur les risques:
- Composant : La CSA se concentre sur l'évaluation et la gestion des risques.
- Importance : L'identification des zones critiques aide à allouer efficacement les efforts de validation.
- Tests non scriptés:
- Composant : La CSA inclut des tests non scriptés au-delà des cas de test scriptés traditionnels.
- Importance : Les tests non scriptés simulent des scénarios réels, révélant ainsi des problèmes cachés.
- Surveillance continue des performances:
- Composant : La CSA implique une surveillance continue des performances du système.
- Importance : La détection précoce des anomalies prévient les défaillances du système et les problèmes d'intégrité des données.
- Supervision des données:
- Composant : La CSA met l'accent sur la qualité et l'intégrité des données.
- Importance : Garantit des données précises pour la prise de décision et la conformité.
- Activités de validation externe:
- Composant : La CSA collabore avec les fournisseurs de logiciels pour la validation externe.
- Importance : La validation indépendante renforce la confiance et réduit les biais.
- Transition du CSV au CSA:
- Étapes initiales:
- Comprendre les principes de la CSA.
- Évaluer les systèmes existants en matière de risque.
- Prioriser les fonctionnalités essentielles.
- Avantages:
- Réduction de la charge de travail de validation.
- Réponse agile aux changements.
- Fiabilité du système renforcée.
- Étapes initiales:
- Fiabilité du système à long terme.:
- La CSA garantit :
- Adaptabilité : Les systèmes évoluent sans compromettre la fiabilité.
- Sécurité : Protection contre les cybermenaces.
- Conformité : Alignement continu avec les réglementations.
- Qualité : Qualité constante des données et des produits.
- La CSA garantit :
Comment le CSA contribue-t-il à l'intégrité des données dans l'industrie pharmaceutique ?
La CSA assure l'intégrité des données au sein de l'industrie pharmaceutique en garantissant l'exactitude, la cohérence et la fiabilité des données tout au long du cycle de vie d'un système. Contrairement aux approches traditionnelles, la CSA adopte une stratégie globale qui va au-delà de la validation, s'attaquant activement aux défis et aux écarts potentiels qui peuvent survenir au fil du temps.
Une contribution de la CSA à l'intégrité des données réside dans ses capacités de surveillance continue. Plutôt que de se fier uniquement aux efforts de validation périodiques, la CSA implique l'analyse de données en temps réel et des mesures proactives de gestion des risques. Cette approche permet aux organisations de détecter et de résoudre les éventuels écarts de données, empêchant les inexactitudes de s'accumuler au fil du temps. L'accent mis par la CSA sur un modèle de cycle de vie dynamique et adaptatif garantit que l'intégrité des données reste une préoccupation constante, s'alignant sur les attentes réglementaires.
Pour prévenir les incohérences de données au fil du temps, le CSA intègre plusieurs mesures stratégiques. Premièrement, il utilise des processus robustes de contrôle des changements, documentant méticuleusement toute modification apportée aux systèmes informatisés ou aux processus susceptible d'affecter l'intégrité des données. Des audits et des évaluations réguliers des systèmes sont menés pour identifier et corriger les problèmes potentiels avant qu'ils ne s'aggravent. De plus, le CSA souligne l'importance des programmes de formation et de sensibilisation des utilisateurs pour s'assurer que le personnel comprend l'importance de maintenir l'intégrité des données et adhère aux meilleures pratiques.
En conclusion, l'approche proactive et complète de CSA en matière d'intégrité des données la distingue comme une solution stratégique dans l'industrie pharmaceutique. En intégrant une surveillance continue, la gestion des risques et des mesures rigoureuses de contrôle des changements, CSA maintient l'intégrité des données et garantit que les entreprises pharmaceutiques sont bien préparées à naviguer dans le paysage évolutif des attentes réglementaires. Alors que les organisations s'efforcent de maintenir les normes les plus élevées en matière d'intégrité des données, CSA apparaît comme un allié clé dans leur parcours, s'alignant sur les tendances de l'industrie et les avancées réglementaires.
Pour les organisations cherchant des conseils sur la mise en œuvre de stratégies CSA efficaces, Freyr est un partenaire fiable offrant des solutions sur mesure pour relever les défis uniques du paysage pharmaceutique.
Quel rôle la conformité réglementaire joue-t-elle dans le CSA ?
La conformité réglementaire est une pierre angulaire de la CSA, garantissant que les entreprises pharmaceutiques respectent les normes et directives évolutives tout au long du cycle de vie d'un système. Contrairement à l'approche traditionnelle de la validation des systèmes informatisés (CSV), la CSA met l'accent sur la conformité continue et l'adaptabilité aux paysages réglementaires en évolution. À mesure que les entreprises passent de la CSV à la CSA, il devient primordial de rester informé des réglementations en constante évolution.
Dans le contexte de la CSA, la conformité réglementaire implique l'alignement des systèmes informatisés avec les exigences réglementaires mondiales et locales, depuis le développement jusqu'à l'utilisation opérationnelle et le retrait éventuel. La CSA met l'accent sur la conformité continue plutôt que sur la validation périodique, favorisant une approche proactive pour répondre rapidement aux changements réglementaires potentiels. Cet alignement stratégique garantit que les entreprises pharmaceutiques sont bien préparées à satisfaire les attentes réglementaires, en protégeant l'intégrité des données, la sécurité des patients et la fiabilité globale du système.

Un dialogue régulier avec les autorités réglementaires, la participation à des forums sectoriels et l'abonnement à des publications réglementaires fournissent des informations précieuses sur l'évolution des normes. Le recours à l'expertise de consultants en réglementation et l'investissement dans la formation continue du personnel impliqué dans les processus CSA renforcent encore davantage la maîtrise des exigences réglementaires. La collaboration avec des partenaires spécialisés dans la réglementation, tels que Freyr Solutions, permet d'adopter une approche proactive, garantissant l'accès à des informations réglementaires actualisées et à des solutions sur mesure pour gérer la transition en toute fluidité.
La conformité réglementaire dans la CSA est un engagement dynamique et continu qui s'aligne sur l'évolution de l'industrie vers l'adaptabilité et l'amélioration continue. Rester informé, proactif et s'associer à des experts en réglementation est crucial pour les entreprises qui passent de la CSV à la CSA, facilitant une évolution fluide et conforme dans le paysage pharmaceutique en constante mutation.
En tant que partenaire réglementaire de confiance, Freyr fournit le soutien et l'expertise nécessaires pour guider les entreprises à travers cette transition, assurant l'excellence et la conformité réglementaires à l'ère du CSA.
Comment un partenaire stratégique en conformité réglementaire peut-il aider ?
Un partenaire stratégique en matière de conformité réglementaire joue un rôle essentiel pour garantir que les entreprises pharmaceutiques respectent les exigences réglementaires et maintiennent des normes de qualité élevées. Voici comment ils peuvent vous aider :
- Conseils d'experts : Un partenaire stratégique offre des conseils d'experts pour naviguer dans les réglementations complexes et en constante évolution à travers différentes régions. Il fournit des informations sur les derniers changements réglementaires, aidant les entreprises à adapter leurs pratiques et à maintenir leur conformité.
- Processus rationalisés : Ils aident à rationaliser les processus de conformité en mettant en œuvre les meilleures pratiques et des flux de travail efficaces. Cela inclut le développement de systèmes robustes pour la documentation, l'audit et la validation, réduisant les charges administratives et améliorant l'efficacité globale.
- Atténuation des risques : En identifiant les risques de conformité et les vulnérabilités potentiels, un partenaire stratégique aide à atténuer les risques avant qu'ils ne deviennent des problèmes. Il mène des audits et des évaluations approfondis pour s'assurer que tous les processus sont conformes et comble proactivement les lacunes.
- Formation et support : Ils offrent une formation et un support pour s'assurer que le personnel est bien informé des exigences réglementaires et des meilleures pratiques. Cela contribue à renforcer les compétences internes et garantit que toutes les personnes impliquées dans les activités de conformité sont à jour avec les normes actuelles.
- Intégration technologique : Un partenaire stratégique aide à l'intégration de technologies innovantes, telles que l'automatisation et l'IA, dans les processus de conformité. Il veille à ce que ces technologies soient mises en œuvre efficacement et conformément aux exigences réglementaires, améliorant ainsi l'intégrité des données et l'efficacité des processus.
- Documentation et tenue des registres : Ils gèrent la création, l'organisation et la maintenance de la documentation essentielle de conformité. Cela garantit que tous les enregistrements sont précis, complets et facilement accessibles pour les audits et les inspections.
- Soumissions et approbations réglementaires : Ils gèrent la préparation et la soumission des documents et demandes réglementaires. Cela inclut de s'assurer que les soumissions respectent toutes les exigences nécessaires et de gérer les communications avec les autorités réglementaires pour faciliter des approbations rapides.
- Actions Correctives et Préventives : Un partenaire stratégique soutient l'élaboration et la mise en œuvre d'actions correctives et préventives en réponse à des constatations d'audit ou à des problèmes de conformité. Il contribue à garantir que ces actions sont efficaces et ne perturbent pas les opérations en cours.
- Stratégie de conformité mondiale : Ils élaborent et mettent en œuvre des stratégies pour atteindre la conformité mondiale, en tenant compte des diverses exigences réglementaires des différents marchés. Cela garantit que les produits respectent toutes les normes nécessaires pour la distribution et l'utilisation internationales.
- Surveillance continue : Ils assurent une surveillance et un soutien continus pour tenir les entreprises informées de toute mise à jour ou modification réglementaire. Cette approche proactive aide les entreprises à rester conformes et à s'adapter aux nouvelles réglementations au fur et à mesure qu'elles apparaissent.
Pourquoi choisir Freyr ?
Plus de dix années d'excellence en conformité réglementaire.
Gamme complète de services de conformité, d'audit et de validation.
Expertise dans diverses industries et zones géographiques.
Utilise des outils innovants pour des résultats précis.
Professionnels qualifiés dotés d'une connaissance approfondie du secteur.
Gestion réussie des défis complexes de conformité.
Foire aux questions
La conformité pharmaceutique implique le respect des lois, réglementations et directives qui régissent l'industrie pharmaceutique. Elle garantit que les entreprises alignent leurs opérations sur les normes de l'industrie, assurant ainsi la sécurité et l'efficacité des produits tout en maintenant l'intégrité des données.
L'objectif d'un audit est d'évaluer systématiquement l'adhésion d'une entreprise aux normes réglementaires et aux politiques internes. Les audits aident à identifier les domaines à améliorer, à atténuer les risques et à garantir que les processus sont efficaces pour produire des produits pharmaceutiques sûrs et conformes.
La validation dans l'industrie pharmaceutique est le processus qui consiste à confirmer que les systèmes, les processus et les équipements répondent constamment aux exigences prédéfinies. Elle est essentielle pour garantir la conformité aux normes réglementaires et pour maintenir la qualité et la sécurité des produits pharmaceutiques tout au long de leur cycle de vie.
Ces processus sont essentiels pour assurer la sécurité et l'efficacité des produits, maintenir la conformité réglementaire, améliorer l'assurance qualité, soutenir l'accès au marché et faciliter l'amélioration continue. Ils aident les entreprises à respecter des normes strictes et à établir la confiance avec les parties prenantes.
Les enjeux comprennent l'adaptation aux réglementations en constante évolution, la garantie de l'intégrité des données, la gestion des contraintes de ressources et le maintien d'une documentation appropriée. De plus, l'intégration de technologies innovantes et la garantie de la compétence du personnel peuvent compliquer les efforts de conformité.
Les audits GxP sont des évaluations menées pour garantir le respect des normes de Bonnes Pratiques (GxP), qui incluent les Bonnes Pratiques de Fabrication (BPF), GCP et GLP. Ces audits aident à identifier les lacunes en matière de conformité et à améliorer les systèmes qualité.
Un audit de conformité GxP indépendant est une évaluation objective de l'adhésion d'une entreprise aux normes de qualité et réglementaires. Mené par des auditeurs qualifiés, il identifie les risques et les domaines d'amélioration, renforçant ainsi la conformité et la sécurité des produits.
Les audits GxP fournissent des évaluations impartiales, améliorent la conformité réglementaire et identifient les domaines d'amélioration opérationnelle. Ils contribuent à maintenir des normes de qualité élevées et à renforcer la confiance des régulateurs et des clients.
La CSV garantit que les systèmes informatisés utilisés dans l'industrie pharmaceutique produisent constamment des données fiables et répondent aux exigences réglementaires. Elle est essentielle pour maintenir l'intégrité des données, atténuer les risques et assurer la sécurité des patients tout au long du cycle de vie du produit.
La CSV se concentre sur la validation qu'un système répond aux exigences réglementaires et fonctionne comme prévu, tandis que la CSA englobe une approche plus large qui inclut une assurance continue de la performance et de la conformité du système tout au long de son cycle de vie.














