La rédaction réglementaire joue un rôle crucial dans les industries pharmaceutique et de la santé, en faisant le lien entre des informations scientifiques complexes et diverses parties prenantes. L'art d'adapter la rédaction réglementaire à différents publics est essentiel pour une communication et une conformité efficaces. Ce blog explorera comment adapter la rédaction réglementaire pour trois (3) publics clés : les patients, les cliniciens et les régulateurs.
Comprendre l'importance d'une rédaction adaptée à l'audience
La rédaction réglementaire englobe divers documents, chacun ayant un objectif spécifique et ciblant différents lecteurs. La capacité d'adapter le contenu à ces publics divers est essentielle pour garantir que l'information est exacte, mais aussi accessible et exploitable.
Points clés à considérer pour l'approche d'adaptation :
Rédaction pour les patients : Simplifier les informations complexes
Lors de la rédaction de documents réglementaires pour les patients, l'objectif principal est de transmettre des informations essentielles de manière claire et compréhensible sans sacrifier la précision.
- Utilisation d'un langage clair et simple
Utilisez des mots courants et évitez le jargon technique. Lorsque des termes médicaux sont nécessaires, fournissez des explications claires.
- Aides visuelles et mise en forme
Intégrez des diagrammes, des graphiques et des infographies pour illustrer des concepts complexes. Utilisez des listes à puces, des titres et des paragraphes courts pour améliorer la lisibilité.
- Répondre aux préoccupations courantes
Anticiper et répondre aux questions ou préoccupations potentielles que les patients pourraient avoir concernant le médicament ou le traitement.
Exemple : Notices d'information destinées aux patients
Ces documents doivent :

Rédaction pour les cliniciens : Équilibrer le détail et la praticité
Les cliniciens ont besoin d'informations complètes mais concises pour prendre des décisions éclairées concernant les soins aux patients. La rédaction réglementaire pour ce public doit équilibrer les détails scientifiques et l'applicabilité pratique.
- Accent mis sur la pertinence clinique
Se concentrer sur les informations ayant un impact sur les soins aux patients, telles que les directives posologiques, les contre-indications et les interactions médicamenteuses.
- Présentation structurée des données
Organisez les résultats des essais cliniques et les données de sécurité dans un format logique et facile à consulter. Utilisez des tableaux et des graphiques pour résumer les principales conclusions.
- Inclusion de recommandations fondées sur des preuves.
Fournir des orientations claires et fondées sur des preuves concernant l'utilisation appropriée des médicaments ou des dispositifs médicaux dans divers scénarios cliniques.
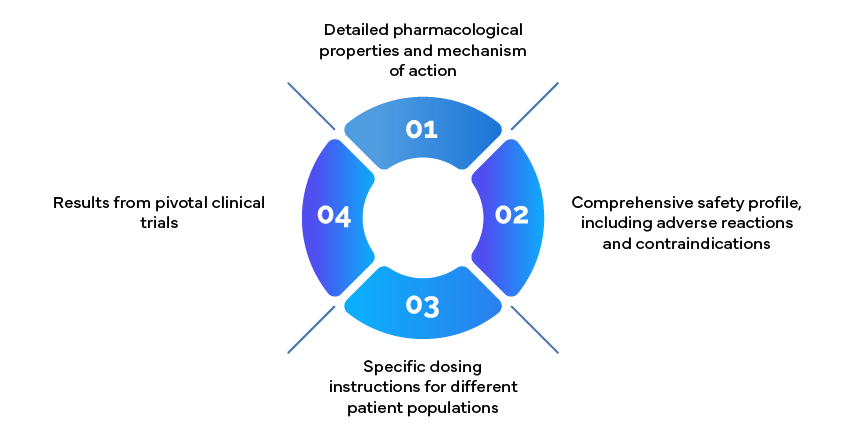
Exemple : Informations de prescription
Les documents d'information sur la prescription, également appelés notices d'emballage, sont des ressources essentielles pour les cliniciens. Ils doivent inclure :
Rédaction pour les régulateurs : Précision et conformité
Les agences réglementaires exigent une documentation exhaustive et scientifiquement rigoureuse pour évaluer la sécurité et l'efficacité des nouveaux produits. La rédaction pour ce public exige une attention méticuleuse aux détails et un respect strict des directives réglementaires.
- Respect des directives réglementaires
Veillez à ce que tous les documents respectent les exigences spécifiques en matière de format et de contenu imposées par les organismes de réglementation tels que la FDA EMA.
- Présentation complète des données
Fournir une analyse approfondie de toutes les données pertinentes, y compris des descriptions détaillées des méthodologies d'étude, des analyses statistiques et de l'interprétation des résultats.
- Transparence des rapports
Divulguer toute limitation ou tout biais potentiel dans la recherche et expliquer comment ces facteurs peuvent influencer les conclusions.
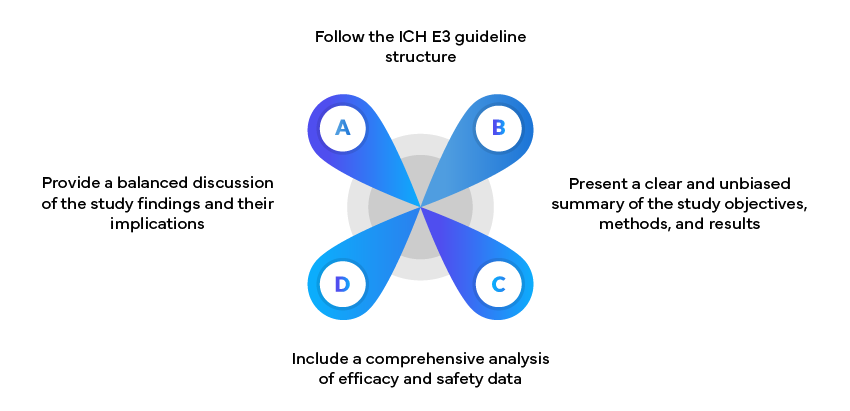
Exemple : Rapports d'études cliniques
Les rapports d'études cliniques (CSR) sont des documents essentiels dans les soumissions réglementaires. Ceux-ci doivent :
Conclusion
Adapter la rédaction réglementaire pour différents publics est une tâche complexe mais essentielle dans les industries pharmaceutique et de la santé. En adaptant le contenu et les styles de présentation pour répondre aux besoins spécifiques des patients, des cliniciens et des régulateurs, les rédacteurs peuvent s'assurer que les informations critiques sont communiquées et comprises efficacement.
La capacité à rédiger des documents réglementaires clairs, précis et adaptés au public n'est pas seulement une question de conformité ; elle a un impact direct sur la sécurité des patients, la prise de décision clinique, ainsi que sur le développement et la commercialisation réussis de nouveaux produits de santé. Alors que le paysage réglementaire continue d'évoluer, l'importance d'une rédaction réglementaire qualifiée, capable de combler le fossé entre des données scientifiques complexes et les besoins variés des parties prenantes, ne fera que croître. Les rédacteurs réglementaires jouent un rôle crucial dans l'amélioration de la santé publique et la promotion de l'innovation dans le domaine médical en se concentrant sur la clarté pour les patients, la pertinence clinique pour les professionnels de la santé et une précision exhaustive pour les régulateurs. Maîtriser l'art de la rédaction réglementaire adaptée à un public spécifique est donc une compétence inestimable dans l'environnement de la santé en rapide évolution d'aujourd'hui.










