Übersicht zur Registrierung von Medizinprodukten in Kolumbien
Kolumbien bietet enorme Chancen für Medizinprodukteunternehmen. Sein Gesundheitssystem ist bekannt für sein Engagement für Patientensicherheit und die Qualität medizinischer Dienstleistungen. Die Regulierung von Medizinprodukten erfolgt durch INVIMA (das Nationale Institut für Lebensmittel- und Arzneimittelüberwachung). INVIMA ist die zuständige Behörde für die Registrierung von Medizinprodukten in Kolumbien.

Aufsichtsbehörde: INVIMA (das Nationale Institut für Lebensmittel- und Arzneimittelüberwachung)
Verordnung: Dekret 4725/2005
Regulatorischer Weg: Registrierung von Medizinprodukten
Bevollmächtigter Vertreter: Rechtsvertreter in Kolumbien
QMS-Anforderung: ISO 13485:2016 / MDSAP
Bewertung technischer Daten: INVIMA
Kennzeichnungspflichten: Kennzeichnungsdokumente müssen in spanischer Sprache verfasst sein
Gültigkeit der Lizenz: 10 Jahre
Einreichungsformat: Elektronisch
Klassifizierung von Medizinprodukten in Kolumbien
| Medizinprodukteklassifizierung | |
|---|---|
| Klasse I (Geringstes Risiko) | |
| Klasse IIa | |
| Klasse IIb | |
| Klasse III (Höchstes Risiko) | |
Rechtsvertreter in Kolumbien
Um als Rechtsvertreter in Kolumbien tätig zu sein, muss man entweder die kolumbianische Staatsbürgerschaft besitzen oder die erforderliche rechtliche Genehmigung haben, um als ausländischer Staatsangehöriger im Land zu leben und zu arbeiten. Ein Rechtsvertreter kann bei allen Registrierungsverfahren in Kolumbien unterstützen und diese verwalten. Er fungiert dabei als Bindeglied zwischen dem Unternehmen und INVIMA, der lokalen Regulierungsbehörde.
Registrierung von Medizinprodukten in Kolumbien
Medizinprodukte und IVDs unterliegen einem Registrierungsverfahren. Daher müssen Medizinprodukte bei INVIMA registriert werden, um in Kolumbien vermarktet werden zu können.
Um ein Medizinprodukt in Kolumbien zu vermarkten, ist es erforderlich, ein Freiverkaufszertifikat (Certificate of Free Sale, CFS) oder ein Zertifikat für ausländische Regierungen (Certificate to Foreign Government, CFG) zu erhalten. Dieses muss von der zuständigen Regulierungsbehörde im Ursprungsland oder einem anerkannten Referenzland (z. B. Kanada, Japan, Australien, der Europäischen Union und den US) ausgestellt werden. Das Freiverkaufszertifikat oder das Zertifikat für ausländische Regierungen dient als Nachweis dafür, dass das Medizinprodukt die erforderlichen Sicherheits- und Qualitätsstandards für den Verkauf in Kolumbien erfüllt.
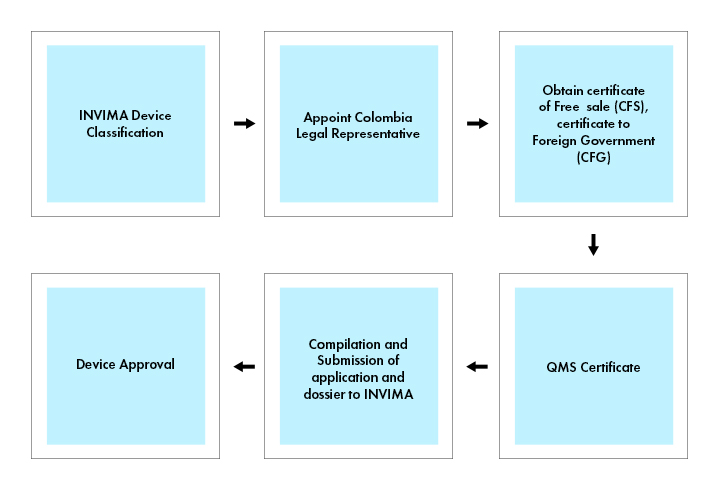
Prozessablauf
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel:
- Änderungsmanagement nach der Zulassung – Änderungen an bestehenden Medizinprodukte-Zulassungen, wie z.B. die Hinzufügung neuer Varianten, Zubehörteile; die Hinzufügung neuer Anwendungsgebiete und Ähnliches
- Aufrechterhaltung von Genehmigungen und Registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren
- Verlängerung von Lizenzen
- Koordination zwischen INVIMA und dem Hersteller
Zusammenfassung
| Medizinprodukteklassifizierung | Neue Lizenzen und Verlängerungen | ||
|---|---|---|---|
| Neuregistrierung | Änderung | Verlängerung | |
| Klasse I | 4-6 Monate | 2-3 Monate | 4-6 Monate |
| Klasse IIa | 4-6 Monate | 2-3 Monate | 4-6 Monate |
| Klasse IIb | 4-6 Monate | 2-3 Monate | 4-6 Monate |
| Klasse III | 4-6 Monate | 2-3 Monate | 4-6 Monate |
| Registrierungsgebühren | |||||
|---|---|---|---|---|---|
| Neue Lizenzen und Verlängerungen | Technische Änderungen | Administrative Änderungen | |||
| Klasse I & Klasse IIa | Klasse IIb & Klasse III | Klasse I & Klasse IIa | Klasse IIb & Klasse III | Klasse I & Klasse IIa | Klasse IIb & Klasse III |
| $ 690,00 | $ 776,00 | $ 196,00 | $ 196,00 | $ 153,00 | $ 153,01 |
Freyr Expertise
- Regulatorische Due Diligence
- Offizielle Klassifizierung
- Registrierung von Medizinprodukten
- Registrierungsinhaber in Kolumbien
- Kennzeichnungsunterstützung
- Übersetzungsunterstützung
- Identifizierung und Qualifizierung von Vertriebspartnern
- Marktüberwachung nach dem Inverkehrbringen
- Änderungsmanagement nach der Zulassung
- Lizenzverlängerung und -übertragung
- Einreichung und Kontakt mit der INVIMA