Übersicht zum Bericht zur wissenschaftlichen Validität (SVR)
Der Bericht zur wissenschaftlichen Validität (SVR) ist von größter Bedeutung innerhalb des Leistungsbewertungsberichts (PER) für In-vitro-Diagnostika (IVD) gemäß der Verordnung (EU) 2017/746 über In-vitro-Diagnostika (EU IVDR). Der SVR spielt eine entscheidende Rolle bei der wissenschaftlichen Validierung der analytischen und klinischen Leistung des Produkts, um die Sicherheit und Wirksamkeit der auf dem Markt erhältlichen Medizinprodukte zu gewährleisten. Im Rahmen des vorgeschriebenen Konformitätsbewertungsverfahrens der EU IVDR müssen Hersteller einer benannten Stelle einen PER vorlegen, der einen SVR enthalten muss, um die Sicherheit und Leistung des Produkts vor seiner Einführung auf dem EU-Markt nachzuweisen.
Berichte zur wissenschaftlichen Validität für die EU IVDR-Einreichung
- Analyse und Schlussfolgerungen
Was beinhaltet der Bericht zur wissenschaftlichen Validität (SVR)?
Die wissenschaftliche Validität eines Analyten bedeutet die Verbindung eines Analyten mit einem klinischen oder physiologischen Zustand. Die wissenschaftliche Validität eines IVD basiert hauptsächlich auf einer oder einer Kombination der folgenden Quellen:
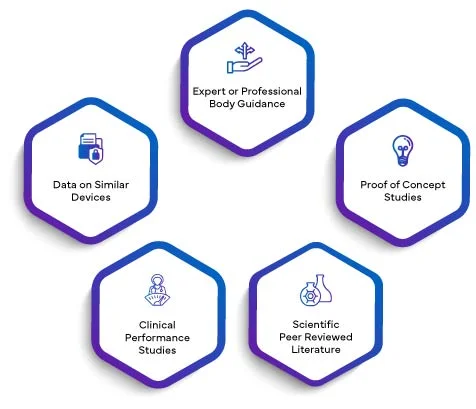
Gegebenenfalls werden Daten aus allen oben genannten Quellen in einem Bericht zur wissenschaftlichen Validität zusammengefasst. Durch die Integration des SVR in den PER heben Hersteller ihre Leistungsbewertung auf eine höhere Ebene der Glaubwürdigkeit. Die durch den SVR hergestellte wissenschaftliche Validität verleiht dem PER eine solide Grundlage und erhöht dessen Gesamtqualität und Bedeutung. Dies wiederum schafft Vertrauen bei Regulierungsbehörden, medizinischem Fachpersonal und Endverbrauchern und stellt sicher, dass die Leistung des IVD gemäß den strengen Anforderungen der EU IVDR 2017/746 sorgfältig bewertet und validiert wird.
Freyr bietet umfassende Unterstützung bei der Erstellung eines soliden Berichts zur wissenschaftlichen Validität (SVR) für IVDs, damit Sie sich sicher in der regulatorischen Landschaft zurechtfinden und sichere und wirksame IVD-Produkte reibungslos auf den Markt bringen können.
Bericht zur wissenschaftlichen Validität
- Übergangsplan für die IVDR-Konformität.
- Bericht zur wissenschaftlichen Validität (SVR) basierend auf Literatur und/oder internen Daten.
- Berichte zur klinischen Leistung (CPR) basierend auf Literatur und/oder internen Daten.
- Berichte zur analytischen Leistung (APR)
- Klinische Evidenz oder Berichte zur Leistungsbewertung gemäß IVDR.
- Plan zur Leistungsbewertung.
- Protokolle und Berichte zur Überwachung der Leistung nach dem Inverkehrbringen (PMPF).
- Protokolle und Berichte zur Marktüberwachung (PMSR).
- Erstellung/Überarbeitung anderer Dokumente, wie z.B. Packungsbeilage/Gebrauchsanweisung (IFU), Kurzanleitungen (QRI), Bedienungs-/Benutzerhandbuch usw.

- Gesicherte Einhaltung der neuesten geltenden Vorschriften.
- Qualifiziertes Expertenteam
- Maßgeschneiderte Lösungen für Ihre Anforderungen
- Regulierungsressourcenmanagement / Personalaufstockungsdienste
- Funktionsübergreifende Beiträge von Medizinprodukteexperten zur Einhaltung der Anforderungen.

Häufig gestellte Fragen
01. Was ist ein Scientific Validity Report (SVR) gemäß der EU-IVDR?
Ein Bericht zur wissenschaftlichen Validität (SVR) dokumentiert Nachweise, die einen Analyten mit einem klinischen Zustand oder physiologischen Status in Verbindung bringen, und ist ein grundlegender Bestandteil des Leistungsbewertungsberichts (PER), der gemäß EU-IVDR 2017/746 für IVD-Produkte erforderlich ist. Er zeigt, dass die wissenschaftliche Begründung des Produkts durch Literatur oder Studiendaten gestützt wird, wodurch die Sicherheit und Wirksamkeit des Produkts gewährleistet ist.
02. Warum ist der SVR für die Leistungsbewertung von IVD-Produkten entscheidend?
Der SVR ist für die Leistungsbewertung entscheidend, da er die wissenschaftliche Validität des IVD-Produkts herstellt, indem er die Verbindung zwischen dem Analyten und dem klinischen Zustand oder physiologischen Status aufzeigt. Er bildet die wissenschaftliche Grundlage für den vorgesehenen Zweck des Produkts und untermauert die klinischen Leistungsansprüche. Ein robuster SVR stärkt den gesamten Leistungsbewertungsbericht (PER) und ermöglicht es Benannten Stellen zu beurteilen, ob die Verwendung des Produkts klinisch gerechtfertigt, sicher und konform mit der In-vitro-Diagnostika-Verordnung ist.
03. Welche Arten von Nachweisen stützen die wissenschaftliche Validität in einem SVR?
Die wissenschaftliche Validität wird in der Regel durch verschiedene Belege nachgewiesen. Dazu gehören zum Beispiel Fachliteratur, die von Experten geprüft wurde, klinische Studien, Daten aus dem Vergleich mit ähnlichen Produkten und anerkannte aktuelle Standards. Diese Belege müssen den Analyten klar mit der jeweiligen Krankheit oder dem klinischen Zustand in Verbindung bringen.
04. Worin unterscheidet sich der SVR von Berichten zur analytischen und klinischen Leistung?
Der SVR konzentriert sich darauf, die wissenschaftliche Begründung für die Verbindung eines Analyten mit einem klinischen Zustand zu belegen. Berichte zur analytischen Leistung bewerten die Messgenauigkeit, und Berichte zur klinischen Leistung beurteilen die Ergebnisse der Leistung im praktischen Einsatz. Zusammen bilden diese den vollständigen PER.
05. Wann sollten Hersteller mit der Planung des SVR beginnen?
Hersteller sollten den SVR frühzeitig in der Entwicklung planen, idealerweise parallel zur Planung der Leistungsbewertung. Dies hilft, den klinischen Kontext, die Strategie zur Literaturrecherche und die regulatorischen Erwartungen aufeinander abzustimmen, wodurch Nacharbeiten minimiert und eine solide Datenbasis sichergestellt werden.
06. Was sind häufige Herausforderungen bei der Erstellung eines Berichts zur wissenschaftlichen Validität?
Zu den größten Herausforderungen gehören die Definition des beabsichtigten klinischen Kontexts, die Auswahl relevanter Literatur, die Sicherstellung der Qualität der Nachweise sowie die Zusammenfassung von Schlussfolgerungen, die die wissenschaftliche Validität für die regulatorische Prüfung klar begründen. Oft sind eine Expertenstrategie und systematische Überprüfungstechniken erforderlich.
07. Wie unterstützt der SVR regulatorische Einreichungen bei Benannten Stellen?
Ein gut erstellter SVR verbessert die Qualität des Leistungsbewertungsberichts, indem er Nachweise und Begründungen klar darlegt. Dies ermöglicht eine reibungslosere Konformitätsbewertung und erhöht das Vertrauen der regulatorischen Prüfer in die wissenschaftliche Grundlage des IVD.
08. Warum gilt Freyr als führender Partner für Dienstleistungen im Bereich der Berichte zur wissenschaftlichen Validität?
Freyr verfügt über umfassende regulatorische Expertise und einen strukturierten Ansatz für die SVR-Erstellung gemäß der EU-IVDR. Dies ermöglicht Herstellern, komplexe Nachweisanforderungen souverän zu erfüllen und gleichzeitig das Risiko einer verzögerten Einreichung zu minimieren. Die nachweisliche Leistung bei verschiedenen IVD-Portfolios unterstreicht Freyrs Rolle als vertrauenswürdiger Partner für regulatorische Exzellenz.








