Compliance-, Audit- und Validierungsdienstleistungen – Übersicht
Erfüllen Sie die Vorschriften? Diese Frage ist für jedes Unternehmen aus den Bereichen Pharmazie, Biotechnologie, Genomik, Chemie, Medizinprodukte und Lieferkettenmanagement schwer zu beantworten. Diese Unternehmen müssen in jeder Region, in der ihre Produkte vertrieben werden, strenge Qualitäts-, Sicherheits- und Compliance-Anforderungen erfüllen. Der aktuelle Trend im Bereich des regulatorischen Compliance-Managements geht in Richtung einer globalen Harmonisierung von Qualität und Sicherheit, wobei der Schwerpunkt auf soliden Praktiken liegt. Unabhängig davon, ob Sie Hersteller oder Zulieferer sind, hängen Ihre Marktexpansion, Ihre kontinuierliche Verbesserung und Ihre Kundenzufriedenheit in erster Linie von den Qualitätsstandards Ihres Unternehmens ab. Das Regulatory Compliance, Audit and Validation Center of Excellence (CoE) von Freyr kann Sie dabei unterstützen, indem es Ihnen professionelle Compliance-, Audit- und Validierungsdienstleistungen für die Pharma-, Medizinprodukte-, Konsumgüter- und Gesundheitsbranche bietet, darunter cGMP (Current Good Manufacturing Practices), GCP Good Clinical Practice), GDP Good Distribution Practice), Good Laboratory Practice (GLP), GPVP Good Pharmacovigilance Practice) undGxP-Computersystemvalidierung (CSV). Unser Beratungsteam für pharmazeutische Compliance bietet maßgeschneiderte Lösungen für Ihre individuellen Compliance-Herausforderungen.
Freyr bietet Dienstleistungen in den Bereichen regulatorische Compliance, Auditierung und Validierung an, die die Bewertung Ihrer Anforderungen sowie Vorschläge zur Optimierung von Geschäftsprozessen umfassen, um die Kundenzufriedenheit sicherzustellen. Mit unseren Strategien zur Erstellung von Compliance-Auditberichten und zur Vorbereitung auf Audits erstellen wir Compliance- und Auditberichte (Lückenanalysen), einschließlich Vorschlägen für Korrektur- und Vorbeugungsmaßnahmen (CAPA), um potenzielle 483-Einträge und Beanstandungen bei Compliance-Audits durch die Aufsichtsbehörden zu vermeiden. Die pharmazeutische Compliance-Beratung von Freyr erstreckt sich auch auf die Beratung zur Compliance bei der Pharma-Automatisierung und stellt sicher, dass Ihre automatisierten Systeme den sich wandelnden regulatorischen Erwartungen entsprechen. Unser umfassender Ansatz für das Compliance-Management gewährleistet, dass jede Phase Ihres Prozesslebenszyklus überwacht und im Hinblick auf die Einhaltung regulatorischer Vorgaben optimiert wird.
Wir bieten Dienstleistungen im Bereich der Einhaltung gesetzlicher Vorschriften und der Validierung an, um sicherzustellen, dass alle Ihre Prozesse und Produkte den geltenden Anforderungen an Qualität, Informationssicherheit und die Einhaltung gesetzlicher Vorschriften entsprechen, wie beispielsweise (unter anderem) den folgenden:
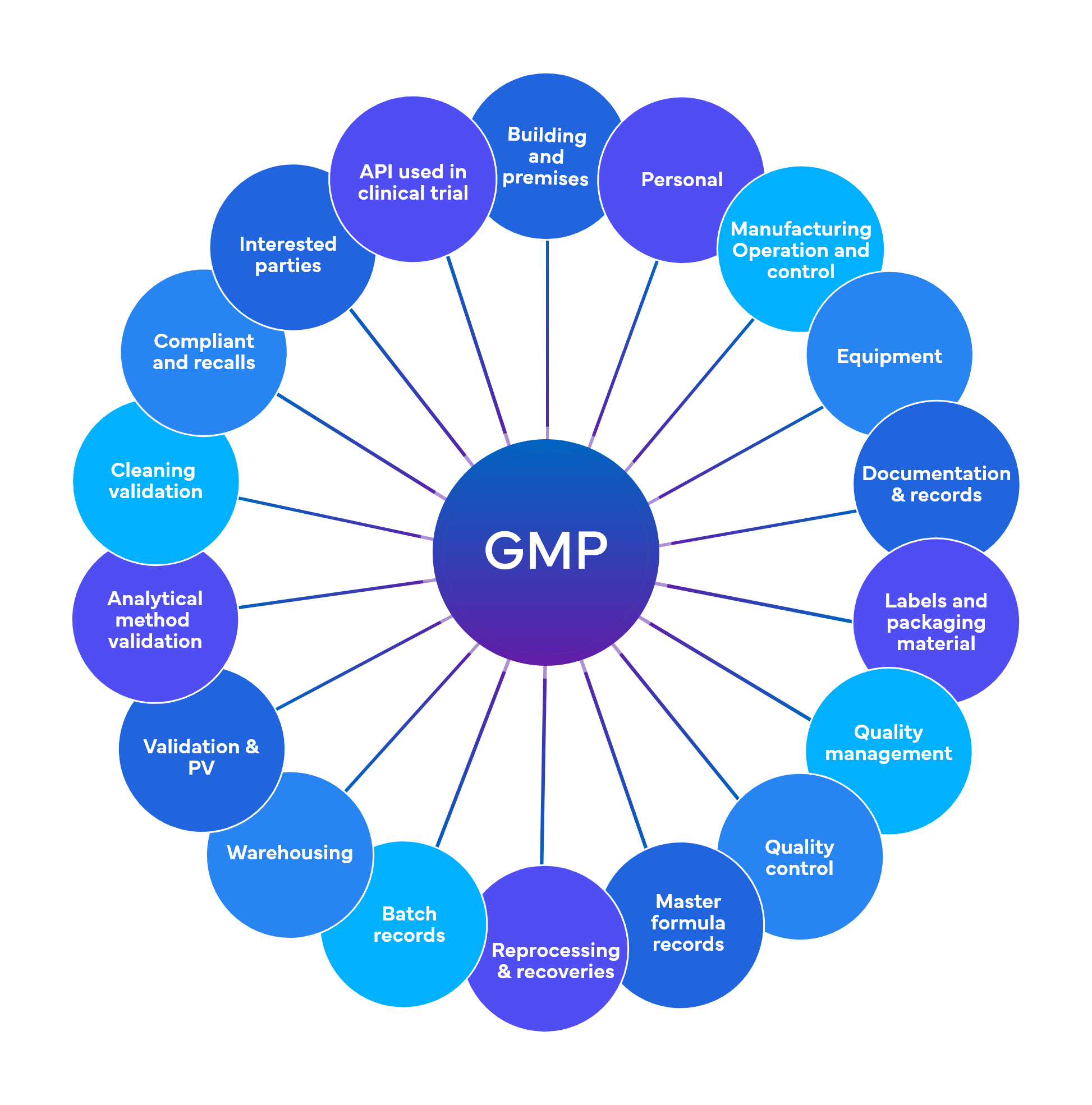
Freyr führt rund 700 Prüfungen auf einer vorläufigen Ebene durch, verteilt auf 18-19 GMP-Funktionsbereiche
Freyr: Compliance, Audit und Validierung
Compliance-, Audit- und Validierungsdienstleistungen
Qualität und regulatorische Compliance – Aktuelle Gute Herstellungspraxis (cGMP)
- ISO / IEC 17025: 2017 – Allgemeine Anforderungen an die Kompetenz von Prüf- und Kalibrierlaboratorien
- OECD (Organisation für wirtschaftliche Zusammenarbeit und Entwicklung) – Leitlinien zur Guten Laborpraxis
- EURACHEM / CITAC Leitfaden: Leitfaden zur Qualität in der Analytischen Chemie – Eine Hilfe zur Akkreditierung, 3. Auflage (2016), ist bei analytischen Verfahren zu beachten.
- 21 CFR 58: Gute Laborpraxis für nicht-klinische Laborstudien
- Leitfaden zu den GLP-Vorschriften im Vereinigten Königreich, Feb. 2000 (von GLPMA)
- WHO-Handbuch zur Guten Laborpraxis (GLP): Qualitätspraktiken für regulierte nicht-klinische Forschung und Entwicklung
- Health Canada: Finalisiertes Leitliniendokument – Daten aus nicht-klinischen Laborstudien zur Unterstützung von Arzneimittelanträgen und -einreichungen: Einhaltung der Guten Laborpraxis
- OSHA (Arbeitsschutzbehörde) Standards
- Anwendbare ICH-Leitlinien
Gute Laborpraxis
- ISO / IEC 17025: 2017 – Allgemeine Anforderungen an die Kompetenz von Prüf- und Kalibrierlaboratorien
- OECD (Organisation für wirtschaftliche Zusammenarbeit und Entwicklung) – Leitlinien zur Guten Laborpraxis
- EURACHEM / CITAC Leitfaden: Leitfaden zur Qualität in der Analytischen Chemie – Eine Hilfe zur Akkreditierung, 3. Auflage (2016), ist bei analytischen Verfahren zu beachten.
- 21 CFR 58: Gute Laborpraxis für nicht-klinische Laborstudien
- Leitfaden zu den GLP-Vorschriften im Vereinigten Königreich, Feb. 2000 (von GLPMA)
- WHO-Handbuch zur Guten Laborpraxis (GLP): Qualitätspraktiken für regulierte nicht-klinische Forschung und Entwicklung
- Health Canada: Finalisiertes Leitliniendokument – Daten aus nicht-klinischen Laborstudien zur Unterstützung von Arzneimittelanträgen und -einreichungen: Einhaltung der Guten Laborpraxis
- OSHA (Arbeitsschutzbehörde) Standards
- Anwendbare ICH-Leitlinien
Gute Klinische Praxis (GCP) und Gute Pharmakovigilanz-Praxis (GVP)
- ICH Harmonisierte Dreigliedrige Leitlinie: Leitlinie für Gute Klinische Praxis – E6
- E2B(R3) Spezifikation für individuelle Fallberichte zur Sicherheit (ICSR) und zugehörige Dateien
- E2C(R2) Periodischer Nutzen-Risiko-Bewertungsbericht (PBRER)
- Weitere anwendbare ICH-Leitlinien
- Leitlinien zu Guten Pharmakovigilanz-Praktiken (GVP) Modulen
- FDA-Anforderungen an die Sicherheitsberichterstattung für INDs und BA/BE-Studien
- Sicherheitsberichterstattung nach der Markteinführung für Humanarzneimittel und biologische Produkte, einschließlich Impfstoffe
- FDA Regionale Implementierungsspezifikationen für die ICH E2B(R3)-Berichterstattung an das FDA Adverse Event Reporting System (FAERS)
- Bereitstellung von Einreichungen in elektronischem Format – Nicht beschleunigte Einzelfall-Sicherheitsberichte nach der Markteinführung: Technische Fragen und Antworten
- End-to-End Pharmakovigilanz-Planung
Informationssicherheit, Datenschutz und Validierung von Computersystemen (CSV)
- ISO 27001: 2013 Informationstechnologie – Sicherheitstechniken – Informationssicherheits-Managementsystem – Anforderungen
- ISO 27002: 2013 Informationstechnologie – Sicherheitstechniken – Leitfaden für das Informationssicherheitsmanagement
- USFDA 21 CFR Part 11: Elektronische Aufzeichnungen; Elektronische Signaturen – Geltungsbereich und Anwendung
- EU-GMP-Leitfaden Anhang 11
- Japanische ERES-Leitlinie Mitteilung Nr. 0401022
- GAMP 5: Ein risikobasierter Ansatz für konforme GxP-Computersysteme
- USFDA – Leitlinien zur Softwarevalidierung
- Anwendbare ICH QSEM-Leitlinien
- SOPs planen, erstellen und Fertigungsanlagen steuern
- Integriertes Prozessmodell
- Markenimage pflegen
- Risikobewertungsdienste
- Gesamtkosteneinsparungen
- Effektive und regelkonforme Geschäftsprozesse umsetzen
- Validierungs- und Qualifizierungsstrategien festlegen
- Fachwissen in regulatorischer und Audit-Konformität
- Erfahrene Compliance-Auditoren
Unser Beratungsansatz in den Bereichen Qualität und Compliance zielt darauf ab, umsetzbare Erkenntnisse und nachhaltige Verbesserungen zu liefern und Ihr Unternehmen dabei zu unterstützen, operative Exzellenz und regulatorischen Erfolg zu erreichen.



 Compliance- und Audit-Dienstleistungen
Compliance- und Audit-Dienstleistungen










