Dienstleistungen für die klinische Kennzeichnung – Überblick
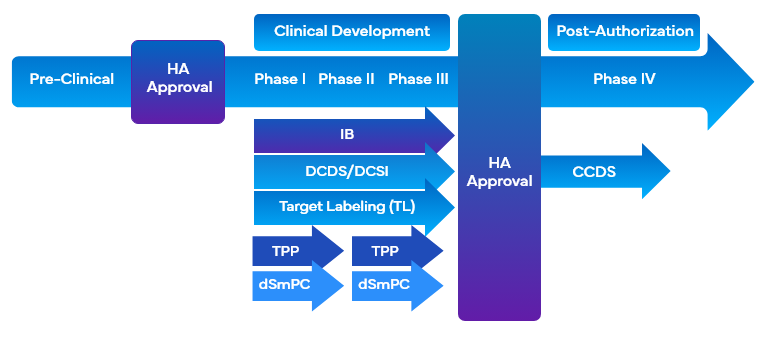
Bei der Arzneimittelentwicklung nutzen Unternehmen eine Vielzahl von Tools für die klinische Kennzeichnung, die auf Zielkennzeichnung basieren, um die Arzneimittelentwicklung zu erleichtern. Diese Tools stimmen die angestrebten Ziele hinsichtlich der Vermarktung und der Kennzeichnung in klinischen Studien gleichzeitig mit der Entwicklung des Programm- oder Studiendesigns ab und erleichtern die Erstellung des Clinical Overview (CO). Zu den Tools für die klinische Kennzeichnung, die bei der Arzneimittelentwicklung auf Zielkennzeichnung basieren, gehören:
- Prüferinformation (IB)
- Zielkennzeichnung (TL)/Zielprofil
- Development Core Data Sheet (DCDS)
- Entwicklung von Kern-Sicherheitsinformationen (DCSI)
- FDA Zielproduktprofil (TPP)
Für Unternehmen ist es wichtig, bei der Sammlung von Sicherheits- und Wirksamkeitsinformationen für verschiedene Arten von klinischen Kennzeichnungen einen modularen Ansatz zu verwenden. So können die Anforderungen an die klinische Kennzeichnung optimal erfüllt werden. Dies würde Prüfärzte und Sponsoren wirksam unterstützen, indem ein gezielter und spezieller DCSI-Abschnitt bereitgestellt und aktualisiert wird, der sich leicht in verschiedene klinische Kategorien einordnen lässt.
Darüber hinaus sind DCSI Teil der Kern-Sicherheitsinformationen des Unternehmens (CCSI). Diese bilden die Grundlage für das erste Kern-Datenblatt des Unternehmens (CCDS) und werden für die Markteinführung des Produkts genutzt. Auch die Erstellung eines detaillierten CO, das den Umfang und die wichtigen Punkte des klinischen Entwicklungsprogramms für das Medikament enthält, ist notwendig, um die Unterlagen für die Prüfer zu unterstützen.
Freyrs Dienstleistungen für klinische Kennzeichnungen
Dienstleistungen für die klinische Kennzeichnung
Erstellung und Überprüfung der Prüfarztbroschüre (IB)
Freyr verfügt über umfangreiche Erfahrung in der Erstellung, Ausarbeitung und Überprüfung von Prüfprotokollen für verschiedene klinische Programme unserer Kunden. IBs sind die frühesten Formen von Begleitdokumenten, die dem Prüfer oder behandelnden Arzt relevante Informationen über das Prüfpräparat bzw. die Intervention liefern sollen. Ihr Zweck besteht darin, den Prüfern und anderen an der Studie beteiligten Personen die notwendigen Informationen zu geben, um ihnen das Verständnis der Gründe für viele wichtige Merkmale des Protokolls sowie deren Einhaltung zu erleichtern. Dazu gehören Dosierung, Dosierungshäufigkeit/-intervall, Verabreichungsmethoden und Verfahren zur Sicherheitsüberwachung. Das IB präklinische und klinische Informationen zu einem Prüfpräparat.

Bei der Erstellung von IBs präsentieren Freyrs Experten für klinische Kennzeichnungen die Informationen prägnant, einfach, objektiv und ausgewogen. Dieselben Eigenschaften können auch bei der Übersetzung von Dokumenten berücksichtigt werden. Neben der Verfassung von IBs unterstützt Freyr auch die jährliche Überprüfung der IBs und nimmt bei Bedarf Überarbeitungen vor, stets in Übereinstimmung mit den von Kunden und Sponsoren festgelegten Standardverfahren.
Entwicklung der Zielkennzeichnung (TL)/des Zielprofils
Entwicklung und Überprüfung von DCDS & DCSI
Freyr verfügt über nachgewiesene Expertise bei der Erstellung hochwertiger Developmental Core Data Sheets (DCDS). Das DCDS ist ein wichtiges, zwischengeschaltetes Kernetikett, das entscheidend ist, um die Inhalte für die ersten nationalen Kennzeichnungen (wie USPI, SmPC usw.) zu entwickeln. Das DCDS/DCSI wird aus der Zielkennzeichnung erstellt und bietet integrierte Sicherheits- und Wirksamkeitsinformationen für eine Intervention oder ein Medikament. Das DCDS/DCSI unterstützt Prüfärzte und Sponsoren, indem es fokussierte und spezielle DCDS-Abschnitte bereitstellt und aktualisiert, die bequem in den IB eingefügt werden können. Das DCSI erleichtert die Entwicklung des CCSI, das später einen integralen Bestandteil des Company's Core Data Sheet (CCDS) bildet.
Entwicklung und Überprüfung von FDA Target Product Profile (TPP) und EU-Entwurf-SmPC (dSmPC)
Das Target Product Profile (TPP)/der Entwurf der Zusammenfassung der Merkmale des Arzneimittels (dSmPC) ist eine Form der klinischen Kennzeichnung, die den Austausch zwischen Pharmaunternehmen und Gesundheitsbehörden erleichtert. Das TPP wird während des gesamten Arzneimittelentwicklungsprozesses verwendet, von den Phasen vor und nach dem Antrag auf Zulassung eines neuen Prüfpräparats (IND) über Programme nach der Markteinführung bis hin zur Erforschung neuer Indikationen oder anderer wesentlicher Änderungen der Kennzeichnung in klinischen Studien. Pharmaunternehmen legen die Kennzeichnungskonzepte, die die Ziele des Arzneimittelentwicklungsprogramms darstellen, in Form von TPP fest. TPP enthalten eine Erklärung zur Gesamtabsicht des Arzneimittelentwicklungsprogramms und liefern Informationen über das Arzneimittel in einer bestimmten Entwicklungsphase. Als strategischer Partner im Bereich Regulatory Affairs verfügt Freyr über Fachkompetenz bei der Erstellung von TPPs für die US dSmPCs für die EU.
- Fachkräfte mit umfassendem regulatorischem Wissen in der klinischen Verpackung und Kennzeichnung
- Erfahrung in der erfolgreichen Abwicklung globaler und regionaler Arzneimittelkennzeichnung für Fortune-Pharma-Kunden in den USA, Europa, im asiatisch-pazifischen Raum, im Nahen Osten und Nordafrika usw.
- Globale regulatorische Expertise zur Unterstützung von Unternehmen der Biowissenschaften, d. h. Pharma-, Biotech- und Ernährungsherstellern
- Hochqualifizierte medizinische Redakteure mit umfassender Erfahrung in der regulatorischen Kennzeichnung
- Ein umfassendes und aktuelles Verständnis der weltweiten Änderungen bei der Arzneimittelkennzeichnung durch verschiedene Gesundheitsbehörden wie die US FDA, EMA, die TGA usw.
- Engagiertes Compliance-Team, das den Status der Implementierung von Core und Company Core Data Sheet (CDS/CCDS) in regionalen Kennzeichnungen verfolgt
- Expertise in der Kennzeichnung klinischer Studien und Dienstleistungen für die klinische Kennzeichnung
- Hocherfahrene Fachleute für die Kennzeichnung von Pharma-, Biotech- und Ernährungsprodukten









