Übersicht über das FDA eSTAR
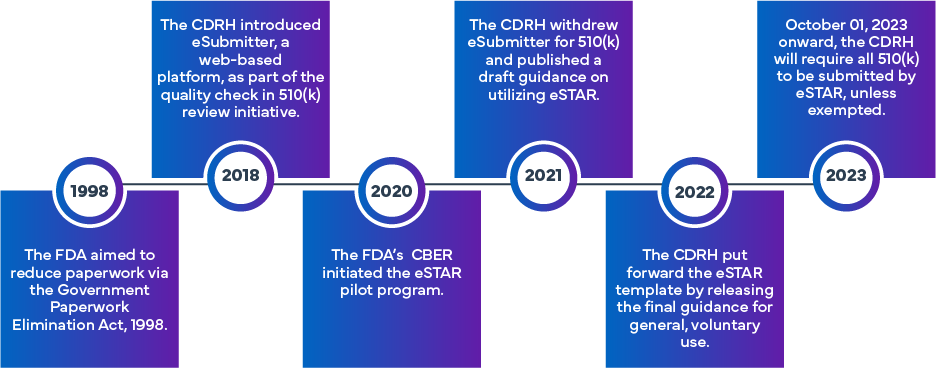
FDA FDA wurde ins Leben gerufen, um die Effizienz und Einheitlichkeit bei der Erstellung und Prüfung FDA (k) FDA , De-Novo- und PMA-Anträgen zu verbessern. Aufbauend auf dem ursprünglichen eSubmitter-Konzept, das die elektronische Einreichung von Anträgen für Medizinprodukte und In-vitro-Diagnostika vorsah, wurde das eSTAR-Programm unter Rückgriff auf die bisherigen Erfahrungen FDAeingerichtet. Die FDA ein weiteres Programm namens „Electronic Submission Template and Resource (eSTAR) Pilot Program“ FDA . 510(k)-Anträge müssen seit dem 1. Oktober 2023 über eSTAR eingereicht werden; De-Novo-Anträge (sofern nicht ausgenommen) müssen seit dem 1. Oktober 2025 über eSTAR eingereicht werden. Die Vorlagen sind online verfügbar, für den eigentlichen Einreichungsprozess sind jedoch die Zugangsdaten FDA erforderlich.
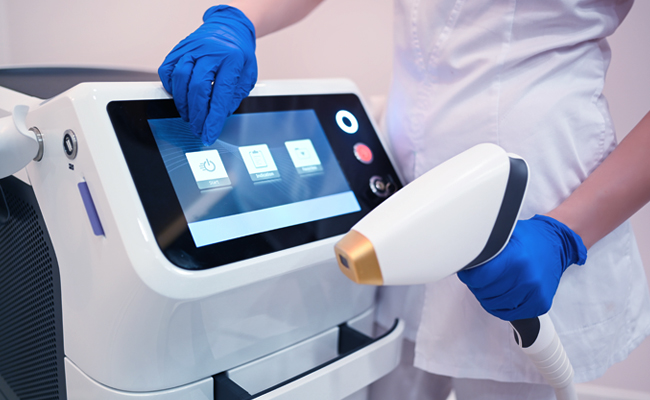
Was ist das FDA eSTAR?
eSTAR ist eine interaktive PDF-Vorlage, die entwickelt wurde, um die Erstellung eines umfassenden Zulassungsantrags für Medizinprodukte bei der FDA zu erleichtern FDA Außerdem können Antragsteller eSTAR nutzen, um Antworten auf die Aufforderungen FDAzur Einreichung zusätzlicher Informationen einzureichen. Ziel ist es, die Qualität der Anträge für verschiedene Medizinprodukte zu verbessern, indem sichergestellt wird, dass die Antragsteller vollständige und qualitativ hochwertige Daten für die Zulassungsprüfung FDAbereitstellen.
Durch die Verwendung des eSTAR-Formats können Antragsteller sicher sein, dass ihre Einreichungen vollständig sind, was es der FDA wiederum ermöglicht, die Prüfungen vor der Markteinführung effizienter FDA und einen zeitnahen Zugang zu sicheren und wirksamen Medizinprodukten FDA gewährleisten. Die eSTAR-Vorlage ist kostenlos verfügbar und kann von allen Einreichern von Medizinprodukten für 510(k)- und De-Novo-Anträge sowie freiwillig für Q-Einreichungen und ergänzende PMA-30-Tage-Meldungen an die FDA verwendet werden. Es gibt zwei Arten von eSTAR-Vorlagen – eine für Medizinprodukte und eine für IVDs. PreSTAR Beta wurde weiterentwickelt; verwenden Sie die neuesten Q-Einreichungsvorlagen über das CDRH Customer Collaboration Portal (CCP). Die eSTAR 6.0-Vorlage für Nicht-IVD-De-Novo-/510(k)-Einreichungen wurde im Oktober 2025 veröffentlicht.
Merkmale und Einschränkungen von eSTAR-Einreichungen
Obwohl das eSTAR-Programm ein interaktives PDF-Formular zur Unterstützung von Antragstellern bei der Erstellung umfassender Einreichungen für Medizinprodukte und IVD bietet, hat es sowohl Vor- als auch Nachteile. Antragsteller müssen diese Vorteile und Einschränkungen kennen, um fundierte Entscheidungen über die Integration von eSTAR in ihren Einreichungsprozess treffen zu können. In der folgenden Tabelle werden wir die Merkmale und Beschränkungen des eSTAR-Programms untersuchen.

Überlegungen für eine effektive Nutzung von eSTAR
Ein vorteilhaftes Merkmal der eSTAR-Vorlage, das zur Optimierung des Einreichungsprozesses beiträgt, ist die automatische Einbeziehung relevanter Vorschriften und anerkannter Standards zur Zitierung. Dies beschleunigt nicht nur den Einreichungsprozess durch die Reduzierung manueller Dateneingaben, sondern mindert auch die Möglichkeit menschlicher Fehler, die bei der Eingabe von Vorschriften und Standards auftreten könnten. Durch die geführte Erstellung für jeden Einreichungsabschnitt kann die Nutzung von eSTAR im Einreichungsprozess mühelos optimiert werden.
- Die FDA empfiehlt Adobe Acrobat Pro oder Foxit PDF Editor zum Bearbeiten von eSTAR-Vorlagen.
- eSTAR enthält bestimmte integrierte Formulare, wodurch die Notwendigkeit einer separaten Ausfüllung entfällt. Dazu gehören Formular 3514 (das Einreichungsdeckblatt) und Formular 3881 (Anwendungsgebiete). Zusätzlich ist die wahrheitsgemäße und genaue Erklärung, die zuvor auf dem Briefkopf eines Unternehmens erforderlich war, nun in eSTAR integriert.
- eSTAR unterstützt verschiedene Anhangsformate über PDFs hinaus, wie z. B. Excel-Tabellen und Video-(mp4)-Dateien.
- Dateien in makrofähigen und ausführbaren Formaten sind nicht zulässig.
- Die Gesamtgröße der eSTAR-PDF-Datei darf zusammen mit ihren Anhängen 1 GB nicht überschreiten, da Dateien, die größer als 4 GB sind, nicht akzeptiert werden.
- Wenn Ihre elektronischen Dateien die technischen Grenzen überschreiten, können Sie die digitale Einreichung per Post an das CDRH Document Control Center (DCC) senden.
Bewährte Methoden für die Vorbereitung von eSTAR-Einreichungen
Die Befolgung einiger bewährter Methoden für die Vorbereitung von eSTAR-Einreichungen kann Antragstellern helfen, den Einreichungsprozess zu optimieren und ihre Chancen auf ein erfolgreiches Ergebnis zu verbessern. Hier sind einige bewährte Methoden:
- Beachten Sie die FDA :Die FDA Leitlinien FDA , die Antragstellern helfen sollen, die eSTAR-Vorlage erfolgreich zu nutzen. Die Befolgung dieser Leitlinien stellt sicher, dass die Einreichungen den Anforderungen und Erwartungen FDAentsprechen.
- Vollständigkeit sicherstellen:Die eSTAR-Vorlage führt die Antragsteller durch die wesentlichen Angaben zur Einreichung. Die Antragsteller müssen alle erforderlichen Angaben machen, um das Risiko von Unvollständigkeiten oder Nachfragen nach zusätzlichen Informationen zu minimieren.
- Konsistenz wahren:Die eSTAR-Vorlage sorgt für Einheitlichkeit bei Inhalt und Struktur von 510(k)-Einreichungen. Anleitungen für die Erstellung der einzelnen Abschnitte der Einreichung erleichtern die Erfassung von Informationen zu einem Medizinprodukt.
- Klarheit hat Vorrang:Geben Sie in Ihren eSTAR-Einreichungen klare und prägnante Angaben an, um einen reibungslosen Prüfprozess zu gewährleisten. Durch diese Detailgenauigkeit und Präzision lassen sich Verzögerungen und Fehler minimieren und wird zudem ein zeitnaher Zugang zu den Einreichungen für Medizinprodukte vor der Markteinführung sichergestellt.
- Sicherheit und Genauigkeit:Die automatische Überprüfung der Angaben in jedem Abschnitt der eSTAR-Einreichungen trägt dazu bei, Verzögerungen bei der Prüfung und mögliche Mängel zu vermeiden.
Bedeutung der Farbcodierung bei der FDA eSTAR-Einreichung
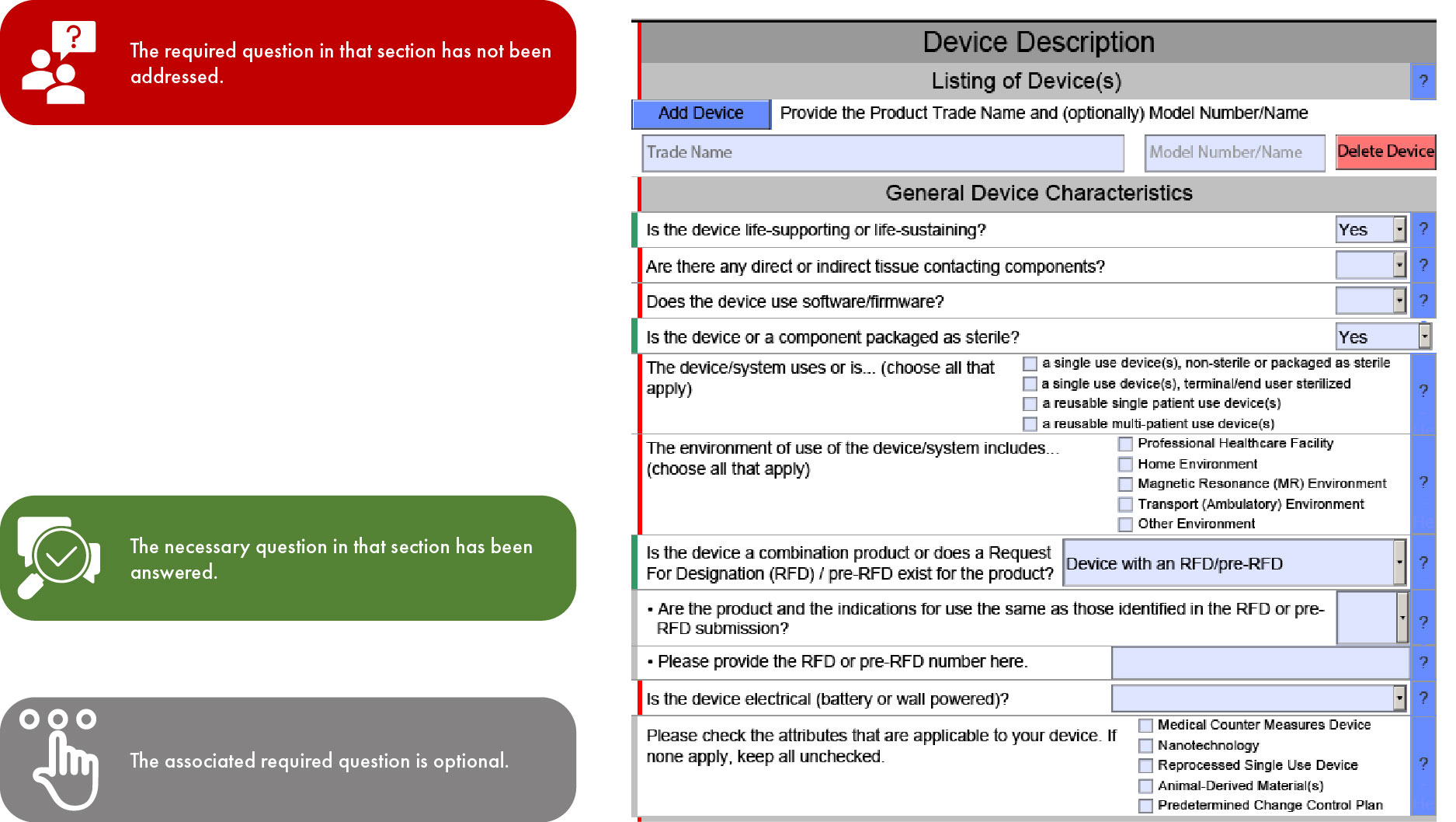
Da eSTAR ab dem 1. Oktober 2023 für 510(k)-Anträge und ab dem 1. Oktober 2025 für De-Novo-Anträge verpflichtend ist, richtet sich der Ablauf durch die einzelnen Abschnitte der Vorlage nach der Art des Antrags. Diese Art der Optimierung ermöglicht eine schnellere Prüfung durch die US FDA und minimiert somit Unstimmigkeiten und Auslassungen in Ihrem Antrag. Es ist jedoch wichtig zu beachten, dass die FDA ihre Prüfung verzögern FDA , wenn englische Übersetzungen für die eingereichten Unterlagen fehlen.

Anhänge abstimmen
Prüfen Sie die eSTAR-Vorlage im Voraus, um zu verstehen, wie Anhänge aufgeteilt sind, und stellen Sie sicher, dass Ihre Dokumente mit den Anhangsabschnitten übereinstimmen. Dieser Schritt ist entscheidend, insbesondere für Unternehmen mit früheren 510(k)-Einreichungen, da Ihr bestehender Ansatz zur Dokumentenorganisation möglicherweise Anpassungen erfordert. Dies könnte auch das Extrahieren von Inhalten aus Anhängen umfassen.
- eSTAR erfordert prägnante Anhänge, die sich von traditionellen Einreichungen unterscheiden.
- Rechnen Sie mit zahlreichen Anhängen, möglicherweise Dutzenden davon.
- Anhänge ermöglichen die Einbindung von Daten wie Excel-Tabellen, MP4-Videodateien, Word-Dokumenten, JPEG-Dateien usw.
- eSTAR fordert Seitenzahlen für Anhangsinformationen, empfiehlt jedoch nicht die Verwendung einer Checkliste für die Ablehnung der Annahme (refusal-to-accept) für FDA-Leitlinien.
Vorlagen: Es stehen die neuesten Vorlagen der Version 6.0 zur Verfügung; für laufende Einreichungen ist auch Version 5 zulässig: fda.
Die Zukunft von eSTAR
Es wird erwartet, dass eSTAR nach der Fertigstellung umfassender anwendbarer Leitliniendokumente aktualisiert wird. Mit diesen Updates kann sich der Hersteller auf die neuesten von der US FDA herausgegebenen Versionen beziehen.
Health Canada (HC) hat eine Pilotinitiative zur Nutzung von eSTAR für Geräte der Klassen III und IV eingeführt. Es wird vermutet, dass andere Nationen dem Beispiel Kanadas folgen könnten, indem sie die Einführung von eSTAR, insbesondere innerhalb des IMDRF-Konsortiums, optional gestalten. Es sollte jedoch beachtet werden, dass es diesbezüglich keine expliziten Erklärungen gegeben hat.
Warum sollten Sie sich für Freyr entscheiden?
Freyr verfügt über umfangreiche Expertise aus zahlreichen früheren Projekten im Bereich der Einreichungen bei der FDA. Durch die Bereitstellung zweier Wege zur proaktiven Unterstützung der Branche bei der Beschleunigung von 510(k)- und De-Novo-Einreichungen bietet Freyr eine Reihe von Kundendienstleistungen an. Diese umfassen eine umfassende Liste wesentlicher Einreichungsdokumente und erforderlicher Informationen, die Durchführung sorgfältiger Lückenanalysen der Dokumentation, die Zusammenstellung von Einreichungen über eSTAR und die Fertigstellung des Prä-Markt-Einreichungspakets für die FDA. Darüber hinaus unterstützt Freyr auch Aktivitäten nach der Einreichung, wie die Bereitstellung zusätzlicher Informationen und die Überprüfung von Branchenantworten auf etwaige ergänzende Informationsanfragen der FDA.
Wie kann Freyr helfen?
Freyr bietet Unterstützung, die bei der Vorbereitung von 510(k)- und De-Novo-Einreichungen hilfreich sein kann. Die Dienstleistungen umfassen:
- Unterstützung beim Zulassungsweg: Dies umfasst die Ermittlung des Produktcodes, des Namens und der Nummer der relevanten Vorschrift, potenzieller Vergleichs- oder Referenzgeräte, der erforderlichen Leistungstests sowie der geltenden Normen und Leitfäden, die für das jeweilige Gerät relevant sind.
- Q-Submission-Unterstützung (Pre-Submissions): Dies beinhaltet die Unterstützung bei der Klärung von Fragen zu den Voraussetzungen einer Prä-Markt-Einreichung, die Organisation der Einreichung, die Vorbereitung auf ein FDA-Meeting, die interaktive Zusammenarbeit mit der FDA während des Meetings und die Erstellung des Sitzungsprotokolls.
Expertise im FDA eSTAR-Programm
- Umfassende FDA-regulatorische Strategie.
- Identifizierung von Referenzprodukten.
- Nachweis der wesentlichen Gleichwertigkeit mit einem Vergleichsgerät.
- Lückenanalyse für die FDA-Konformität.
- Zusammenstellung von einundzwanzig (21) Abschnitten der 510(k)-technischen Akte.
- Veröffentlichung und Erstellung der eCopy.
- Validierung und Einreichung der eCopy.
- Dienstleistungen zur Kontaktpflege für die Zulassung von Medizinprodukten.
- Bearbeitung von RTA-Antworten und Mängeln.
- Beratungsdienstleistungen zur Behebung von Mängeln.
- Geräteregistrierung und Pflege der FURLS-Datenbank.