Übersicht zur Registrierung von Medizinprodukten bei Health Canada
Kanada verfügt mit seinen strengen Richtlinien über eines der besten Regulierungssysteme der Welt für Medizinprodukte. In Kanada werden alle Medizinprodukte von Health Canada, dem Health Products and Food Branch, dem Therapeutic Products Directorate, Medical Devices Bureau, reguliert. Health Canada prüft Medizinprodukte, um deren Sicherheit, Wirksamkeit und Qualität zu bewerten, bevor sie gemäß der 1998 eingeführten kanadischen Medizinprodukteverordnung SOR/98-282 für den Verkauf in Kanada zugelassen werden. Freyr ist ein aktiver Partner von Medizinprodukteunternehmen, um sie bei der Einhaltung der Registrierungsrichtlinien für Medizinprodukte von Health Canada zu unterstützen.
Aufsichtsbehörde: Health Canada
Verordnung: Medizinprodukte-Verordnungen (SOR/98-282)
Bevollmächtigter Vertreter: Nicht erforderlich
QMS-Anforderung: ISO 13485:2016 Konformität als Medical Device Single Audit Program (MDSAP)
Bewertung technischer Daten: Health Canada
Gültigkeit der Lizenz: Unbegrenzt
Kennzeichnungspflichten: Teil 21 der MDR (SOR/98-282)
Einreichungsformat: Papier
Sprache: Englisch & Französisch
Health Canada Medizinprodukt-Klassifizierung
Das Klassifizierungssystem für Medizinprodukte von Health Canada lehnt sich stark an die Richtlinie 93/42/EWG des Rates der Europäischen Union an. Viele der Regeln und Begriffsdefinitionen ähneln denen, die von der Europäischen Union vorgeschlagen wurden. Es ist jedoch nicht zwangsläufig der Fall, dass ein Medizinprodukt, das nach dem Klassifizierungssystem der Europäischen Union in einer bestimmten Klasse eingestuft ist, auch nach dem kanadischen Klassifizierungssystem für Medizinprodukte in derselben Klasse eingestuft wird. Antragsteller müssen die in den Vorschriften festgelegten Regeln befolgen, um die passende Klassifizierung für ihr Produkt in Kanada zu bestimmen.
Die folgenden Risikofaktoren eines bestimmten Produkts wurden zur Erstellung der kanadischen Klassifizierungsregeln herangezogen: Invasionsgrad, Kontaktdauer, betroffenes Körpersystem sowie lokale im Vergleich zu systemischen Effekten.
| Geräteklasse | Risiko |
|---|---|
| I | Niedrig |
| II | Gering bis mittel |
| III | Mittel-Hoch |
| IV | Hoch |
Bevollmächtigter Vertreter in Kanada
Es gibt keine Vorschrift, dass der Hersteller einen Bevollmächtigten in Kanada benennen muss. Der Händler muss jedoch die Anforderungen von Health Canada für gute Vertriebspraktiken (GDP) einhalten.
Registrierung von Medizinprodukten – Kanada
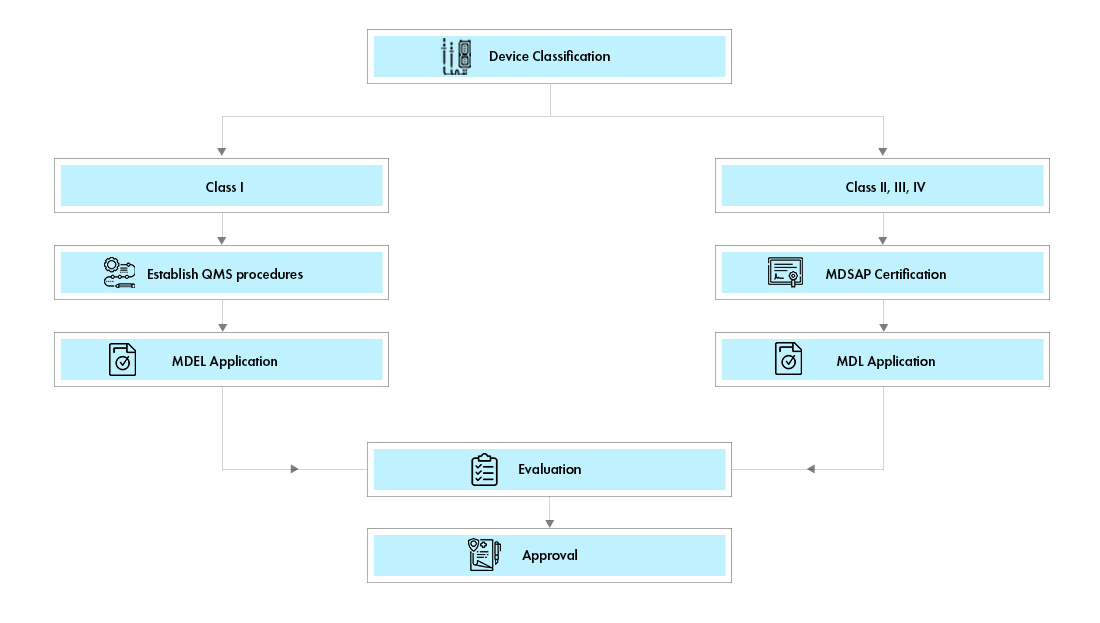
Es gibt zwei Wege für die Registrierung von Medizinprodukten in Kanada:
Zulassung für Medizinprodukte-Betriebsstätten (MDEL): Produkte der Klasse I können eine Zulassung für Medizinprodukte-Betriebsstätten (MDEL) in Kanada beantragen, indem sie die vorgeschriebenen Verfahren vorbereiten und die Gebühren von Health Canada entrichten.
Medizinproduktlizenz (MDL): Produkte der Klassen II, III und IV müssen eine kanadische Medizinproduktlizenz (MDL) beantragen. Die Dokumentenanforderungen variieren je nach Produktklasse.
Prozessablauf
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End-Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel:
- Änderungsmanagement nach der Zulassung – Änderungen an bestehenden Medizinprodukte-Zulassungen, wie z.B. die Hinzufügung neuer Varianten, Zubehörteile; die Hinzufügung neuer Anwendungsgebiete und Ähnliches
- Aufrechterhaltung von Genehmigungen und Registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren
- Verlängerung von Lizenzen
- Koordination zwischen Health Canada und dem Hersteller
Zusammenfassung
| Risiko | Geräteklasse | QMS-Audit | Regulatorischer Weg | Dokumentenanforderungen | Health Canada Zeitpläne |
|---|---|---|---|---|---|
| Niedrig | I | N/A | MDEL |
| N/A |
| Gering bis mittel | II | MDSAP-Zertifikat | MDL |
| 15 Tage |
| Mittel-Hoch | III | MDSAP-Zertifikat | MDL |
| 60 Tage |
| Hoch | IV | MDSAP-Zertifikat | MDL |
| 75 Tage |
Dienstleistungen von Freyr zur Registrierung von Medizinprodukten
Freyr Expertise
- Health Canada Klassifizierungs- und Gruppierungsdienstleistungen für Medizinprodukte
- Registrierung von Medizinprodukten, Kanada
- Voranmeldungsgespräche mit Health Canada
- MDSAP, Kanada
- Identifizierung/Qualifizierung von Distributoren zur Einhaltung der Anforderungen von Health Canada
- Betriebslizenz für Medizinprodukte Kanada (MDEL)
- Lizenzierung von Medizinprodukten in Kanada (MDL)
- Änderungsmanagement nach der Zulassung
- Kennzeichnungsdienstleistungen gemäß den Kennzeichnungsanforderungen von Health Canada für Medizinprodukte