Entwicklung von Generika – Übersicht
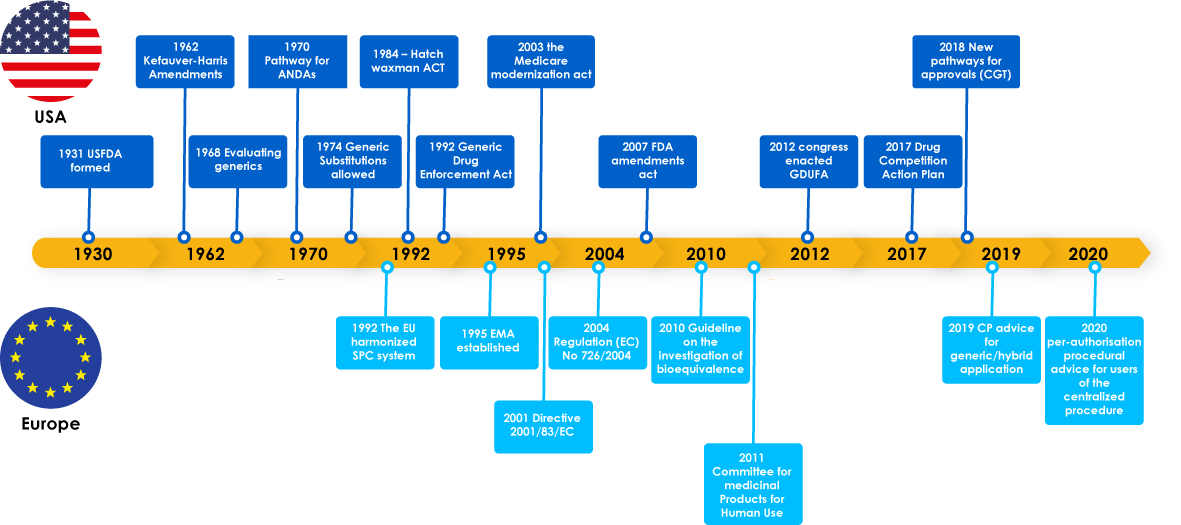
Generika haben wichtige Meilensteine erreicht, darunter regulatorische Gesetze zur Unterstützung der Generikaentwicklung, die Hersteller ermutigten, den Generikamarkt zu erschließen. Diese Gesetzgebungen gaben den Ärzten auch die Sicherheit, einen Ersatz für ein Markenmedikament zu verschreiben, und kamen letztendlich den Patienten zugute, da Generikahersteller die kritischen Bedürfnisse von Patienten weltweit erfüllten.
FAQs zu Generika
F1: Was sind Generika?
Antw: Generika sind pharmazeutische Arzneimittel, die identische Kopien des Originalarzneimittels sind und denselben API (Wirkstoff), dieselbe Dosierung, denselben Verwendungszweck, dieselben Nebenwirkungen, denselben Verabreichungsweg, dieselben Risiken, dieselbe Sicherheit und dieselbe Stärke wie das Innovatorarzneimittel aufweisen, können sich jedoch in einigen Merkmalen wie dem Herstellungsprozess, der Formulierung, den Hilfsstoffen, der Farbe, dem Geschmack und der Verpackung unterscheiden. Mit anderen Worten, ein Generikum ist therapeutisch gleichwertig mit einem Markenmedikament und kann daher durch sein Markenäquivalent ersetzt werden.
F2: Warum kosten Generika weniger als ein Innovatorarzneimittel?
Antw: Generika sind im Vergleich zum Innovatorarzneimittel kostengünstiger, da Generika die kostspieligen und langwierigen präklinischen und klinischen Studien nicht wiederholen müssen, die für Innovatorarzneimittel erforderlich sind, um Sicherheit und Wirksamkeit nachzuweisen, und stattdessen nur die pharmazeutische Äquivalenz für ihr Produkt nachweisen müssen.
F3: Sind Generika genauso gut wie Innovatorarzneimittel?
Antwort: Ja, Generika haben die gleiche Qualität, Wirksamkeit und Sicherheit wie Markenmedikamente. Der niedrigere Preis dieser Medikamente bedeutet nicht, dass sie von minderer Qualität sind. Denn Generika müssen, genau wie Markenmedikamente, ein strenges Zulassungsverfahren durchlaufen, um ihr Arzneimittelprodukt auf den Markt zu bringen. Pharmaunternehmen müssen den Antrag für Generika einreichen und dabei nachweisen, dass ihr Arzneimittelprodukt den gleichen klinischen Nutzen wie die Markenmedikamente hat und als Ersatz für das jeweilige Markenmedikament geeignet ist.
F4: Warum sehen Generika anders aus als das Markenarzneimittel?
Antwort: Generika müssen bioäquivalent zu Markenarzneimitteln sein und den gleichen Wirkstoff wie Innovator-Medikamente enthalten. Es kann jedoch geringfügige Unterschiede bei Generika hinsichtlich Form, Kennzeichnung (geringfügige Abweichungen), Verpackung und inaktiven Inhaltsstoffen wie Farbe, Aromen und Konservierungsstoffen geben; die Wirksamkeit des Medikaments muss jedoch gleich bleiben.
Q5: Was gehört zur Prüfung und Genehmigung von Anträgen für Generika in den US?
Antwort: Jedes Pharmaunternehmen, das sein Generikum in den US vermarkten möchte, sollte alle regulatorischen Anforderungen der US FDA für die Einreichung von Generika erfüllen und muss Folgendes nachweisen:
- Das Generikum ist dem Markenprodukt „pharmazeutisch/therapeutisch äquivalent“
- Der Hersteller ist in der Lage, das Medikament korrekt und konsistent herzustellen
- Der „Wirkstoff“ ist derselbe wie der des Markenprodukts
- Die richtige Menge des Wirkstoffs gelangt an die Stelle im Körper, wo sie ihre Wirkung entfaltet
- Die „inaktiven“ Inhaltsstoffe des Medikaments sind sicher
- Das Medikament zersetzt sich im Laufe der Zeit nicht
- Der Behälter, in dem das Medikament versendet und verkauft wird, ist geeignet
- Das Etikett ist dasselbe wie das des Markenmedikaments
- Relevante Patente oder rechtliche Exklusivrechte sind abgelaufen
F6: Hat jedes Markenmedikament ein Generikum?
Antwort: Nein. Nicht jedes Markenmedikament hat eine Generika-Version. Neue Medikamente werden bis zu zwanzig (20) Jahre lang unter Patentschutz hergestellt. Das bedeutet, dass während dieser Zeit kein anderes Medikament hergestellt und vermarktet werden darf, bis das Patent abläuft. Einige Medikamente erhalten jedoch möglicherweise nie Generika-Versionen, entweder aufgrund von Herstellungsschwierigkeiten oder weil das Generikum als unrentabel angesehen werden könnte.








