Übersicht der EU-IVDR-Konformitätsdienstleistungen
Die europäische Verordnung über In-vitro-Diagnostika (EU IVDR) ist eine neue regulatorische Grundlage für das Inverkehrbringen von IVD auf dem europäischen Markt. Die EU IVDR-Verordnung wird die derzeitige EU-Richtlinie über In-vitro-Diagnostika (EU 98/79/EG) ersetzen. Als europäische Verordnung wird sie in allen EU Member States und den Staaten der Europäischen Freihandelsassoziation (EFTA) wirksam sein, ohne dass sie in das nationale Recht der jeweiligen Staaten überführt werden muss. Als bewährter regulatorischer Partner bietet Freyr Herstellern EU IVDR-Konformitätsdienstleistungen und IVDR-Beratungsdienstleistungen für konforme In-vitro-Diagnostika-Vorschriften und die CE-Kennzeichnung an.
Die IVDR-Verordnung – Übergangszeitplan
Die neue EU-IVDR, die ab dem 26. Mai 2022 in Kraft treten soll, gilt als eine wesentliche Änderung der regulatorischen Überwachung von IVDs. Eine Übersicht über den IVDR-Übergang finden Sie unten –
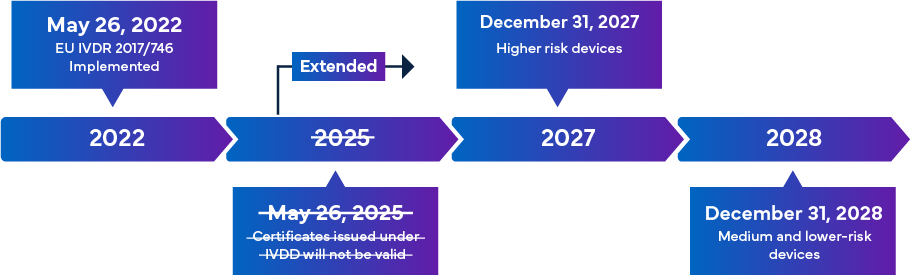
Nach vollständiger Umsetzung stellen die IVDR-Konformitätsregeln sicher, dass fast alle IVDs, die auf den europäischen Markt gelangen, einer Prüfung durch eine benannte Stelle (NB) gemäß IVDR und einer CE-Kennzeichnungszertifizierung im Rahmen des IVD-Zulassungsverfahrens unterliegen. In diesem Szenario müssen Hersteller, neben der Anpassung an die aktualisierte IVDR-Klassifizierung, umgehend die wesentlichen technischen Dokumentationen für eine erfolgreiche IVD-Registrierung und CE-Kennzeichnung effektiv überprüfen. Die IVDR-Anforderungen variieren je nach Risikoklasse des IVD. Im Allgemeinen müssen Hersteller für die IVD-Zertifizierung Folgendes durchführen:
- Überprüfung der technischen Dokumentation gemäß der IVDR-Verordnung (Verordnung (EU) 2017/746)
- Erstellung des Leistungsbewertungsberichts (Performance Evaluation Report, PER) für alle IVDs
- Leistungsüberwachung nach dem Inverkehrbringen (Post-market Performance Follow-up, PMPF) gemäß Anhang XIII Teil B der IVDR
- Vigilanz-Meldepflichten gemäß Artikel 82 der IVDR
Freyr unterstützt Kunden bei der Durchführung einer systematischen Überprüfung der wissenschaftlichen Literatur und hilft bei der Planung und Erstellung eines PER zur Einhaltung der In-vitro-Diagnostika-Verordnung. Freyr verfügt über engagierte Experten, die IVDR-Beratungsdienste und Unterstützung bei der Post-Market Surveillance (PMS) anbieten, die zusammen mit der Post-Market Performance Follow-up (PMPF) ein integraler Bestandteil des Qualitätsmanagementsystems des Herstellers ist.
Erhalten Sie fachkundige Beratung zur Einhaltung der EU-IVDR
EU-IVDR-Konformitätsdienstleistungen: Fachwissen und Vorteile
- Übergangsplan für die IVDR-Konformität
- Technische Überprüfung und Lückenanalyse der IVDR-Anforderungen für die GSPR (Allgemeine Sicherheits- und Leistungsanforderungen)
- Unterstützung bei der Erstellung der technischen Dokumentation gemäß den IVDR-Anforderungen
- Berichte zur wissenschaftlichen Validität basierend auf Literatur und/oder internen Daten
- Berichte zur klinischen Leistung basierend auf Literatur und/oder internen Daten
- Berichte zur klinischen Evidenz oder Leistungsbewertung
- Protokolle und Berichte zur Leistungsüberwachung nach dem Inverkehrbringen (PMPF)
- Post-market Surveillance (PMS)-Protokolle und -Berichte
- Erstellung/Überarbeitung weiterer Dokumente wie Packungsbeilagen/Gebrauchsanweisungen (IFU), Kurzanleitungen (QRI), Bedienungs-/Benutzerhandbücher usw.

- Gesicherte IVDR-Konformität, IVD-Registrierung und CE-Kennzeichnung
- Umfassendes regulatorisches Verständnis und Fachwissen in den wichtigsten Wirkungsbereichen der EU-IVDR
- Ein starkes, projektmanagementgesteuertes Liefermodell zur Gewährleistung der Termintreue
- Interne NB-Experten (Überprüfung des Berichts durch interaktive Prüfer der Benannten Stelle)
- Fokussierte Teams mit übergreifender Expertise in spezifischen Wirkungsbereichen und Geräteklassen
- Funktionsübergreifende Beiträge von Medizinprodukteexperten zur Einhaltung der Anforderungen
- Umfassendes Dienstleistungsspektrum in den Bereichen Konformität, Überprüfung und Planung
- Umfassendes Fachwissen bei der Sicherstellung der Konsistenz von Ergebnissen (Zeit und Qualität)









