Der nordamerikanische Markt für Medizinprodukte ist einer der attraktivsten und am stärksten regulierten Märkte weltweit. In den Vereinigten Staaten wird die Zulassung von Medizinprodukten von der FDA überwacht, vor allem durch das Center for Devices and Radiological Health (CDRH), während sie in Kanada von Health Canada im Rahmen eines risikobasierten Regelwerks geregelt wird.
Für Hersteller kann die Erschließung dieser Märkte komplex sein. Beide Länder stützen sich auf eine risikobasierte Klassifizierung von Medizinprodukten (Klasse I, II, III und in Kanada Klasse IV), die durch fundierte Nachweise hinsichtlich Sicherheit und Leistung sowie ein konformes Qualitätsmanagementsystem (QMS) untermauert wird. Programme wie MDSAP Normen wie ISO 13485 sowie unterschiedliche Terminologie, Zulassungsverfahren und Anforderungen an die Dokumentation erhöhen die Komplexität bei der Planung des Markteintritts in den US Kanada zusätzlich.
Freyr unterstützt Hersteller dabei, diese Komplexität in einen klaren, umsetzbaren Plan für den Marktzugang US Kanada umzuwandeln. Wir wissen, wie sich FDA und die Vorschriften von Health Canada für Medizinprodukte überschneiden, und helfen Ihnen dabei, Klassifizierungen, Nachweise, Qualitätsmanagementsysteme und Unterlagen aufeinander abzustimmen, damit Sie in beiden Ländern eine einheitliche, effiziente Strategie für Zulassungen, Markteinführungen und die langfristige Einhaltung der Vorschriften verfolgen können.
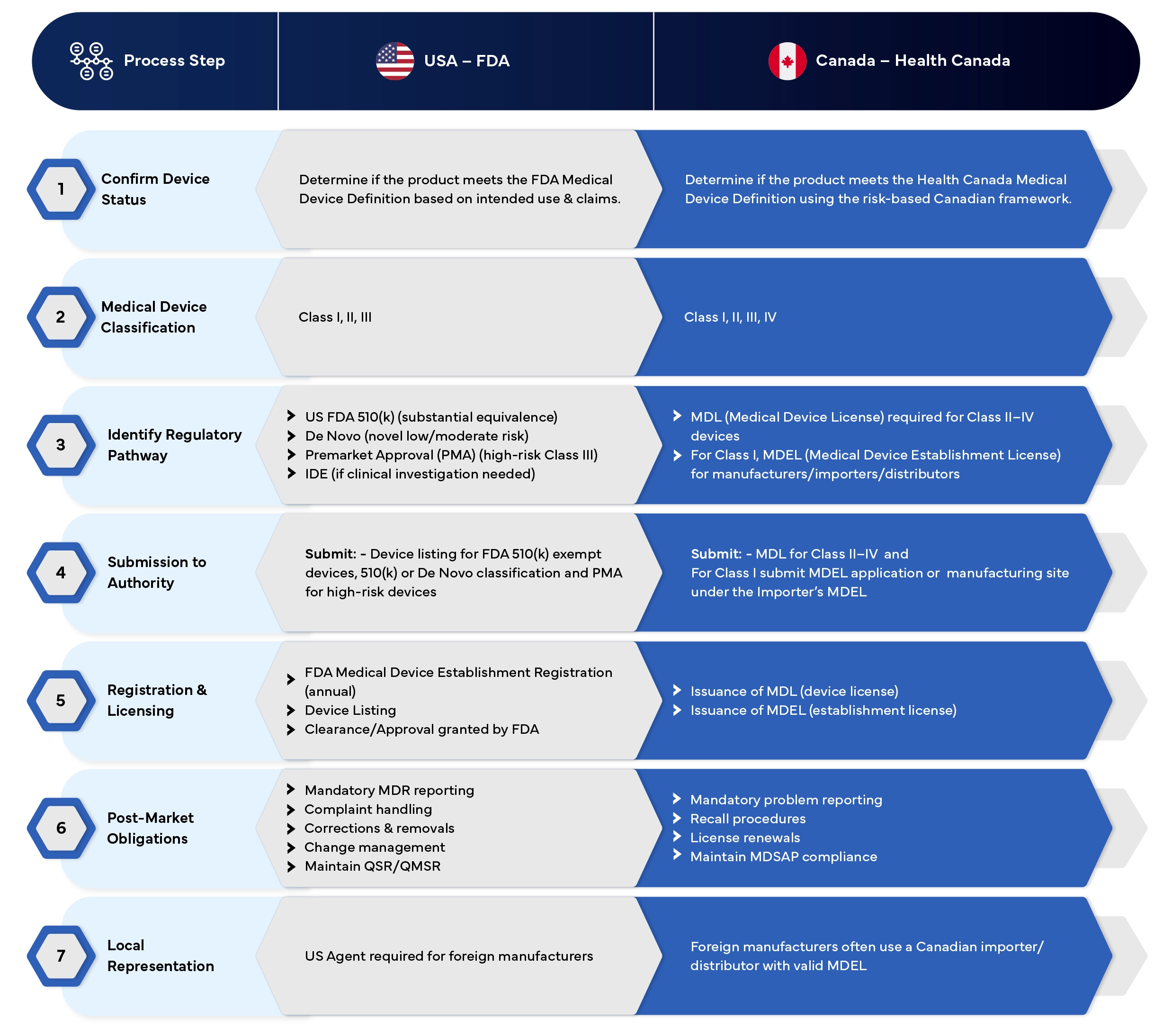
USA gegen Kanada
Verfahren zur Registrierung von Medizinprodukten – Vergleichstabelle
Freyrs Dienstleistungen zur Registrierung von Medizinprodukten
Registrierung von Medizinprodukten in Nord- und Südamerika.
- Unterstützung bei regulatorischen und Marktanalysen
- Produktklassifizierung gemäß den regulatorischen Anforderungen
- Registrierung von Medizinprodukten US -513 (G) & (Wahl des passenden Zulassungswegs unter 510 (K)/De-NOVO/PMA/IDE)
- Vorgespräch zur Einreichung mit Gesundheitsbehörden
- Regulatorische Unterstützung für Produktdokumente wie das Design History File (DHF)
- Lückenanalyse der technischen Dokumente und Good Manufacturing Practice (GMP)-Systeme
- Regulatorische Unterstützung für die Erstellung der Technischen Dokumentation gemäß dem jeweiligen Registrierungsweg
- USFDA-Strategie zur Einhaltung der Qualitätsanforderungen (21 CFR 820)
- MDSAP (Medical Device Single Audit Program)-Konformitätsdienstleistungen
- Registrierung von Medizinprodukten in Kanada – Medizinproduktelizenz (MDL) und Registrierung der Betriebserlaubnis für Medizinprodukte (MDEL)
- Kontaktpflege und Unterstützung bei Gesundheitsbehörden
- Vertretung im Land – US-Agent und Dienstleistungen der hygienisch verantwortlichen Person
- Compliance-Aktivitäten nach der Zulassung

- Erfolgreiche Einreichungen für verschiedene Geräteklassen, von Software bis hin zu Nahtmaterial
- Zugang zu lokalen Niederlassungen, um den behördlichen und sprachspezifischen Anforderungen gerecht zu werden
- Engagiertes und erfahrenes Personal für die regulatorische Unterstützung von Medizinprodukten und IVD
- Kosteneffizientes Modell für die Unterstützung bei der Inlands- oder Rechtsvertretung
- Erfolgreiche Umsetzung verschiedener Projekte in den US und Kanada
- Hauptsitz in den US.

Warum mit Freyr zusammenarbeiten?
- End-to-end Fachkompetenz in Bezug auf die End-to-end Vorschriften, die alle Bereiche abdeckt – von der Vorabmeldung (Einreichung von Anträgen) bei FDA Health Canada bis hin zur Überwachung nach der Markteinführung und der Einhaltung der Vorschriften während des gesamten Produktlebenszyklus.
- Nachweisliche Erfolge bei über 1500 weltweiten Zulassungen für Medizinprodukte, darunter Produkte der Klassen I bis III in den US der Klassen I bis IV in Kanada.
- Präsenz vor Ort durch US und Unterstützung bei der Einhaltung kanadischer Vorschriften, unterstützt durch weltweit verteilte Expertenteams für eine reibungslose Umsetzung.
- Eine integrierte Strategie US Kanada, die Anforderungen an Nachweise, Dokumentation und Qualität vereinheitlicht, um Kosten, Doppelarbeit und Genehmigungsfristen zu reduzieren.
- Direkter Austausch mit FDA Health Canada, um eine klare Kommunikation, zeitnahe Antworten und eine proaktive Ausrichtung auf die behördlichen Anforderungen sicherzustellen.
- Über 470 Medizinproduktehersteller weltweit – von Start-ups bis hin zu globalen Konzernen – vertrauen auf uns als ihren langfristigen Partner für Zulassungsangelegenheiten in Nordamerika.












