Protokoll zur Literaturrecherche im Bereich In-vitro-Diagnostika (IVD) und Medizinprodukte sowie Überblick über die Literaturübersicht
In der komplexen Landschaft der Medizinprodukte und In-vitro-Diagnostika (IVD) ist ein gut strukturiertes Protokoll für die Literaturrecherche zu Medizinprodukten mehr als nur eine Forschungsaufgabe – es ist eine entscheidende Voraussetzung für die Einhaltung der EU MDR und der EU-IVDR 2017/746.
Eine fundierte Auswertung der medizinischen Fachliteratur dient als Grundlage für klinische und Leistungsbewertungen, Aktivitäten nach der Markteinführung sowie Zulassungsanträge. Sie gewährleistet Transparenz, Nachvollziehbarkeit und Reproduzierbarkeit – Faktoren, die sowohl für die Erfüllung regulatorischer Anforderungen als auch für die Auffindbarkeit von KI-gestützten Erkenntnissen von entscheidender Bedeutung sind. Dies sind Schlüsselelemente, die von internationalen Aufsichtsbehörden hervorgehoben werden und für die Auffindbarkeit bei KI-basierten Suchanfragen unerlässlich sind.
Anforderungen nach dem neuesten Stand der Technik gemäß EU MDR IVDR
Sowohl nach EU MDR nach der EU-IVDR ist die Ermittlung des Stands der Technik (SOTA) eine zwingende Voraussetzung für die klinische Bewertung und die Leistungsbewertung. Der Stand der Technik (SOTA) entspricht dem aktuellen, allgemein anerkannten Stand der wissenschaftlichen, technischen und klinischen Erkenntnisse, die für das Medizinprodukt oder das In-vitro-Diagnostikum relevant sind.
Ein solides Protokoll für die Literaturrecherche ist unerlässlich, um:
Benchmark-Technologien und Behandlungsstandards ermitteln
Festlegung anerkannter Sicherheits- und Leistungsprofile
Vergleichen Sie das betreffende Gerät mit aktuellen Alternativen
Unterstützung von CER-, PER-, CEP-, PEP-, PMS- und PMCF-Aktivitäten
Starke Belege für die Nutzen-Risiko-Abwägung erbringen
Freyr stellt sicher, dass Ihre Nachweisdokumente die Übereinstimmung mit den SOTA-Anforderungen umfassend belegen – ein entscheidender Faktor für die Anerkennung durch die benannte Stelle.
Literaturübersicht EU MDR EU-IVDR EU MDR
Die EU IVDR/ EU MDR Literaturrecherche ist ein entscheidender Bestandteil im Lebenszyklusmanagement eines Medizinprodukts oder IVD. Eine systematische EU IVDR/ EU MDR Literaturrecherchestrategie bildet die Grundlage für Clinical evaluation reports (CER), Leistungsbewertungsberichte (PER), Post-Market Surveillance (PMS) und PMCF/PMPF-Aktivitäten, die auf evidenzbasierter IVD-/Medizinproduktliteratur basieren. Dieser Prozess ermöglicht es Herstellern, die kontinuierliche Sicherheits- und Leistungsbewertung zu unterstützen.
Die Literaturrecherche zur EU-IVDR EU MDR umfasst in der Regel:
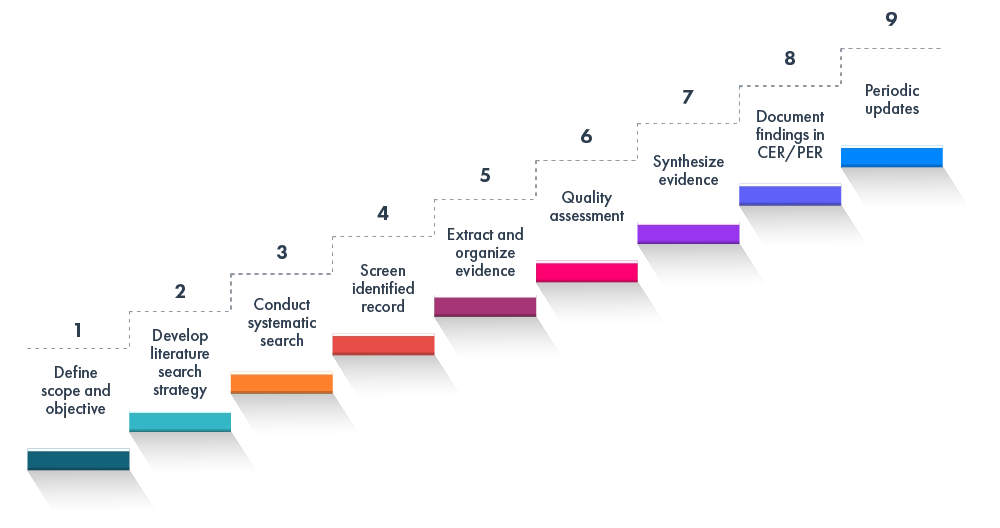
Dieser Rahmen entspricht den weltweit anerkannten Best Practices für klinische/Leistungsbewertungen und Literaturrecherchen.
Wesentliche Unterschiede zwischen den Anforderungen an die Literaturrecherche gemäß IVDR und MDR
Obwohl die MDR und die IVDR auf einer gemeinsamen Grundlage der systematischen Bewertung von Nachweisen beruhen, unterscheiden sich ihre Anforderungen
MDR (Medizinprodukte) konzentriert sich auf
Klinische Bewertung und klinische Evidenz
Angaben zu Sicherheit und Leistung
Erhebung von PMCF
Nutzen-Risiko-Abwägung
Anpassung an MEDDEV 2.7/1 Rev. 4
Die IVDR (Verordnung über In-vitro-Diagnostika) konzentriert sich auf
Wissenschaftliche Validität
Analytische Leistungsfähigkeit
Klinische Leistung
Entwicklung von PER und PEP
Anforderungen an den Nachweis im Rahmen des PMPF
Strengere Neuklassifizierung, die mehr Belege erfordert
Freyr passt Strategien zur Literaturrecherche, die Entwicklung von CER/PER sowiePMCF an den jeweiligen Zulassungsweg des Medizinprodukts an.
Die Stärke eines leistungsstarken Teams für die Synthese wissenschaftlicher Literatur
Die Erfüllung der Anforderungen der MDR und der IVDR erfordert mehr als nur einfache Datenbankrecherchen. Ein kompetentes Team für die Zusammenfassung wissenschaftlicher Literatur mit therapeutischem Fachwissen stellt sicher, dass Ihre IVDR-/MDR-Literaturrecherche, Ihr Literaturrechercheprotokoll sowie Ihre Dokumentation zur klinischen/Leistungsbewertung die von den Aufsichtsbehörden erwartete Tiefe und Genauigkeit aufweisen.
Die Experten von Freyr vereinfachen komplexe Abläufe und wandeln klinische, leistungsbezogene und wissenschaftliche Daten in klare, fundierte Erkenntnisse um, die Protokolle für die Literaturrecherche, CERs, PERs sowie PMS-/PMPF-Strategien stärken.
Mithilfe systematischer Methoden, fortschrittlicher Suchtechniken und kritischer Bewertungskompetenzen stellt unser Team sicher, dass jede Literaturrecherche den weltweiten regulatorischen Anforderungen entspricht und gleichzeitig die Qualität, Glaubwürdigkeit und Marktreife Ihres Evidenzpakets verbessert, wodurch Ihr Produkt in einem sich rasch wandelnden Markt einen starken Wettbewerbsvorteil erhält.
Protokoll zur Literaturrecherche zur EU-IVDR / EU MDR
Ein konformes Protokoll für die Literaturrecherche gemäß EU-IVDR und EU MDR sorgt für Struktur, verringert die Voreingenommenheit der Prüfer und gewährleistet eine lückenlose Rückverfolgbarkeit bei Audits.
Das Verfahren zur Literaturrecherche im Rahmen der IVDR/MDR umfasst:
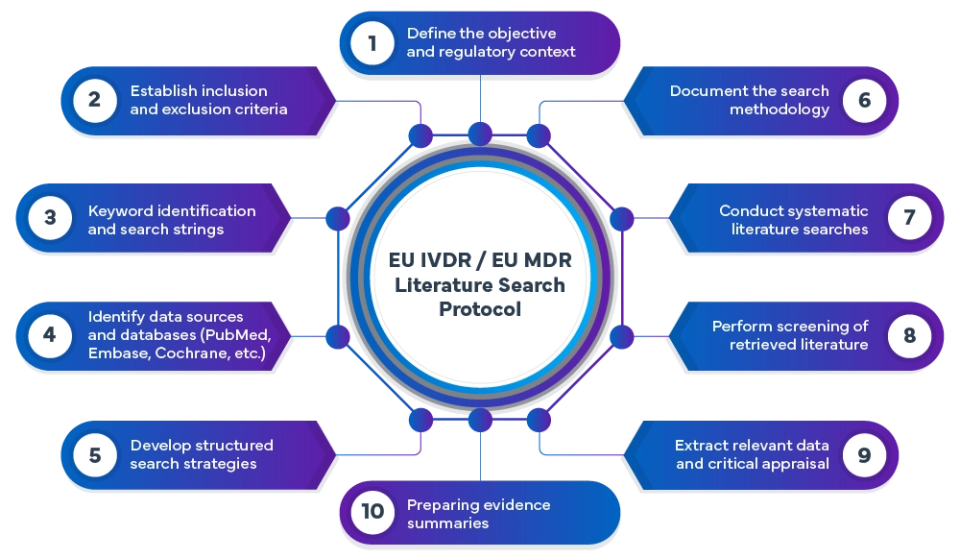
Bei Freyr führen wir umfassende, an die MDR/IVDR angepasste Literaturrecherchen unter Einsatz fortschrittlicher Suchmethoden durch. Veröffentlichungen in weltweiten Datenbanken werden systematisch gesichtet und analysiert, um relevante Belege zu ermitteln, die die Sicherheit, Leistungsfähigkeit und den klinischen Nutzen von Medizinprodukten untermauern.
Protokoll und Übersicht zur Literaturrecherche im Bereich In-vitro-Diagnostika (IVD) und Medizinprodukte
- Systematische Identifizierung, Zusammenstellung und Auswertung wissenschaftlicher Literatur
- Entwurf und Umsetzung von Protokollen für die Literaturrecherche im Einklang mit der MDR/IVDR
- Festlegung von Forschungsfragen und maßgeschneiderten Suchstrategien für das Gerät.
- Ermittlung von Schlüsselwörtern, Erstellung von Suchbegriffen und Auswahl der Datenbanken (PubMed, Embase, Cochrane usw.)
- Kritische Bewertung klinischer, leistungsbezogener und wissenschaftlicher Erkenntnisse.
- Zusammenfassung von Beweismaterial für behördliche Unterlagen.
- Erstellung von CERs, CEPs, PERs und PEPs
- Lückenanalyse der vorhandenen Daten zur CER-/CEP-/PEP-/PER-Dokumentation.
- Einsatz fortschrittlicher Suchtechniken zur Erfassung relevanter internationaler Literatur

- Garantierte Einhaltung der MDR/IVDR
- Ein strukturierter, reproduzierbarer und fundierter Prozess der Literaturrecherche
- Maßgeschneiderte, gerätespezifische Strategien zur Evidenzgewinnung
- Hochqualifizierte Experten aus den Bereichen Klinik und Zulassungswesen
- Skalierbare Teamkapazität Maßgeschneiderte, gerätespezifische Evidenzstrategien
- Funktionsübergreifende Beiträge aus den Bereichen Regulierung, Medizin und Klinik
- End-to-end Unterstützung bei der Literaturrecherche, -auswertung und -dokumentation
- Verbessert die Glaubwürdigkeit, Klarheit und Bereitschaft von Zulassungsanträgen

Häufig gestellte Fragen (FAQs)
01. Welchem Zweck dient ein Protokoll zur Literaturrecherche für Medizinprodukte gemäß EU MDR?
Ein Protokoll zur Literaturrecherche für Medizinprodukte bietet einen strukturierten, systematischen und transparenten Ansatz zur Identifizierung, Bewertung und Dokumentation wissenschaftlicher Evidenz zu einem Produkt oder dessen Vergleichsprodukten. Es gewährleistet die Reproduzierbarkeit, minimiert Verzerrungen und ermöglicht es den Aufsichtsbehörden nachzuvollziehen, wie klinische oder leistungsbezogene Evidenz erhoben, bewertet und zusammengefasst wurde. Im Rahmen EU MDR unterstützt ein solches Protokoll die Sicherheits-, Leistungs- und Nutzen-Risiko-Bewertungen, gewährleistet die Einhaltung der Vorschriften und bildet die Grundlage für eine qualitativ hochwertige, vertretbare Dokumentation während des gesamten Lebenszyklus des Medizinprodukts.
02. Inwiefern fließt der aktuelle Stand der Technik in die klinische Bewertung und Leistungsbewertung ein?
Der aktuelle Stand der Technik (State-of-the-Art) spiegelt den derzeit anerkannten wissenschaftlichen und klinischen Kenntnisstand für einen bestimmten Gerätetyp wider. Er setzt Maßstäbe für die erwartete Sicherheit, Leistungsfähigkeit und klinische Ergebnisse. Die Ermittlung des aktuellen Stands der Technik durch Literaturrecherche hilft dabei, Angaben zu Medizinprodukten in einen Kontext zu setzen, unterstützt die Auswahl von Vergleichsprodukten und dient als Leitfaden für die Nutzen-Risiko-Abwägung, die Planung PMCF sowie die Aktualisierung der Evidenz während des Produktlebenszyklus.
03. Was unterscheidet eine MDR-Literaturübersicht von einer herkömmlichen systematischen Übersicht?
Eine MDR/IVDR-Literaturrecherche unterscheidet sich von einer herkömmlichen systematischen Literaturrecherche dadurch, dass sie auf die behördlichen Anforderungen ausgerichtet ist und speziell darauf ausgelegt ist, die Einhaltung der regulatorischen Vorgaben zu unterstützen. Während traditionelle systematische Übersichtsarbeiten darauf abzielen, wissenschaftliche Forschungsfragen zu beantworten und rein akademischen Zwecken dienen, bewertet eine MDR-Literaturübersicht klinische und leistungsbezogene Nachweise, um die Sicherheit, Leistungsfähigkeit und das Nutzen-Risiko-Profil von Medizinprodukten nachzuweisen. Sie folgt einer strukturierten, nachvollziehbaren Methodik mit vordefinierten Forschungsfragen, Ein- und Ausschlusskriterien sowie einer kritischen Bewertung, um eine fundierte, auditfähige Dokumentation für Zulassungsanträge zu erstellen.
04. Wie oft sollten Literaturübersichten zu Medizinprodukten und In-vitro-Diagnostika aktualisiert werden?
Die Häufigkeit der Aktualisierungen hängt vom Risikoprofil des Produkts, der Marktdynamik und neuen Erkenntnissen ab. Produkte mit hohem Risiko erfordern in der Regel jährliche Aktualisierungen, während für andere festgelegte Intervalle gelten können. Die Bewertungen müssen zudem überarbeitet werden, wenn sich wesentliche Sicherheitshinweise, neue klinische Daten, technologische Fortschritte oder Änderungen der Leitlinien ergeben, um ein genaues Nutzen-Risiko-Profil zu gewährleisten.
05. Welche Rolle spielen Ein- und Ausschlusskriterien bei der Literaturrecherche im Bereich MDR/IVDR?
Einschluss- und Ausschlusskriterien stellen sicher, dass nur relevante, qualitativ hochwertige Evidenz ausgewählt wird. Sie verbessern die Objektivität, verringern die Voreingenommenheit der Gutachter und gewährleisten eine einheitliche Entscheidungsfindung. Gemäß MDR/IVDR müssen diese Kriterien im Voraus festgelegt, begründet und auf die Forschungsfragen abgestimmt sein, um während des gesamten Bewertungsprozesses die Rückverfolgbarkeit und die regulatorische Rechtfertigbarkeit zu gewährleisten.
06. Warum ist eine kritische Bewertung bei Literaturrecherchen im Rahmen der MDR/IVDR unerlässlich?
Bei der kritischen Bewertung werden die methodische Qualität, die Relevanz und die Zuverlässigkeit der einbezogenen Evidenz beurteilt. Die Rahmenwerke der MDR und IVDR legen besonderen Wert auf diese Bewertung, da sich die Regulierungsbehörden auf fundierte Angaben zu Sicherheit und Leistung stützen. Eine strenge Bewertung trägt dazu bei, solide Daten von weniger aussagekräftigen Studien zu unterscheiden, und stärkt die Schlussfolgerungen, die in vergleichenden Wirksamkeitsstudien (CERs), Wirksamkeits- und Sicherheitsstudien (PERs), Berichten zur Marktüberwachung (PMS) sowie Nutzen-Risiko-Analysen verwendet werden.
07. Inwiefern unterscheiden sich die Anforderungen an die Literaturrecherche gemäß MDR und IVDR?
Die MDR konzentriert sich auf die klinische Bewertung, die Nutzen-Risiko-Abwägung und die klinische Leistungsfähigkeit, während die IVDR den Schwerpunkt auf die analytische Leistungsfähigkeit, die wissenschaftliche Validität und die klinische Leistungsfähigkeit im Hinblick auf die diagnostische Genauigkeit legt. Die Literaturstrategien müssen diesen Unterschieden Rechnung tragen, indem Forschungsfragen, Datensätze und Bewertungsrahmen auf die jeweils für die einzelnen Verordnungen erforderlichen spezifischen Evidenzpfade zugeschnitten werden.
08. Welche Datenbanken und Informationsquellen werden bei einer an die MDR/IVDR angepassten Literaturrecherche erwartet?
Die Aufsichtsbehörden erwarten die Nutzung verschiedener wissenschaftlicher Datenbanken wie PubMed, Embase und Cochrane, ergänzt durch Vigilanzdatenbanken, Register für klinische Studien, Leitlinien und einschlägige Graue Literatur. Die Nutzung vielfältiger Quellen gewährleistet eine umfassende Erfassung der klinischen, leistungsbezogenen und sicherheitsrelevanten Informationen, die für eine fundierte Bewertung und kontinuierliche Überwachung erforderlich sind.
09. Warum gilt Freyr als führender Partner im Bereich Literaturrecherche und Protokollierung?
Freyr gilt aufgrund seiner umfassenden Kenntnis der regulatorischen Rahmenbedingungen, seiner wissenschaftlichen Genauigkeit und seiner konsequenten Einhaltung der Evidenzanforderungen der MDR/IVDR als führender Partner. Das Team wendet Prinzipien der systematischen Literaturrecherche, eine transparente Methodik und Fachwissen in den jeweiligen Therapiebereichen an, um fundierte und prüfungsreife Ergebnisse zu erzielen. Der Ansatz von Freyr legt den Schwerpunkt auf Rückverfolgbarkeit, kritische Bewertung und Benchmarking nach dem neuesten Stand der Technik – Schlüsselfaktoren, die von benannten Stellen und globalen Regulierungsbehörden geschätzt werden.

 Benchmark-Technologien und Behandlungsstandards ermitteln
Benchmark-Technologien und Behandlungsstandards ermitteln Festlegung anerkannter Sicherheits- und Leistungsprofile
Festlegung anerkannter Sicherheits- und Leistungsprofile Vergleichen Sie das betreffende Gerät mit aktuellen Alternativen
Vergleichen Sie das betreffende Gerät mit aktuellen Alternativen Unterstützung von CER-, PER-, CEP-, PEP-, PMS- und PMCF-Aktivitäten
Unterstützung von CER-, PER-, CEP-, PEP-, PMS- und PMCF-Aktivitäten Starke Belege für die Nutzen-Risiko-Abwägung erbringen
Starke Belege für die Nutzen-Risiko-Abwägung erbringen Nutzen-Risiko-Abwägung
Nutzen-Risiko-Abwägung Wissenschaftliche Validität
Wissenschaftliche Validität Analytische Leistungsfähigkeit
Analytische Leistungsfähigkeit Entwicklung von PER und PEP
Entwicklung von PER und PEP Anforderungen an den Nachweis im Rahmen des PMPF
Anforderungen an den Nachweis im Rahmen des PMPF Strengere Neuklassifizierung, die mehr Belege erfordert
Strengere Neuklassifizierung, die mehr Belege erfordert






