Übersicht der EU MDR Konformitätsdienstleistungen
Die EU-Medizinprodukte-Verordnung (MDR) ist am 26. Mai 2021 in Kraft getreten, nach einer dreijährigen Übergangsfrist und einer zusätzlichen einjährigen Verlängerung aufgrund der COVID-19-Pandemie. Geräte, die jetzt auf dem EU-Markt eingeführt werden, müssen diesen Vorschriften entsprechen und von den unter diesen Vorschriften akkreditierten Benannten Stellen gemäß EU MDR CE-zertifiziert werden. Geräte, die bereits gemäß EU MDD CE-zertifiziert wurden, haben jedoch Übergangsfristen, bevor sie die EU MDR-Anforderungen vollständig erfüllen müssen. Während dieser Übergangsfrist werden die gemäß EU MDD und EU MDR zertifizierten Geräte gleichberechtigt und ohne Diskriminierung auf dem Markt koexistieren. Freyr bietet unübertroffene EU MDR Konformitätsdienstleistungen an, um Medizinprodukteunternehmen dabei zu unterstützen, die EU MDR-Anforderungen zeitnah zu erfüllen.
Übergangszeitplan und neue Klassifizierungen für Medizinprodukte
Die Europäische Medizinprodukte-Verordnung (MDR) wird ab Mai 2021 in allen EU Member States und den Staaten der Europäischen Freihandelsassoziation (EFTA) vollständig wirksam sein und gewährt Herstellern eine Übergangsfrist von 4 Jahren für die vollständige EU MDR-Zertifizierung.
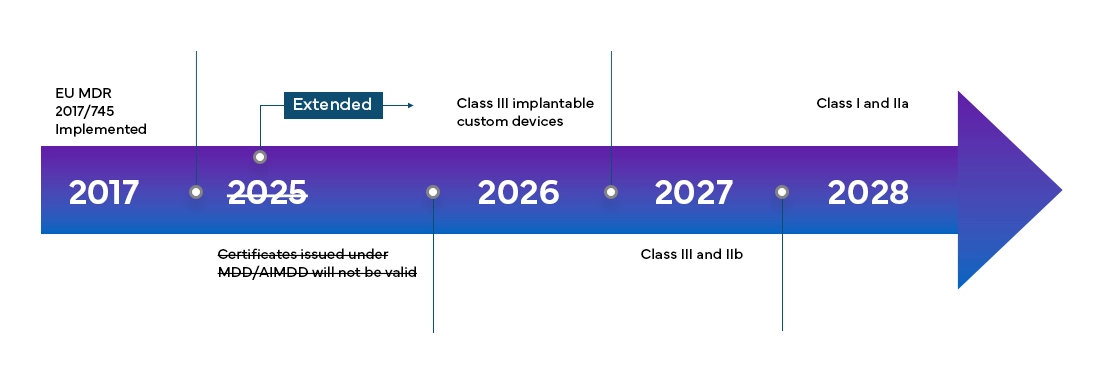
Die neue Europäische Medizinprodukte-Verordnung (MDR) hat, wie festgestellt, auch Änderungen am bestehenden Klassifizierungssystem für Geräte mit sich gebracht, wie zum Beispiel:
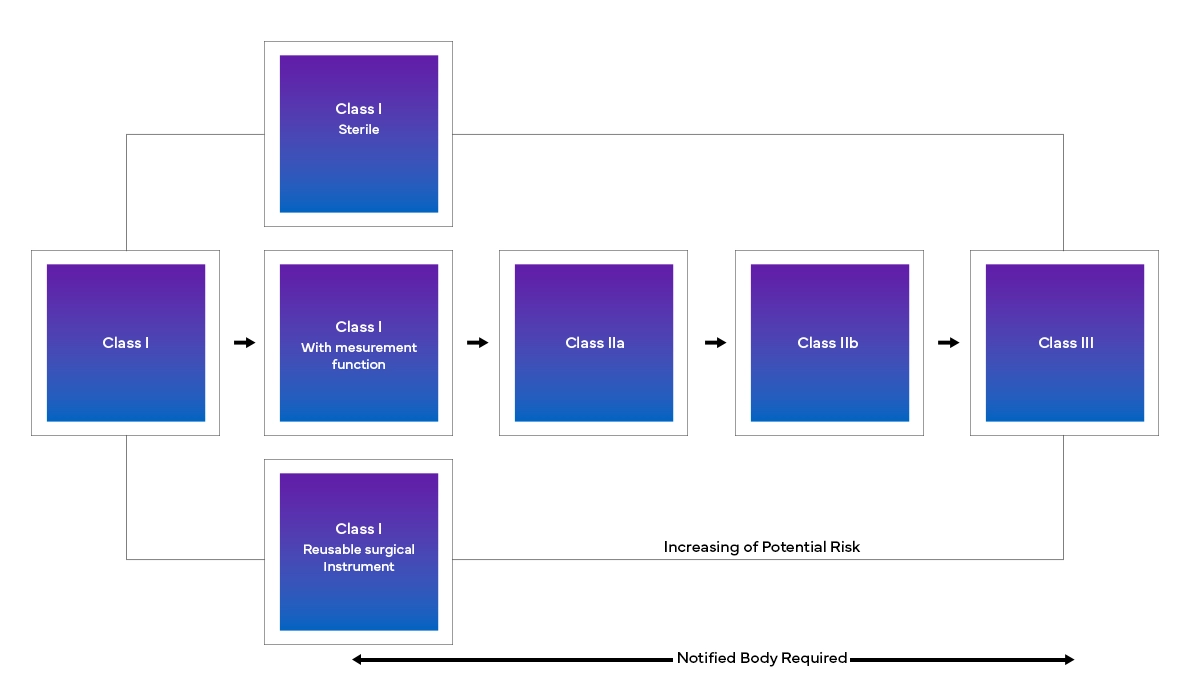
Von der Identifizierung der genauen Änderungen bis zu deren Echtzeit-Implementierung müssen Hersteller möglicherweise eine Reihe von Herausforderungen bewältigen, um die EU MDR-Anforderungen zu erfüllen. Angefangen bei der Entschlüsselung der neuen Struktur, der genauen Klassifizierung eines Geräts bis hin zur Zusammenstellung und Einreichung aller Daten ist für Hersteller ein detaillierterer und funktionsübergreifender regulatorischer Ansatz erforderlich, um den neuen europäischen Medizinprodukte-Verordnungen gerecht zu werden. Mit einer strengen Lückenanalyse unterstützt Freyr Kunden beim Status quo und bietet somit die notwendigen regulatorischen Maßnahmen, die für den Übergang und die EU MDR Konformität erforderlich sind.
EU MDR Konformitätsdienstleistungen
- Entwicklung einer klaren Implementierungsstrategie für die Medizinprodukte-Verordnung (MDR)
- Die neue Gesetzgebung verstehen und eine Lückenanalyse der bestehenden Qualitätsmanagementsysteme (QMS) und Prozesse durchführen
- Entwicklung eines detaillierten Plans mit einem funktionsübergreifenden Ansatz, um die Aspekte des Qualitätssystems zu bestimmen, die im Hinblick auf die neue EU-Medizinprodukte-Verordnung angepasst werden müssen
- Bildung mehrerer Teams innerhalb der Organisation zur Analyse von Produktumfang, Klassifizierung, QMS-Management usw., mit einem zentralen Ansprechpartner in jedem Team
- Zuweisung und Planung von Ressourcen.
- Berücksichtigung der Interaktion Ihres QMS mit anderen Vorschriften und Nutzung dieser Gelegenheit zur Prozessoptimierung, wobei gleichzeitig Flexibilität für zukünftige Änderungen gewährleistet wird
- Analyse der vorhandenen Testdaten und Prüfung auf zusätzliche Anforderungen, die die MDR festlegt
- Abstimmung von Erwartungen und Übergangsplan mit Ihren benannten Stellen in der EU
- Lückenanalyse für bestehende Medizinprodukte von den EU MDD- zu den EU MDR-Vorschriften
- End-to-End-Unterstützung bei der Erstellung von Klinischen Bewertungsberichten (CER), einschließlich Literaturrecherche gemäß den Leitlinien der Europäischen Medizinprodukte-Verordnung (EU MDR)
- End-to-End-Dienstleistungen für Berichte zur Überwachung nach dem Inverkehrbringen (PMSR), regelmäßige Berichte zur Aktualisierung der Sicherheit (PSUR) und die Zusammenfassung der Sicherheit und der klinischen Leistung (SSCP)
- Erweiterung regulatorischer Ressourcen mit Optionen für den Einsatz im In- und Ausland
- Dienstleistungen als Europäischer Bevollmächtigter (EAR)
- MDR-Konformität und Unterstützung bei der Einreichung bei benannten Stellen
- Regulatorische Intelligenz, die den Importprozess verschiedener regulierter Märkte abdeckt
- QMS-Konformität und Schein-Audits
- Dokumentenmanagementsystem und Tool für MDR-Unternehmen
- Klassifizierung und Reklassifizierung von Medizinprodukten nach Risiko
- UDI-Implementierung und Beratung
- EU-Medizinprodukte-Verordnung-konforme Dienstleistungen zur Überwachung nach dem Inverkehrbringen
- Beratung zum Risikomanagement nach ISO 14971
- Inhouse- und Online-Schulungen
- Verantwortliche Person für Regulierungs-Compliance-Dienstleistungen und Unterstützung
- Identifizierung von MDR Benannten Stellen

Für End-to-End-Regulierungsunterstützung bei EU MDR kontaktieren Sie Freyr.








