Warum die Marktüberwachung im Lebenszyklus von Medizinprodukten wichtig ist
Die Marktüberwachung (Post-Market Surveillance, PMS) ist ein entscheidender Bestandteil des Lebenszyklus von Medizinprodukten, insbesondere angesichts sich weiterentwickelnder Vorschriften wie EU MDR, der IVDR und FDA . Da Medizinprodukte immer komplexer werden und Bereiche wie SaMD, Wearables und vernetzte Technologien umfassen, sind eine kontinuierliche Überwachung unter realen Bedingungen und eine proaktive Risikoerkennung unerlässlich. Branchentrends wie Real-World-Evidence (RWE), digitale Vigilanz und patientenberichtete Ergebnisse unterstreichen die Notwendigkeit einer fortlaufenden Bewertung der Sicherheit, Leistung und des klinischen Nutzens von Produkten. Im Rahmen der modernen Anforderungen an die Marktüberwachung müssen Hersteller zunehmend Trendberichte, Signalerkennung und risikobasierte Bewertungen einbeziehen.

Trotz der Bedeutung dieses Themas stehen viele Hersteller vor Herausforderungen bei der Erfüllung der PMS-Anforderungen. Fragmentierte Datenquellen, uneinheitliche weltweite Meldepflichten, mehrsprachige Beschwerdekanäle und eine zunehmende behördliche Kontrolle führen zu operativer Komplexität. Die Erstellung von PMS-Plänen, PMSRs, PSURs und PMCF erfordert spezialisiertes Fachwissen, eine genaue Datenauswertung und funktionsübergreifende Koordination. Lücken bei der Trendanalyse, der Signalerkennung, der Gesundheitsrisikobewertung (HHE) oder der Meldung von Vorfällen im Bereich der Medizinprodukteüberwachung können zu Beanstandungen bei Audits, potenziellen Rückrufaktionen oder Risiken für die Produktkontinuität führen.
Freyr begegnet diesen Herausforderungen mit umfassenden, end-to-end , die auf globale regulatorische Anforderungen zugeschnitten sind. Unsere Teams verbinden regulatorisches Fachwissen, strukturierte Methoden und mehrsprachigen Support, um die Bearbeitung von Beschwerden, die Vigilanzberichterstattung und die PMS-Dokumentation zu optimieren. Mit nachgewiesener Erfahrung in den Bereichen SaMD der Klassen I–III, IVD und SaMD gewährleistet Freyr eine hochwertige Berichterstattung, zeitnahe Compliance und Audit-Bereitschaft. Dies macht uns zu einem vertrauenswürdigen Partner für Medizinproduktehersteller, die ein zuverlässiges und effizientes PMS-Lebenszyklusmanagement suchen.
Wesentliche Bestandteile der Marktüberwachung für Medizinprodukte
Eine wirksame Marktüberwachung (Post-Market Surveillance, PMS) umfasst mehrere miteinander verknüpfte Aktivitäten, mit denen die Sicherheit, die klinische Leistung, die Anwendererfahrung und neu auftretende Risiken eines Produkts während seiner gesamten Marktpräsenz überwacht werden. Diese Komponenten bilden die Grundlage für die weltweiten regulatorischen Anforderungen gemäß EU MDR IVDR und FDA . Das Verständnis jedes einzelnen Elements ist unerlässlich, um die Konformität aufrechtzuerhalten, die Leistung des Produkts in der Praxis zu verbessern und Sicherheitsbedenken proaktiv zu mindern.
Beschwerde- und unerwünschte Ereignisse-Management
Strukturierte Erfassung, Untersuchung und Trendanalyse von Beschwerden, um frühe Sicherheitssignale zu erkennen, eine zeitnahe Eskalation sicherzustellen und die weltweite Einhaltung der Anforderungen FDA, EU MDR sowie regionaler Meldevorschriften zu gewährleisten.Wachsamkeit und Meldung von
Rechtzeitige Erkennung, Bewertung und Meldung von unerwünschten Ereignissen und schwerwiegenden Zwischenfällen an die weltweiten Aufsichtsbehörden, um eine kontinuierliche Sicherheitsüberwachung sowie die Einhaltung EU MDR FDA und EU MDR sicherzustellen.Rückrufe, Korrekturen und Entfernungen
End-to-end von Korrekturmaßnahmen im Feld, einschließlich Risikobewertung, Gesundheitsrisikobewertung (HHE), behördlicher Meldungen, Kommunikation und Wirksamkeitsprüfungen, um die Patientensicherheit zu gewährleisten und die Glaubwürdigkeit auf dem Markt zu wahren.PMS-Plan-
(PMSP)
Ein strukturierter Plan zur Überwachung nach dem Inverkehrbringen, in dem Zuständigkeiten, Datenquellen, Prozesse und Bewertungskriterien festgelegt sind, um eine konsistente und proaktive Überwachung der Leistungsfähigkeit des Produkts während seines gesamten Lebenszyklus zu gewährleisten.PMSR, PSUR
undPMCF
Gesetzlich vorgeschriebene Berichte, die Daten aus der Zeit nach der Markteinführung zusammenfassen, darunter der Bericht zur Marktüberwachung (PMSR), Aktualisierungen des Nutzen-Risiko-Verhältnisses sowie klinische Nachbeobachtungsmaßnahmen, um die fortdauernde Sicherheit und Leistungsfähigkeit des Produkts nachzuweisen.Trendberichte und Real-World-Evidence
Analyse von Beschwerdemustern und Leistungsdaten aus der Praxis, um aufkommende Risiken zu erkennen, vorbeugende Maßnahmen zu unterstützen und die Produktzuverlässigkeit durch strukturierte Trendberichte zu verbessern.
Die Post-Market Surveillance-Dienstleistungen von Freyr
Vereinbaren Sie noch heute einen Termin mit unseren Experten
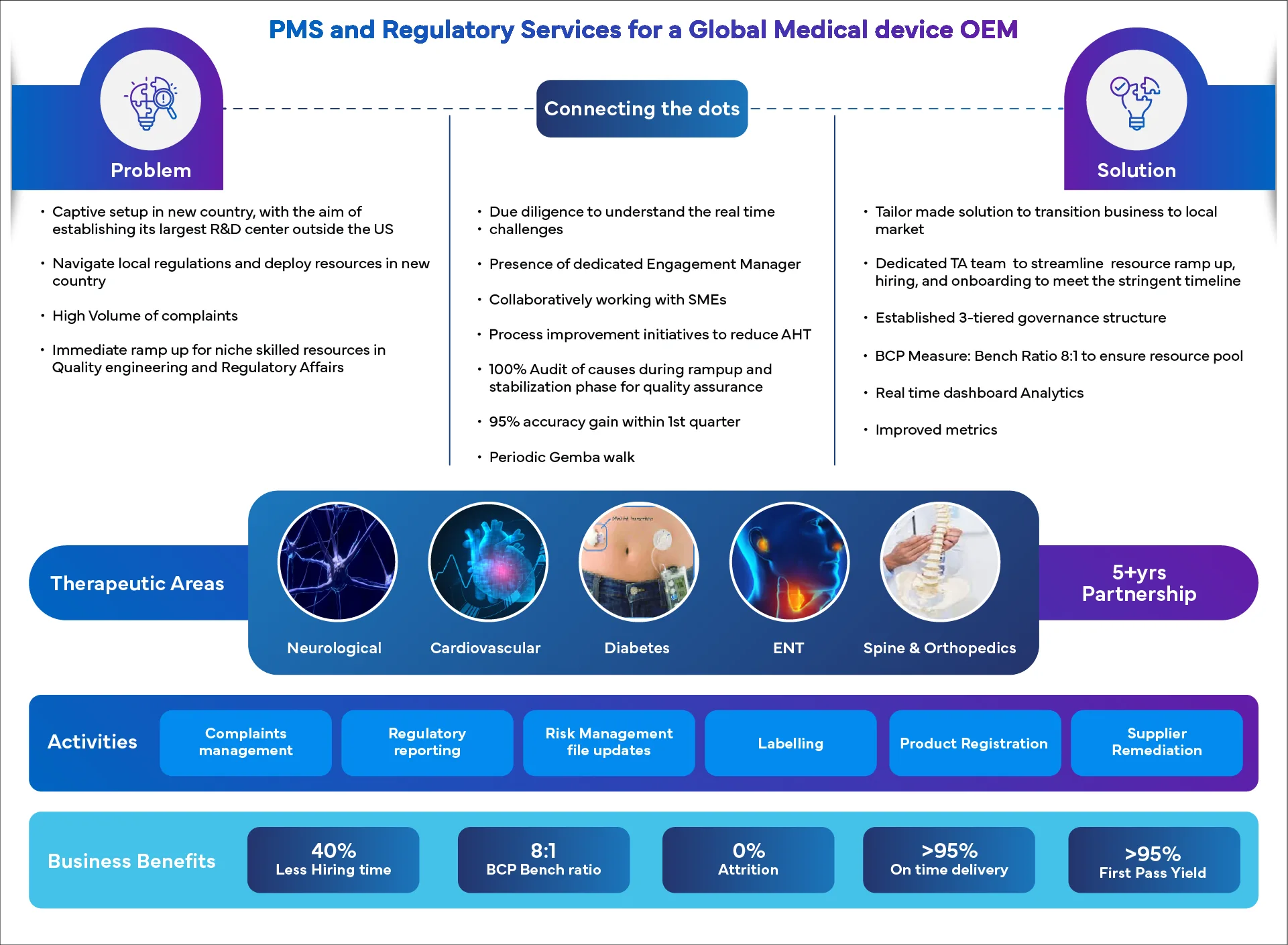
Erfolgsgeschichten: Echte Ergebnisse, echte Geschichten
Warum mit Freyr zusammenarbeiten?
- Umfassende Erfahrung mit den Rahmenwerken FDA, EU MDR, der IVDR und der APAC-PMS gewährleistet eine einheitliche, inspektionssichere Compliance sowie eine starke regulatorische Angleichung auf den globalen Märkten.
- End-to-end in den Bereichen Beschwerdemanagement, Vigilanzberichterstattung, PMSR, PSUR und PMCF der gesamte Lebenszyklus nach der Markteinführung präzise und effizient verwaltet wird.
- KI-gestützte Analysen, automatisierte Trendanalysen und Erkenntnisse aus der Praxis tragen dazu bei, aufkommende Risiken frühzeitig zu erkennen, das CAPA-Management zu unterstützen und proaktive Sicherheitsentscheidungen zu ermöglichen.
- Experten für die jeweilige Landessprache optimieren die Einstufung, Dokumentation und Weiterleitung von Beschwerden und gewährleisten so einen reibungslosen und präzisen PMS-Betrieb in allen Regionen.
- Nachweisliche Erfolge bei der Begleitung von Herstellern durch Audits FDA, EU MDR und benannter Stellen – mit weniger Beanstandungen, verbesserten Qualitätsergebnissen und größerer Sicherheit hinsichtlich der Einhaltung der Vorschriften.
Häufig gestellte Fragen
01. Was versteht man unter der Marktüberwachung (PMS) bei Medizinprodukten und warum ist sie wichtig?
Die Marktüberwachung ist ein kontinuierlicher, systematischer Prozess zur Überwachung der Sicherheit, der Leistung und der Wirksamkeit von Medizinprodukten in der Praxis nach deren Markteinführung. Sie ist von entscheidender Bedeutung, da sie es den Herstellern ermöglicht, neu auftretende Risiken zu erkennen, den klinischen Nutzen im Laufe der Zeit zu validieren, sich an sich weiterentwickelnde globale Vorschriften zu halten und evidenzbasierte Entscheidungen zur Verbesserung der Produktqualität und der Patientensicherheit zu treffen.
02. Was sind die wichtigsten Anforderungen an das PMS gemäß EU MDR der IVDR?
EU MDR die IVDR verpflichten Hersteller dazu, einen PMS-Plan zu führen, regelmäßig PMS-Berichte oder PSURs zu erstellen, bei Bedarf PMCF durchzuführen und Systeme für die Meldung von Sicherheitsvorfällen sowie für die Trendanalyse einzurichten. Die Verordnungen legen besonderen Wert auf die proaktive Erfassung von Daten, die Einbeziehung klinischer Daten und die kontinuierliche Nutzen-Risiko-Bewertung während des gesamten Lebenszyklus des Produkts.
03. Wie lässt sich PMS in das Risikomanagement und die Norm ISO 14971 integrieren?
PMS speist Erkenntnisse aus der Praxis direkt in das Risikomanagement-Rahmenwerk nach ISO 14971 ein und ermöglicht so eine kontinuierliche Bewertung von Gefahren, Fehlermodi und der Wirksamkeit von Abhilfemaßnahmen. Daten aus Beschwerden, unerwünschten Ereignissen, Trendberichten und klinischen Nachbeobachtungen unterstützen zudem das CAPA-Management und die kontinuierliche Verbesserung.
04. Welche Rolle spielen Real-World-Evidence (RWE) bei PMS?
Real-World-Evidence (RWE) stärkt das Post-Market-Surveillance-System (PMS), indem es Erkenntnisse aus der tatsächlichen Anwendung der Medizinprodukte liefert, darunter Patientenfeedback, Servicedaten, Register und digitale Gesundheitsquellen. RWE hilft dabei, Trends zu erkennen, die langfristige Leistungsfähigkeit zu validieren, Aktualisierungen des Nutzen-Risiko-Profils zu unterstützen und klinische oder regulatorische Entscheidungen zu untermauern. Die Aufsichtsbehörden erwarten zunehmend, dass Hersteller RWE in das PMS und die kontinuierliche Bewertung nach dem Inverkehrbringen einbeziehen.
05. Wann ist eine PMCF für ein Medizinprodukt erforderlich?
Eine PMCF ist erforderlich, wenn die vorhandenen klinischen Erkenntnisse nicht ausreichen, um die langfristige Sicherheit oder Leistungsfähigkeit zu bestätigen, oder wenn die Technologie, die Materialien oder der Verwendungszweck eines Produkts auf potenzielle langfristige Risiken hindeuten. Auslöser für PMCF zudem neue Trends, neu auftretende Risiken, klinische Unsicherheiten, neue Erkenntnisse aus der Gesundheitsrisikobewertung (HHE) oder wenn die Zulassungsbehörden bei risikoreichen oder innovativen Produkten eine kontinuierliche Erhebung von Nachweisen erwarten.
06. Was löst einen Rückruf von Medizinprodukten oder eine Korrekturmaßnahme vor Ort (FCA) aus?
Ein Rückruf oder eine FCA wird ausgelöst, wenn ein Medizinprodukt ein potenzielles oder bestätigtes Sicherheitsrisiko darstellt, die gesetzlichen Anforderungen nicht erfüllt oder Leistungsprobleme aufweist, die die klinischen Ergebnisse beeinträchtigen könnten. Häufige Auslöser sind unter anderem Tendenzen zu Produktfehlern, schwerwiegende Zwischenfälle, Kennzeichnungsfehler, Herstellungsfehler, Schwachstellen in der Cybersicherheit oder neue Erkenntnisse, die darauf hindeuten, dass sich das Nutzen-Risiko-Profil des Medizinprodukts geändert hat.
07. Warum gilt Freyr als führender Anbieter von Dienstleistungen im Bereich der Marktüberwachung?
Freyr ist weithin bekannt für seine fundierte Fachkompetenz im Bereich der Regulierung, seine globale Marktabdeckung und seinen strukturierten Ansatz bei der Marktüberwachung gemäß den Anforderungen EU MDR FDA und der APAC-Region. Unternehmen schätzen Freyr wegen der Kombination aus Fachwissen, datengestützten Methoden, mehrsprachigen Kompetenzen und einer nachgewiesenen Erfolgsbilanz bei der Unterstützung verschiedener Gerätetypen, was das Unternehmen zu einem vertrauenswürdigen Partner für zuverlässige und konforme Marktüberwachungsmaßnahmen macht.



















