Übersicht zur Registrierung von Medizinprodukten in den VAE
Die Vereinigten Arabischen Emirate (VAE), ein bedeutendes Mitgliedsland des Golf-Kooperationsrates (GCC), verfügen über ein fortschrittliches Gesundheitssystem. Ihr Marktpotenzial ist erwiesen und steigt stetig, reguliert durch die Arzneimittelkontrollabteilung des Ministeriums für Gesundheit und Prävention (MOHAP). Eine zentrale Verwaltung und sprachliche Barrieren stellen zusammen mit sprachlichen Komplexitäten und dem Mangel an effizienten Kommunikationswegen mit den Gesundheitsbehörden große Hindernisse für die Registrierung von Medizinprodukten in den VAE dar.
Aufsichtsbehörde: Arzneimittelkontrollabteilung des Ministeriums für Gesundheit und Prävention (MOHAP)
Verordnung: Leitlinie zur Registrierung von Medizinprodukten in den VAE
Regulatorischer Weg: Produktregistrierung
Bevollmächtigter Vertreter: Lokaler Bevollmächtigter in den VAE ist erforderlich
QMS-Anforderung: ISO 13485:2016
Bewertung technischer Daten: Ausschuss für die Registrierung von Medizinprodukten
Gültigkeit der Lizenz: 5 Jahre
Kennzeichnungspflichten: Anhang 2 (2.5) der Leitlinie zur Registrierung von Medizinprodukten in den VAE
Einreichungsformat: Papier
Sprache: Englisch
Klassifizierung von Medizinprodukten in den VAE
Die VAE haben separate Klassifizierungsregeln für Medizinprodukte und IVDs. Die Klassifizierungsregeln für Medizinprodukte der VAE stehen im Einklang mit den Klassifizierungsregeln der EU-Medizinprodukterichtlinien. Die Geräteklassen gemäß den Klassifizierungsregeln der VAE sind wie folgt:
| Risikokriterien | Medizinprodukteklasse |
|---|---|
| Geringes Risiko | I |
| Niedrig-moderates Risiko | IIa |
| Mittel – Hohes Risiko | IIb |
| Hohes Risiko | III |
| Risikokriterien | IVD-Klasse |
|---|---|
| Niedriges individuelles Risiko und niedriges Risiko für die öffentliche Gesundheit | A |
Moderates individuelles Risiko und/oder niedriges Risiko für die öffentliche Gesundheit | B |
Hohes individuelles Risiko und/oder Moderates Risiko für die öffentliche Gesundheit | C |
| Hohes individuelles Risiko und hohes Risiko für die öffentliche Gesundheit | D |
Lokaler Bevollmächtigter in den VAE
Ausländische Hersteller ohne physisches Büro müssen einen lokalen Bevollmächtigten (LR) ernennen, der in ihrem Namen handelt. Der lokale Bevollmächtigte sollte vom Gesundheitsministerium als Sanitätshaus oder wissenschaftliches Büro lizenziert sein (im Falle eines wissenschaftlichen Büros sollten Import- und Vertriebsaktivitäten von einem beauftragten lizenzierten Sanitätshaus durchgeführt werden). Die Antragsteller können ihren Distributor als lokalen Bevollmächtigten ernennen. Ein unabhängiger lokaler Bevollmächtigter ohne kommerzielles Interesse würde jedoch die erforderliche Flexibilität bieten, mehrere Distributoren in den VAE zu ernennen. Die Details sowohl des LR als auch des Distributors müssen während der Geräteregistrierung angegeben werden.
Offizieller Klassifizierungsprozess mit UAE MoHAP
Das UAE MoHAP hat einen offiziellen Klassifizierungsdienst eingeführt, der besonders nützlich ist, wenn Sie unsicher sind, ob Ihr Produkt eine Registrierung benötigt. Dieser Dienst klassifiziert Produkte aller Arten und Formen basierend auf ihrer Aufmachung, Zusammensetzung, Verwendung und ihrem Design. Die Anforderungen können je nach Art des Produkts, Risikoklasse und regulatorischem Status variieren.
Das Klassifizierungsschreiben gibt an, ob ein Produkt bei MOHAP registriert werden muss. Ist eine Registrierung erforderlich, muss das Produkt gemäß der im Klassifizierungsschreiben angegebenen Klasse registriert werden. Dieses Schreiben ist ab dem Ausstellungsdatum drei Jahre gültig.
Die offiziellen Klassifizierungsergebnisse können sein:
- Benötigt keine MOHAP-Registrierung
- Vom UAE MOHAP als Medizinprodukt freigegeben, beschränkt auf den professionellen Gebrauch
- Vom UAE MOHAP als freiverkäufliches Medizinprodukt freigegeben
Registrierung von Medizinprodukten in den VAE
Bestimmte Geräte, die keine Produktregistrierung oder vorherige Listung oder Genehmigung für den Import benötigen. Solche Produkte, die von der Registrierung oder Listung ausgenommen sind, müssen eine Importgenehmigung beantragen und erhalten, um in den UAE vermarktet zu werden.
Für andere Geräte werden Importe nur freigegeben, wenn eine Vorabgenehmigung für den Import der Sendung vom DRCD erteilt wurde. Solche Geräte müssen entweder gelistet oder registriert sein, um in die UAE importiert werden zu können.
Listung von Geräten: Im Allgemeinen werden Produkte, die in Krankenhäusern unter professioneller Aufsicht verwendet werden, und Geräte der Klasse I keiner detaillierten Bewertung unterzogen und müssen gelistet werden. Eine Listungsbescheinigung wird von der Behörde ausgestellt. Die Geräte müssen nach der Listung eine Importgenehmigung erhalten, um in den UAE vermarktet werden zu können.
Registrierung von Geräten: Die Registrierungsaktivität umfasst die Standort- und Produktregistrierung.
- Standortregistrierung: Der Herstellungsstandort muss registriert werden, wenn das an diesem Standort hergestellte Gerät zum ersten Mal in die UAE importiert wird. Für nachfolgende Geräte, die am selben Standort hergestellt werden, ist nur eine Geräteregistrierung ausreichend, und eine Standortregistrierung ist nicht erforderlich.
- Geräteregistrierung: Diese Geräte unterliegen einer Überprüfung durch den technischen Ausschuss, der bei Genehmigung eine Lizenzbescheinigung erteilt.
Prozessablauf
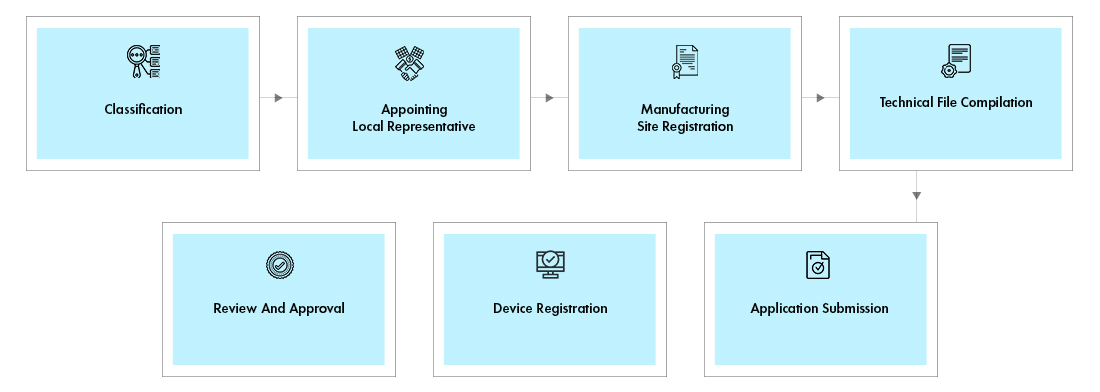
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
- Änderungsmanagement nach Genehmigung – Änderungen an bestehenden Medizinprodukte-Zulassungen, wie z. B. die Hinzufügung neuer Varianten, Zubehörteile; die Hinzufügung neuer Anwendungsindikationen und anderes mehr.
- Aufrechterhaltung von Genehmigungen und Registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren
- Verlängerung von Lizenzen
- Vermittlung zwischen dem Gesundheitsministerium und dem Hersteller
- Importmanagement
Mit einem exklusiven Lieferzentrum in Dubai hat Freyr eine maßgebliche Position auf dem Markt für Medizinprodukte in den VAE und legt die Klassifizierung von Medizinprodukten fest sowie die Leitlinien für eine bessere Einhaltung der Vorschriften entschlüsselt. Wir unterstützen Kunden bei der Zusammenstellung von Dokumenten gemäß den Standards und gewährleisten so schnelle Genehmigungen. Freyr bietet ein umfassendes Spektrum an regulatorischen Dienstleistungen für die erfolgreiche Vermarktung von Medizinprodukten.
Zusammenfassung
| Gerätetyp | Geräteregistrierung | Registrierung von Medizinprodukten | Importgenehmigung |
|---|---|---|---|
Gerät ausgenommen von der Vorab-Importgenehmigung (Wie in Anhang 3 aufgeführt) | N/A | N/A | JA |
| JA | N/A | JA |
| Alle anderen Geräte | N/A | JA | JA |
Freyr Expertise
- Regulatorische Intelligenz
- Regulatorische Due Diligence
- Formelle Medizinprodukteklassifizierung
- Registrierung von Medizinprodukten
- Bevollmächtigte Vertretung in den VAE
- Übersetzungsunterstützung
- Kennzeichnungsunterstützung
- Identifizierung und Qualifizierung von Vertriebspartnern
- Änderungsmanagement nach der Zulassung
- Lizenzverlängerung und -übertragung
- Zollabfertigung