
Regulierungsdienstleistungen für Medizinprodukte
in Singapur – Überblick
Medizinprodukte in Singapur werden durch den Health Products Act (HPA) und die Health Product (Medical Devices) Regulations 2010 reguliert.
Aufsichtsbehörde: Gesundheitsbehörde (HSA)
Verordnung: Gesundheitsprodukte (Medizinprodukte) Verordnung 2010
Regulatorischer Weg: Abteilung für Medizinprodukte der Gesundheitsbehörde (HSA)
Bevollmächtigter Vertreter: Registrant in Singapur
QMS-Anforderung: SS 620:2016, Singapur-Standard für gute Vertriebspraxis für Medizinprodukte, und ISO 13485:2016
Bewertung technischer Daten: Gesundheitsbehörde (HSA)
Gültigkeit der Lizenz: Alle Händlerlizenzen sind 12 Monate ab dem Datum der Genehmigung gültig
Anforderungen an die Kennzeichnung: Regulierungsleitfaden, GN-23 Überarbeitet (1. März 2020)
Einreichungsformat: Online
Sprache: Englisch
HSA-Klassifizierung von Medizinprodukten
Die HSA wendet 16 Regelwerke an, um Medizinprodukte nach dem Risiko von der niedrigsten bis zur höchsten Stufe in die Klassen A, B, C und D einzuteilen.
Die Risikoklassifizierung hängt von Faktoren wie der Kontaktdauer, dem Invasionsgrad, dem Verwendungszweck und der Anwendungsmethode ab.
Medizinprodukteklassifizierung, HSA
| Risikoklasse | Risikostufe | Beispiele für Medizinprodukte |
|---|---|---|
| Klasse A | Geringes Risiko | Filmbetrachter, chirurgische Hand, Hülle, Sauerstoffmaske |
| Klasse B | Geringes bis mittleres Risiko | Blutdruckmanschette, Dampfsterilisator |
| Klasse C | Mittleres bis hohes Risiko | Patientenmonitor, Röntgengerät |
| Klasse D | Hohes Risiko | Herzstents, Herzschrittmacher |
IVD-Klassifizierung
In-vitro-Medizinprodukte werden unten vom niedrigsten zum höchsten Risiko klassifiziert.
Risikoklasse | Risikostufe | Beispiele für In-vitro-Medizinprodukte |
|---|---|---|
| Klasse A | Niedriges individuelles Risiko und niedriges Risiko für die öffentliche Gesundheit | Probengefäß |
| Klasse B | Moderates individuelles Risiko oder niedriges Risiko für die öffentliche Gesundheit oder beides | Vitamin B12, Schwangerschafts-Selbsttests, antinukleärer Antikörper, Urinteststreifen |
| Klasse C | Hohes individuelles Risiko oder moderates Risiko für die öffentliche Gesundheit oder beides | Blutzucker-Selbsttest, HLA-Typisierung, PSA-Screening, Röteln-IgM |
| Klasse D | Hohes individuelles Risiko und hohes Risiko für die öffentliche Gesundheit | HIV-Blutspenderscreening, HIV-Diagnosekit |
Bevollmächtigter für Medizinprodukte in Singapur / Registrant
Ein Registrant ist die Kontaktperson zwischen Ihrem Unternehmen und der HSA, die die Auflistung der Geräteregistrierung in Singapur bearbeitet. Der autorisierte Vertreter für Medizinprodukte in Singapur bearbeitet den Registrierungsantrag bei der HSA und ist Inhaber Ihrer HSA-Geräteregistrierung. Nur in Singapur ansässige Unternehmen oder juristische Personen können als Registrant fungieren; sie müssen auch bei der HSA registriert sein.
HSA-Registrierung von Medizinprodukten
Der HSA-Registrierungsprozess für Medizinprodukte wird über das Online-Informations- und Kommunikationssystem für Medizinprodukte (MEDICS) der HSA durchgeführt. Jede HSA-Geräteregistrierung erfolgt über einen spezifischen Bewertungsweg, abhängig von den folgenden Faktoren:
- Risikoklassifizierung des Geräts.
- Anzahl der vorherigen Genehmigungen, die von den ausländischen Referenz-Regulierungsbehörden erteilt wurden.
- Dauer der Sicherheits-Markthistorie des Geräts.
Der Bewertungsweg des Geräts bestimmt die Bearbeitungszeit (TAT), die Gebühren und die für die Registrierung erforderlichen Dokumente.
Klasse-A-Registrierung – Medizinprodukte der Klasse A sind von der Produktregistrierung ausgenommen. Es ist jedoch erforderlich, die Ausnahmeliste für Klasse-A-Produkte in MEDICS während des Antrags auf eine Händlerlizenz auszufüllen.
Prozessablauf
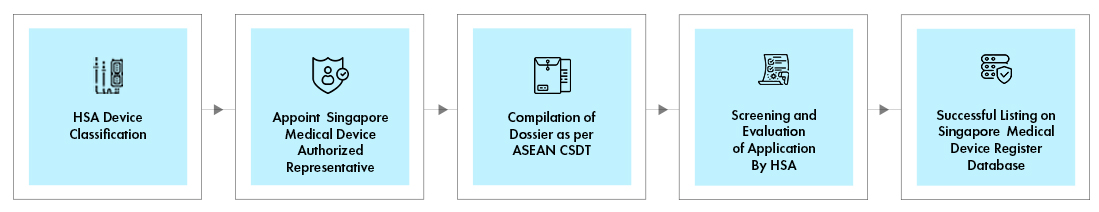
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End-Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel:
- Änderungsmanagement nach der Zulassung – Änderungen an bestehenden Medizinproduktezulassungen, wie zum Beispiel die Hinzufügung neuer Varianten und Zubehörteile oder die Erweiterung um neue Verwendungszwecke.
- Aufrechterhaltung von Medizinproduktezulassungen und -registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren.
- Verlängerung der Lizenz.
Mit einem professionellen Team zur Bereitstellung regulatorischer Unterstützung hilft Freyr Herstellern, die für die Zulassung erforderliche Qualität und Sicherheit aufrechtzuerhalten. Die Experten von Freyr beobachten aufmerksam regulatorische Aktualisierungen und informieren Kunden über die notwendigen Schritte zur Produktkonformität mit den geltenden Standards.
Zusammenfassung
Die Bearbeitungszeit für die Produktregistrierung ist in der folgenden Tabelle aufgeführt.
| Risikoklasse | Sofort | Beschleunigt | Verkürzt | Vollständige Bewertung | Vollständig (Verfahren mit vorrangiger Prüfung) |
|---|---|---|---|---|---|
| Klasse B | Sofortige Registrierung bei Einreichung | 100 Arbeitstage | 160 Arbeitstage | 120 Arbeitstage | |
| Klasse C | Sofortige Registrierung bei Einreichung (nur für eigenständige medizinische mobile Anwendungen der Klasse C) | 120 Arbeitstage | 160 Arbeitstage | 220 Arbeitstage | 165 Arbeitstage |
| Klasse D | 180 Arbeitstage | 220 Arbeitstage | 310 Arbeitstage | 235 Arbeitstage | |
| Klasse D (Produkte, die Arzneimittel enthalten) | 220 Arbeitstage | 310 Arbeitstage |
Die Bearbeitungszeit für einen Wechsel des Registranten beträgt 40 Arbeitstage.
HINWEIS-
- Medizinprodukte der Klasse A sind von der Produktregistrierung ausgenommen.
- Die Bearbeitungszeit schließt die Zeit aus, die für die Beantwortung von Anfragen der HSA nach Klärung oder zusätzlichen Informationen während der Bewertungsphase benötigt wird.
Freyr Expertise
- Regulatorische Due Diligence für die Geräteregistrierung bei der HSA, Singapur
- HSA-Klassifizierung und -Gruppierung von Medizinprodukten
- Unterstützung bei der Bewertung durch eine Konformitätsbewertungsstelle (CAB)
- Erstellung des ASEAN Common Submission Dossier Template (CSDT) Dossiers
- HSA Geräteregistrierung;
- Rechtliche Vertretung
- Unterstützung bei der Kennzeichnung
- Identifizierung und Qualifizierung von Distributoren
- Überwachung nach dem Inverkehrbringen
- Änderungsmanagement nach der Zulassung
- Lizenzverlängerung und -übertragung
- Einreichungs- und Kommunikationsdienste mit der HSA



