Leistungsbeschreibung (SOW) für den 510(k)-Antrag für aktive und nicht-aktive Medizinprodukte – Überblick
Bei Freyr sammelt und aufbereitet unser Expertenteam sorgfältig die neuesten Informationen, die für Ihre 510(k)-Einreichungen unerlässlich sind, und deckt dabei sowohl aktive als auch nicht-aktive Medizinprodukte ab. So stellen wir sicher, dass Sie über das erforderliche Wissen verfügen, um sich sicher im regulatorischen Rahmen zu bewegen. Von der Klärung der Unterschiede zwischen aktiven und nicht-aktiven Produkten bis hin zur Vertiefung der Feinheiten des 510(k)-Antrags haben wir ein umfangreiches Repository an Ressourcen als Ihre primäre Referenz zusammengestellt. Begeben Sie sich mit unserem umfassenden Leitfaden auf den Weg zur Beherrschung des 510(k)-Antrags für aktive Medizinprodukte und des 510(k)-Antrags für nicht-aktive Medizinprodukte.
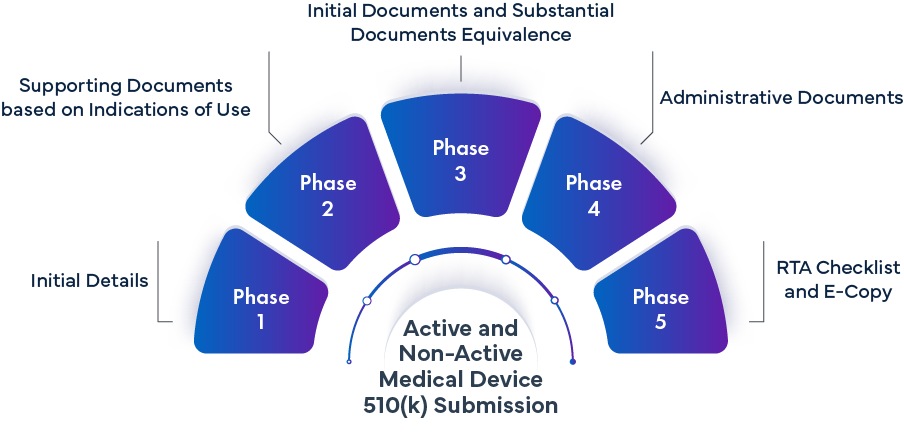
Phase -1 Erste Details | ||
|---|---|---|
Anforderungen | Umfang des 510(k)-Antragstellers | Leistungsumfang von Freyr |
| Zweckbestimmung |
|
|
| Angaben zum Verwendungszweck (Formular 3881) |
|
|
| Gerätebeschreibung |
|
|
| Standards und Leitlinien |
|
|
| Referenzprodukt |
|
|
| Zusammenfassung zum 510(k)-Verfahren |
|
|
Phase 2: Begleitende Dokumentation basierend auf den Zweckbestimmungen | |||
|---|---|---|---|
Dokumentenanforderungen | Umfang des 510(k)-Antragstellers | Leistungsumfang von Freyr | |
| 2.1 | Gerätezeichnung | Reichen Sie die Gerätezeichnungsdatei ein, um eine genaue Darstellung des Gerätedesigns zu gewährleisten. | Stellen Sie einen formellen Antrag für eine Gerätezeichnung eines aktiven Geräts. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig die notwendigen Informationen für die 510(k)-Einreichung. |
| 2.2 | Design und Entwicklung des Geräts | Reichen Sie die Design- und Entwicklungsdatei des aktiven Geräts ein, die alle relevanten Informationen und Dokumentationen umfasst. | Reichen Sie einen Antrag für das Design und die Entwicklung eines aktiven Geräts ein. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.3 | Sicherheitsdatenblatt | Bereitstellung der Sicherheitsdatenblätter (MSDS) für die wesentlichen Komponenten des aktiven Geräts, um umfassende Informationen zu deren Sicherheit und Zusammensetzung zu gewährleisten. | Senden Sie eine Anforderung für ein Sicherheitsdatenblatt der entscheidenden Komponenten des aktiven Geräts. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.4 | Herstellungsflussdiagramm | Stellen Sie ein Herstellungsflussdiagramm bereit, das den Produktionsprozess des aktiven Geräts detailliert darstellt und eine visuelle Darstellung der Herstellungsschritte und ihrer Abfolge bietet. | Einreichung einer Anforderung für das Material Safety Data Sheet (MSDS) der wesentlichen Komponenten für das aktive Gerät. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.5 | Gerätebeschreibung | Geben Sie umfassende Details an, einschließlich: o Eine Übersicht über das Gerät o Funktionen und Betriebsmodi o Blockdiagramme o Fotos, Kabel und relevantes Zubehör o Geräteinteroperabilität. o Beschreibung der Stromversorgung | Reichen Sie eine Anfrage für detaillierte Informationen über das Gerät ein. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.6 | Vorgeschlagene Kennzeichnung | Stellen Sie die Gebrauchsanweisung (IFU), das Benutzerhandbuch und alle zugehörigen Werbematerialien für das aktive Medizinprodukt bereit. | Reichen Sie einen Antrag für die Gebrauchsanweisung (IFU), das Benutzerhandbuch und alle Werbematerialien ein, sofern verfügbar. Prüfen Sie die vom Antragsteller bereitgestellte Gebrauchsanweisung (IFU), das Benutzerhandbuch und das Werbematerial. Dokumentieren Sie die Gebrauchsanweisung (IFU), das Benutzerhandbuch und das Werbematerial für die 510(k)-Einreichung. |
| 2.7 | Verpackung & Transport | Legen Sie die Studienpläne und Berichte für die Validierung von Verpackung und Transport vor. | Reichen Sie eine Anfrage für den Studienplan und die Berichte zur Validierung von Verpackung und Transport ein. Prüfen Sie die Studienpläne und Berichte zur Validierung von Verpackung und Transport und geben Sie gegebenenfalls notwendige Korrekturen oder Feedback. |
| 2.8 | Sterilisation (Sofern Sterilität erforderlich) | Legen Sie die Studienpläne und Berichte für die Sterilisationsvalidierung vor. | Reichen Sie eine Anforderung für den Studienplan und die Berichte zur Sterilisationsvalidierung ein. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.9 | Leistungsprüfung – Bench-Tests | Stellen Sie einen förmlichen Antrag für die Studienpläne und Berichte der Bench-Tests zur Leistungsprüfung, in dem die spezifischen Anforderungen und zu berücksichtigenden Ziele dargelegt werden. | Reichen Sie eine Anforderung für die Studienpläne und Berichte der Bench-Tests des aktiven Geräts zur Leistungsprüfung ein. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
Elektromagnetische Verträglichkeit und elektrische Sicherheit – Begleitdokumentation | |||
| 2.10 | EMV-bezogene Geräteeigenschaften und Umgebungen des bestimmungsgemäßen Gebrauchs | Geben Sie Details zu EMV-bezogenen Geräteeigenschaften und Umgebungen des bestimmungsgemäßen Gebrauchs an, einschließlich: o Eine Übersicht über das Gerät. o Funktionen und Betriebsmodi. o Blockdiagramme. o Fotos, Kabel und relevantes Zubehör. o Geräteinteroperabilität. o Beschreibung der Stromversorgung, einschließlich der Möglichkeit, das intern betriebene Medizinprodukt während des Ladevorgangs zu verwenden. o Umgebungen, in denen das Medizinprodukt verwendet werden soll. o Beschreibung jeglicher drahtloser Technologie (falls zutreffend) für zusätzliche Überlegungen bezüglich drahtlos aktivierter Medizinprodukte. o Beschreibung aller internen HF-Sender im Medizinprodukt, die potenziell elektromagnetische Störungen verursachen könnten. o Berücksichtigung gängiger elektromagnetischer (EM) Sender sowie einzigartiger medizinischer Sender.
| Fordern Sie Informationen zu EMV-bezogenen Geräteeigenschaften und beabsichtigten Einsatzumgebungen an. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.11 | Risikobewertung | Legen Sie einen Risikomanagementplan vor, der eine Risikobewertung zur effektiven Risikominderung sowie einen umfassenden Risikomanagementbericht umfasst, der alle Risikoelemente abdeckt. Stellen Sie das überarbeitete Dokument mit vorgeschlagenen Korrekturen und Verbesserungen bereit. | Fordern Sie die Risikomanagementakte an und verlangen Sie die Dokumentation des Risikomanagementplans und -berichts, einschließlich der Identifizierung von Risikogefahren, der Risikobewertung und des Nachweises einer angemessenen Risikominderung. Der Risikomanagementbericht sollte alle Risikoelemente abdecken, vorzugsweise mit separaten Abschnitten zur besseren Übersichtlichkeit. Stellen Sie auf Anfrage des Antragstellers eine Vorlage des Risikomanagementplans und des Risikomanagementberichts bereit, die alle gerätebezogenen Risiken abdeckt. Überprüfen Sie die Daten in der Risikomanagementakte, einschließlich des vom Antragsteller bereitgestellten Plans und Berichts, und geben Sie Vorschläge für notwendige Korrekturen, um eine umfassende Dokumentation für die 510(k)-Einreichung zu gewährleisten. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.12 | Konsensstandard | Legen Sie eine Bestätigung der relevanten Konsensstandards und eine Erläuterung etwaiger Abweichungen von den von der FDA anerkannten Standards vor. | Fordern Sie die anwendbaren Konsensstandards bezüglich EMV und elektrischer Sicherheit für das aktive Gerät an. Dokumentieren Sie die bestätigten Konsensstandards für das aktive Gerät zum Zweck der 510(k)-Einreichung. |
| 2.13 | Kriterien für wesentliche Leistung und Störfestigkeit (Bestanden/Nicht bestanden) | Reichen Sie den Studienplan und die Berichte für die am aktiven Medizinprodukt durchgeführten Tests zur wesentlichen Leistung und Immunität ein, unter Einhaltung der von der FDA anerkannten Standards. | Reichen Sie eine Anforderung für den Studienplan und die Berichte der am aktiven Medizinprodukt durchgeführten Tests zur wesentlichen Leistung und Immunität ein, gemäß den von der FDA anerkannten Standards. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.14 | Konfiguration und getestete Funktionen des Medizinprodukts | Stellen Sie die Konfiguration und die getesteten Funktionen des aktiven Medizinprodukts bereit, einschließlich der folgenden Details: o Geben Sie eine umfassende Beschreibung des zu prüfenden Medizinprodukts an, einschließlich detaillierter Informationen zu seiner Konfiguration, Funktionen, Modi und den spezifischen Einstellungen, die getestet wurden. o Die Beschreibung des zu prüfenden Geräts sollte den Namen des Medizinprodukts, die Modellnummer und einen Hinweis darauf enthalten, ob es sich um das endgültige, produktionsreife Medizinprodukt handelt, das derzeit geprüft wird. | Reichen Sie eine Anfrage für die Konfiguration und Testfunktionen des aktiven Medizinprodukts ein. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
| 2.15 | Ergebnisse der EMV-Prüfung | Stellen Sie den Studienplan und Bericht zu EMV-Tests (elektromagnetische Verträglichkeit) bereit, gemäß dem von der FDA anerkannten Konsensstandard, der für das aktive Medizinprodukt empfohlen wird. | Stellen Sie einen formellen Antrag für den Studienplan und Bericht zu EMV-Tests, im Einklang mit dem von der FDA anerkannten Konsensstandard, der für aktive Medizinprodukte empfohlen wird. Überprüfen Sie gründlich und dokumentieren Sie sorgfältig alle notwendigen Informationen in Vorbereitung auf die 510(k)-Einreichung. |
Phase 3 – Erstdokumente und Dokumente zur wesentlichen Gleichwertigkeit | |||
|---|---|---|---|
Dokumentenanforderungen | Umfang des 510(k)-Antragstellers | Leistungsumfang von Freyr | |
| 3.1 | CDRH Deckblatt für die Einreichung zur Vorvermarktungsprüfung (FDA Form 3514) | - | Füllen Sie das FDA Form 3514 unter Verwendung der vom Antragsteller bereitgestellten Angaben aus. |
| 3.2 | Zusammenfassung und Zertifizierung für Klasse III | - | Dieser Schritt ist nicht erforderlich, wenn keine klinischen Studien benötigt werden. |
| 3.3 | Finanzielle Bestätigung oder Offenlegungserklärung | - | Dieser Schritt ist nicht erforderlich, wenn keine klinischen Studien benötigt werden. |
| 3.4 | Zusammenfassung für die Geschäftsleitung | - | Entwickeln Sie eine Vorlage und bereiten Sie das Dokument sorgfältig vor. Legen Sie Begründungen für alle festgestellten Abweichungen zwischen dem vorgeschlagenen Produkt und dem Vergleichsprodukt vor. Wird eine vergleichende Studie zwischen dem vorgeschlagenen Produkt und dem Vergleichsprodukt gewählt, erstellen Sie eine Vorlage und bereiten Sie das entsprechende Dokument vor. |
| 3.5 | Diskussion zur wesentlichen Gleichwertigkeit | - | Entwickeln Sie eine Vorlage und bereiten Sie das Dokument sorgfältig vor. Wird eine vergleichende Studie zwischen dem vorgeschlagenen Produkt und dem Vergleichsprodukt gewählt, erstellen Sie eine Vorlage und bereiten Sie das entsprechende Dokument vor. |
Phase 4 – Administrative Dokumente | |||
|---|---|---|---|
Dokumentenanforderungen | Umfang des 510(k)-Antragstellers | Leistungsumfang von Freyr | |
| 4.1 | 510(k)-Anschreiben | Unterschreiben Sie das auf Firmenbriefpapier gedruckte Dokument und veranlassen Sie den Kurierversand einer gedruckten Kopie an das US-Büro. Stellen Sie eine digitale Kopie des unterzeichneten 510(k)-Anschreibens zur Aufnahme in die 510(k)-Dokumentation bereit. | Erstellen Sie eine umfassende Vorlage, die alle notwendigen Details für das Anschreiben enthält, und stellen Sie diese dem Antragsteller zur Verfügung. Weisen Sie den Antragsteller an, sein offizielles Briefpapier zu verwenden und sicherzustellen, dass das Anschreiben von einer autorisierten Person unterzeichnet ist. |
| 4.2 | Erklärung zur Richtigkeit und Genauigkeit | Stellen Sie sicher, dass das Dokument von der benannten Kontaktperson des Unternehmens unterzeichnet und entsprechend bereitgestellt wird. | Entwickeln Sie eine umfassende Vorlage, die alle notwendigen Inhalte für das Einreichungsdokument enthält. |
| 4.3 | Konformitätserklärungen und Zusammenfassender Bericht | Stellen Sie sicher, dass das Dokument von der benannten Kontaktperson des Unternehmens unterzeichnet und entsprechend bereitgestellt wird. | Entwickeln Sie eine umfassende Vorlage, um die erforderlichen Dokumente systematisch aufzulisten und vorzubereiten. |
| 4.4 | MDFUSC (FDA Form 3601) | Reichen Sie die erforderliche Zahlung bei der FDA ein, bevor Sie die 510(k)-Akte offiziell einreichen. | Erstellen Sie ein Deckblatt für die Benutzergebühr und eine eindeutige Persönliche Identifikationsnummer (PIN) speziell für die Einreichung des Medizinprodukts. |
Phase 5 – RTA-Checkliste und E-Kopie | |||
|---|---|---|---|
Dokumentenanforderungen | Umfang des 510(k)-Antragstellers | Leistungsumfang von Freyr | |
| 5.1 | RTA-Checkliste | Genehmigung der Überprüfung der RTA (Ready to Accept)-Checkliste, die bestätigt, dass alle Anforderungen erfolgreich erfüllt wurden. | Entwickeln Sie eine maßgeschneiderte RTA-Checklisten-Vorlage, die auf die spezifische Art der Einreichung zugeschnitten ist. Füllen Sie die Checkliste sorgfältig aus, indem Sie alle erforderlichen Felder gewissenhaft ausfüllen und sicherstellen, dass die genannten Dokumente ordnungsgemäß bei der FDA eingereicht und dem Antragsteller mitgeteilt werden. |
| 5.2 | E-Kopie | Genehmigung der Dokumentation im finalen Einreichungsordner, die deren Einhaltung aller notwendigen Anforderungen und Standards bestätigt. | Ordnen Sie die Abschnitte des Einreichungsordners gemäß den FDA-Leitlinien und teilen Sie diese umgehend dem Antragsteller mit. Wandeln Sie den Einreichungsordner in eine elektronische Kopie um, um einen bequemen Zugriff und eine einfache Überprüfung zu ermöglichen. Reichen Sie die elektronische Kopie der Einreichung beim benannten US-Vertreter ein. |
Registrierung von Medizinprodukten
- Umfassende regulatorische Strategie für die US FDA
- Identifizierung des Vergleichsprodukts
- Herstellung der wesentlichen Gleichwertigkeit mit dem Vergleichsprodukt
- Lückenanalyse zur Einhaltung der US FDA-Vorschriften
- Erstellung von 21 Abschnitten der 510(k) Technischen Dokumentation
- Veröffentlichung und Erstellung von eCopy
- Validierung und Einreichung von eCopy
- Koordinationsdienste für die Produktzulassung
- Bearbeitung der RTA-Antwort und Behebung von Mängeln
- Beratungsleistungen zur Behebung von Mängeln
- Produktlistung & FURLS-Datenbankpflege

- Wir haben zahlreiche 510(k)-Registrierungen in verschiedenen Produktkategorien durchgeführt.
- Expertenteam für die Erstellung von 510(k)-Einreichungen gemäß den Anforderungen der US FDA Premarket Notification (510(k)).
- Zusätzliche Unterstützung bei der Bearbeitung von 510(k)-Anfragen.
- Beratung zur geeigneten Art des 510(k) gemäß den Einreichungsanforderungen der US FDA für 510(k) für das Produkt
- Rechtzeitige Einreichung von Leistungen
- Auf dem neuesten Stand der neuen Änderungen der US FDA.

