Nahtlose Einhaltung der britischen Vorschriften und Registrierungsanforderungen für Medizinprodukte
Ausländische Hersteller müssen die britischen Medizinproduktevorschriften von 2002 (in der jeweils gültigen Fassung) einhalten. Alle Medizinprodukte und In-vitro-Diagnostika müssen MHRA dem Verkauf im Vereinigten Königreich bei der MHRA registriert werden. Hersteller mit Sitz außerhalb des Vereinigten Königreichs sind verpflichtet, eine im Vereinigten Königreich ansässige verantwortliche Person (UKRP) zu benennen, die sie vertritt. Die MHRA strenge Anforderungen an die Dokumentation, Kennzeichnung und Meldung von Sicherheitsvorfällen MHRA , um die Patientensicherheit und die Rückverfolgbarkeit der Produkte zu gewährleisten.
Die neuen Anforderungen, die im Ergebnis der Konsultation für das Vereinigte Königreich vorgeschlagen wurden, können hinsichtlich der UKCA-Kennzeichnung, der Datenanforderungen und der Erwartungen nach dem Inverkehrbringen komplex sein. Viele Unternehmen stehen vor Herausforderungen aufgrund unvollständiger technischer Unterlagen, unterschiedlicher Klassifizierungen von Medizinprodukten und begrenzter Vertrautheit mit dem „Device Online Registration System“ (DORS). Regulatorische Änderungen und sich weiterentwickelnde MHRA erschweren die Planung und die Ressourcenzuweisung zusätzlich.
Freyr vereinfacht jeden Schritt Ihres Markteintritts in Großbritannien. Wir kümmern uns um die Einreichung von DORS-Anträgen, fungieren als Ihr UKRP, stellen sicher, dass alle Unterlagen vollständig sind, und schließen Compliance-Lücken während des Übergangs von CE zu UKCA. Unsere Regulierungsexperten begleiten Sie durch MHRA sich ändernden MHRA und helfen Ihnen dabei, einen konformen, zeitnahen und kosteneffizienten Marktzugang zu erreichen.
Schritt-für-Schritt-Anleitung zur Registrierung von Medizinprodukten im Vereinigten Königreich
Die Registrierung eines Medizinprodukts im Vereinigten Königreich umfasst mehrere festgelegte Schritte. So wickelt Freyr den gesamten Prozess für Sie ab:
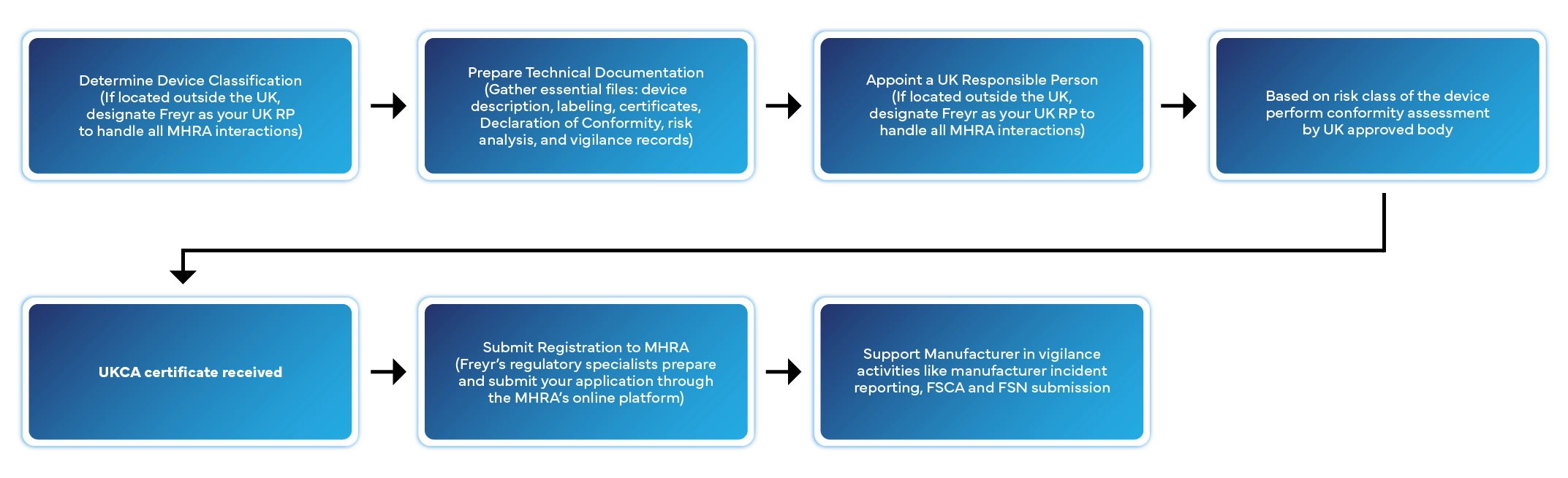
Übliche Bearbeitungszeit: 2–6 Wochen, abhängig von der Geräteklasse und der Vollständigkeit der Unterlagen.
Freyr Medical Device UK – Wichtigste Angebote
Produktregistrierung Freyr wickelt MHRA gesamte MHRA über die DORS-Plattform ab und gewährleistet damit vorschriftsmäßige Einreichungen, korrekte Daten und zeitnahe Genehmigungen für alle Produktkategorien.
Verantwortliche Person im Vereinigten Königreich Als Ihre benannte UKRP vertritt Freyr Sie gegenüber der MHRA, übernimmt die gesamte Kommunikation und gewährleistet die kontinuierliche Überwachung der Einhaltung der Vorschriften und der Vigilanz.
TF / Erstellung von Unterlagen Freyr erstellt technische Unterlagen und Dossiers, die den britischen Vorschriften für die UKCA-Kennzeichnung entsprechen, und stellt so sicher, dass das Unternehmen für Audits, Inspektionen und Einreichungen gerüstet ist.
Unterstützung beim Qualitätsmanagementsystem Wir unterstützen Sie bei der Einführung und Aufrechterhaltung von Qualitätsmanagementsystemen ISO 13485, die auf MHRA der britischen MDR und MHRA zugeschnitten sind.
Unterstützung bei der Erstellung von Zulassungsunterlagen Freyr bietet fachkundige Unterstützung bei der Erstellung von CERs, PMS-Plänen, PSURs und Risikomanagement-Unterlagen und gewährleistet dabei technische Klarheit und regulatorische Korrektheit.
Kennzeichnung und Einhaltung gesetzlicher Vorschriften Unser Team stellt sicher, dass Ihre Kennzeichnungen, Gebrauchsanweisungen und Verpackungen den UKCA-Anforderungen hinsichtlich Kennzeichnung und Sprache entsprechen, und gewährleistet dabei Einheitlichkeit und die Einhaltung der Vorschriften.
Überwachung nach dem Inverkehrbringen Freyr unterstützt Aktivitäten im Rahmen der Überwachung nach dem Inverkehrbringen, darunter die Meldung unerwünschter Ereignisse, Vigilanzberichte und MHRA , um den Marktzugang dauerhaft zu sichern.
Dienstleistungsangebot von Freyr UK Responsible Person (UKRP)
Freyr fungiert als Ihr benannter UKRP und gewährleistet die vollständige Einhaltung der britischen Medizinprodukteverordnung von 2002 (UK Medical Devices Regulations 2002) MHRA. Wir vertreten Ihr Unternehmen vor Ort im Vereinigten Königreich und übernehmen die gesamte Kommunikation mit der MHRA.
- Produktregistrierung bei MHRA
Freyr fungiert als Ihre benannte zuständige Person im Vereinigten Königreich (UKRP) und wickelt den gesamten MHRA über die DORS-Plattform ab, um sicherzustellen, dass jedes Produkt korrekt gelistet, verifiziert und für den Verkauf im Vereinigten Königreich zugelassen ist. - Dokumentation und Konformitätssicherung
Unsere Experten für regulatorische Angelegenheiten stellen sicher, dass Ihre Konformitätserklärung, die technische Dokumentation und die Produktzertifizierungen vorliegen, und bewahren eine Kopie auf, um die Unterlagen der MHRA auf Anfrage zur Verfügung stellen zu können. - Beantwortung von MHRA
Freyr übernimmt MHRA Ihrem Namen die gesamte Kommunikation und Klärung mit der MHRA und gewährleistet so zeitnahe und präzise Antworten auf behördliche Anfragen oder Überprüfungen nach dem Inverkehrbringen. - Wachsamkeit und Meldung von Zwischenfällen
Als Ihr UKRP fungiert Freyr als primäre Anlaufstelle für sicherheitsrelevante Angelegenheiten. Wir koordinieren den Austausch zwischen Herstellern, medizinischem Fachpersonal, Patienten und der MHRA unerwünschte Ereignisse und sorgen so für eine ordnungsgemäße Meldung sowie für Korrekturmaßnahmen.
zur Vorbereitung auf Inspektionen und Audits bei MHRA Freyr führt alle für MHRA und Audits MHRA erforderlichen Unterlagen und Korrespondenz. Unser Team stellt sicher, dass technische Unterlagen, Kennzeichnungen und Aufzeichnungen nach dem Inverkehrbringen jederzeit verfügbar sind.
Vereinbaren Sie noch heute einen Termin mit unseren Experten
Warum mit Freyr zusammenarbeiten?
- End-to-end Expertise, die von der Zulassung vor der Markteinführung bis hin zur Marktüberwachung nach der Markteinführung reicht und alle Phasen der Compliance abdeckt.
- Eine nachweisliche Erfolgsbilanz mit über 1500 erfolgreich abgeschlossenen Geräteregistrierungen in verschiedenen Kategorien.
- Lokale Präsenz in Großbritannien mit vor Ort ansässigen Regulierungsspezialisten in Reading, unterstützt durch globale Umsetzungsteams.
- Eine maßgeschneiderte Übergangsplanung, die strategische Unterstützung bietet, um reibungslos und kosteneffizient von CE auf UKCA umzustellen.
- Transparente Kommunikation durch direkten Kontakt mit MHRA proaktive Informationen zu Compliance-Themen für unsere Kunden.
- Weltweit führende Marken vertrauen auf Freyr, das mehr als 470 Hersteller weltweit als Partner in regulatorischen Fragen betreut.
Häufig gestellte Fragen (FAQs)
01. Wie läuft das Zulassungsverfahren für Medizinprodukte im Vereinigten Königreich ab?
Im Rahmen des britischen Registrierungsverfahrens für Medizinprodukte muss die MHRA Medicines and Healthcare products Regulatory Agency) über Ihr Produkt informiert werden, bevor es in Großbritannien in Verkehr gebracht wird. Hersteller müssen Unternehmensdaten, die Produktklassifizierung und die technische Dokumentation vorlegen. Hersteller mit Sitz außerhalb des Vereinigten Königreichs müssen zudem eine im Vereinigten Königreich ansässige verantwortliche Person (UK RP) benennen, die für die Registrierung und die laufende Kommunikation im Zusammenhang mit der Einhaltung der Vorschriften zuständig ist.
02. Wer muss eine für das Vereinigte Königreich zuständige Person (UK RP) benennen?
Jeder Hersteller mit Sitz außerhalb des Vereinigten Königreichs muss eine im Vereinigten Königreich ansässige verantwortliche Person benennen, bevor er Medizinprodukte auf dem britischen Markt in Verkehr bringt. Die im Vereinigten Königreich ansässige verantwortliche Person fungiert als Ansprechpartner des Herstellers in regulatorischen Angelegenheiten und stellt sicher, dass die gesamte technische Dokumentation, alle Erklärungen und MHRA ordnungsgemäß gepflegt werden. Hersteller mit Sitz im Vereinigten Königreich können MHRA eine im Vereinigten Königreich ansässige verantwortliche Person direkt mit der MHRA kommunizieren.
03. Welche Unterlagen sind für MHRA erforderlich?
Die MHRA wesentliche Unterlagen, darunter die Konformitätserklärung, die Produktbeschreibung und -klassifizierung, Angaben zum Hersteller sowie Informationen zur Kennzeichnung. Bei Produkten mit höherem Risiko können auch technische Unterlagen und klinische Nachweise geprüft werden. Eine vollständige, für Audits vorbereitete Dokumentation gewährleistet eine schnellere Zulassung und reibungslosere Nachmarktinspektionen durch die MHRA Bevollmächtigte.
04. Wie lange dauert das MHRA ?
In der Regel dauert MHRA 2 bis 6 Wochen, abhängig von der Produktklasse, der Vollständigkeit der Unterlagen und davon, ob eine für das Vereinigte Königreich zuständige Person beteiligt ist. Einfache Produkte der Klasse I können schneller bearbeitet werden, während komplexe oder risikoreichere Produkte aufgrund zusätzlicher Datenvalidierungen und Überprüfungen der technischen Dokumentation unter Umständen länger dauern können.
05. Was ist der Unterschied zwischen der CE-Kennzeichnung und der UKCA-Kennzeichnung?
Die CE-Kennzeichnung belegt die Einhaltung der Vorschriften der Europäischen Union, während die UKCA-Kennzeichnung (UK Conformity Assessed) für Produkte gilt, die in Großbritannien in Verkehr gebracht werden. Seit dem Brexit hat die UKCA-Kennzeichnung die CE-Kennzeichnung für den britischen Markt abgelöst, wobei die CE-Kennzeichnung vorübergehend weiterhin akzeptiert wird. Nordirland erkennt die CE-Kennzeichnung und die CE-UKNI-Kennzeichnung im Rahmen der EU-Angleichungsvorschriften weiterhin an.
06. Welche Verpflichtungen bestehen nach der Zulassung?
Nach der Registrierung müssen Hersteller und im Vereinigten Königreich ansässige Verantwortliche eine Marktüberwachung durchführen, unerwünschte Ereignisse melden, MHRA Änderungen MHRA Produkten oder Kennzeichnungen informieren und die Registrierungen bei Bedarf erneuern. Außerdem müssen sie die technische Dokumentation mindestens 10 Jahre lang aufbewahren. Diese Maßnahmen gewährleisten die kontinuierliche Einhaltung der Vorschriften und schützen die Gesundheit der Patienten während des gesamten Lebenszyklus des Produkts.
07. Wie oft sollten die MHRA aktualisiert werden?
Die Registrierungsdaten sollten unverzüglich aktualisiert werden, sobald sich die Produktklassifizierung, die Kennzeichnung, der Herstellungsstandort oder die verantwortliche Stelle ändern. Die MHRA von der für das Vereinigte Königreich zuständigen Person oder dem Hersteller eine umgehende Aktualisierung, um die Richtigkeit der Marktdaten zu gewährleisten. Regelmäßige interne Audits tragen dazu bei, dass Ihre Daten stets auf dem neuesten Stand bleiben und den sich ändernden Vorschriften entsprechen.
08. Welche Sanktionen drohen bei Nichteinhaltung der MHRA ?
Die Nichteinhaltung der britischen Registrierungs- oder Post-Market-Anforderungen für Medizinprodukte kann zu behördlichen Verwarnungen, Produktrückrufen, Geldstrafen oder strafrechtlichen Verfolgungen führen. Die MHRA ist MHRA befugt, die Marktzulassung auszusetzen oder zu widerrufen. Durch proaktive Compliance und die Benennung einer qualifizierten britischen verantwortlichen Person können Hersteller Strafen vermeiden und die Marktkontinuität gewährleisten.
09. Wie vereinfacht Freyr die Zulassung von Medizinprodukten im Vereinigten Königreich?
Freyr bietet end-to-end – von der Übernahme der Rolle als Ihre für das Vereinigte Königreich zuständige Person (UKRP) bis hin zur Abwicklung MHRA , der technischen Dokumentation und der laufenden Compliance. Unsere erfahrenen Berater optimieren den Prozess, verkürzen die Genehmigungsfristen und tragen dazu bei, den kontinuierlichen Marktzugang sicherzustellen.













