
Übersicht zur Medizinprodukteregistrierung in Vietnam
Der vietnamesische Markt für Medizinprodukte nimmt Fahrt auf und ist derzeit einer der boomenden Sektoren des Landes. Medizinprodukte im Land werden vom Department of Medical Equipment and Health Works (DMEHW) unter dem Gesundheitsministerium reguliert. Ausländische Hersteller müssen einen lokalen bevollmächtigten Vertreter in Vietnam ernennen, der sie beim Registrierungsprozess für Medizinprodukte in Vietnam unterstützt.
Aufsichtsbehörde: Abteilung für Medizinprodukte und Gesundheitswesen (DMEHW)
Verordnung: Erlass Nr. 98/2021/ ND-CP
Bevollmächtigter Vertreter: Lokaler Bevollmächtigter in Vietnam
QMS-Anforderung: ISO 13485:2016
Bewertung technischer Daten: Abteilung für Medizinprodukte und Bauwesen (DMEC) des Gesundheitsministeriums
Anforderungen an die Kennzeichnung: Verordnung Nr. 111/2021
Einreichungsformat: Online- Bearbeitungszeiten: 15 - 60 Tage
Sprache: Englisch und Vietnamesisch
Klassifizierung von Medizinprodukten in Vietnam
Die Produkte werden in 4 Klassen (A, B, C und D) eingeteilt, die wiederum in zwei Gruppen unterteilt sind: Gruppe 1 (Klasse A) und Gruppe 2 (Klasse B, C und D). Eine offizielle Klassifizierung ist bei der Abteilung für Medizinprodukte und Gesundheitswesen (DMEHW) in Vietnam erhältlich.
| Gruppe | Klasse | Risiko |
|---|---|---|
Gruppe 1 | Klasse A | Geringes Risiko |
Gruppe 2 | Klasse B | Mittleres bis geringes Risiko |
Klasse C | Mittleres bis hohes Risiko | |
Klasse D | Hohes Risiko |
Lokaler Bevollmächtigter in Vietnam
Die Benennung eines zuverlässigen und kompetenten vietnamesischen Bevollmächtigten für ausländische Hersteller ist entscheidend, da dieser die vom Hersteller im Rahmen des Geräteverkaufs angebotenen Garantieleistungen übernehmen muss. Eine Übersetzung ins Vietnamesische ist für den Markteintritt in dieser Region unerlässlich, was sich in der Praxis als schwierig erweisen kann.
Freyr bietet regulatorische Unterstützung, die das gesamte Spektrum an Aktivitäten abdeckt, wie die Beschaffung der Freiverkaufs-Anerkennungsnummer, die für die behördliche Zulassung von Medizinprodukten benötigt wird. Wir bieten zudem sprachliche Fachunterstützung, um die regulatorische Perspektive der Übersetzung zu wahren. Wir kümmern uns um die Bedürfnisse der Kunden nach der Zulassung, um die Einhaltung der Vorschriften während des gesamten Produktlebenszyklus in Vietnam zu gewährleisten.
Registrierung von Medizinprodukten in Vietnam
Alle Produkte der Klassen A und B benötigen eine Marktzulassung (MA-Lizenz). Geräte der Klassen A und B werden einer schnellen administrativen Prüfung durch das Gesundheitsamt der Provinz unterzogen, in der der Registrierungsinhaber seinen Sitz hat.
Geräte der Klassen C und D müssen nun eine Marktzulassung (MA-Lizenz) beantragen. MA-Lizenzen bleiben auf unbestimmte Zeit gültig.
Prozessablauf
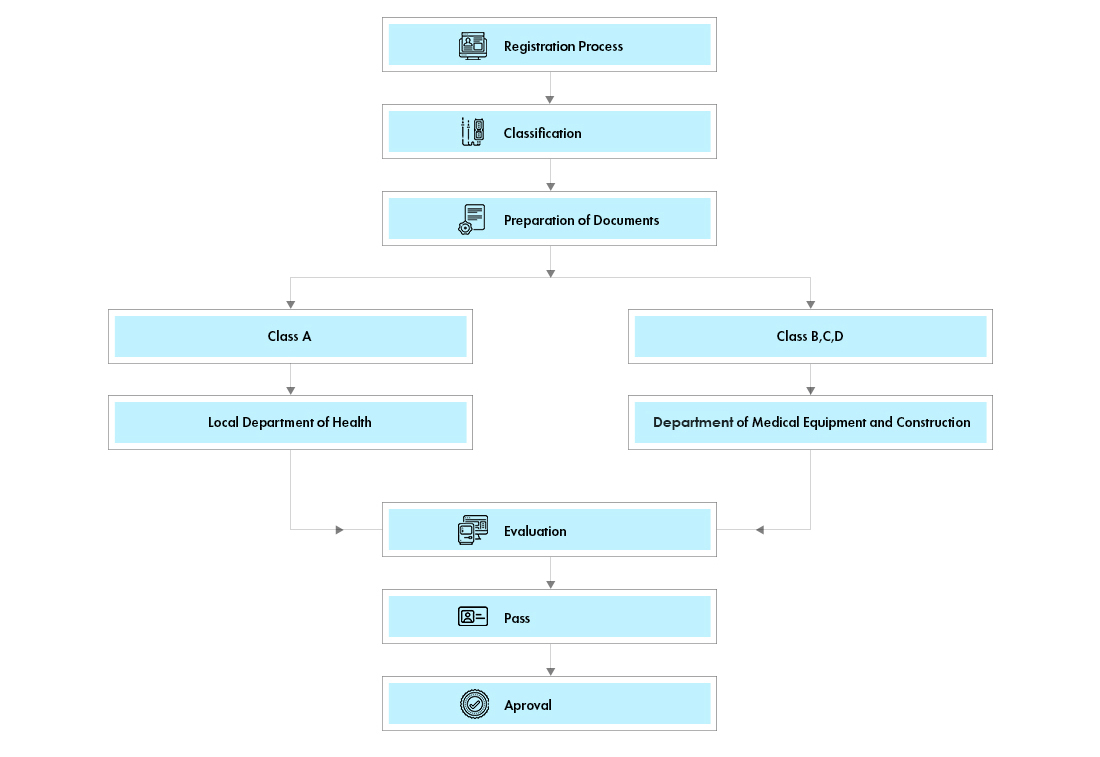
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel:
- Änderungsmanagement nach Genehmigung – Änderungen an bestehenden Medizinprodukte-Zulassungen, wie z. B. die Hinzufügung neuer Varianten, Zubehörteile; die Hinzufügung neuer Anwendungsindikationen und anderes mehr.
- Aufrechterhaltung von Genehmigungen und Registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren
- Verlängerung von Lizenzen
- Koordination zwischen der DMEHW und dem Hersteller
- Importmanagement
Zusammenfassung
Gruppe | Klasse | Risiko | Regulatorischer Weg | Fristen | Gültigkeit |
|---|---|---|---|---|---|
Gruppe 1 | Klasse A | Geringes Risiko | Erklärung des anwendbaren Standards | 15 - 60 Tage | Unbegrenzt |
Gruppe 2 | Klasse B | Mittleres bis geringes Risiko | Bescheinigung über die Registrierung für den freien Verkauf | 15 - 60 Tage | 5 Jahre |
Klasse C | Mittleres bis hohes Risiko | Bescheinigung über die Registrierung für den freien Verkauf | 15 - 60 Tage | 5 Jahre | |
Klasse D | Hohes Risiko | Bescheinigung über die Registrierung für den freien Verkauf | 15 - 60 Tage | 5 Jahre |
Freyr Expertise
- Regulatorische Due-Diligence
- Offizielle Klassifizierung
- Registrierung von Medizinprodukten
- Importgenehmigung
- Kennzeichnungsunterstützung
- Übersetzungsunterstützung
- Identifizierung und Qualifizierung von Vertriebspartnern
- Marktüberwachung nach dem Inverkehrbringen
- Änderungsmanagement nach der Zulassung
- Lizenzverlängerung und -übertragung
- Einreichung und Koordination
- Zollabfertigung


