Übersicht zur Medizinprodukte-Registrierung in Argentinien
Argentinien ist eines der sich schnell entwickelnden Länder in Lateinamerika, das Chancen für Medizinprodukteunternehmen mit einem Gesundheitssystem bietet, das für sein Engagement für Patientensicherheit und hochwertige medizinische Dienstleistungen bekannt ist. Die Registrierung von Medizinprodukten in Argentinien wird von der Regulierungsbehörde – der Nationalen Verwaltung für Arzneimittel, Lebensmittel und Medizinprodukte (ANMAT) – überwacht.

Zulassungsbehörde: Nationale Behörde für Arzneimittel, Lebensmittel und Medizinprodukte (ANMAT)
Vorschriften: Verfügung 2318/2002 und Verfügung 727/2013
Regulatorischer Weg: Elektronisches webgestütztes System zur Meldung von Medizinprodukten (WAND)
Bevollmächtigter Vertreter: Argentinischer Bevollmächtigter (AAR)
QMS-Anforderung: ISO 13485 (ANMAT MDS) und MDSAP (Affiliate Member)
Bewertung technischer Daten: Nationale Behörde für Arzneimittel, Lebensmittel und Medizinprodukte (ANMAT)
Kennzeichnungspflichten: Anhang III.B der Verfügung 2318/2002 und Anhang V der Verfügung 727/2013.
Einreichungsformat: Elektronisch (HELENA-Portal)
Sprache: Spanisch
Klassifizierung von Medizinprodukten in Argentinien
Im Regulierungsprozess der ANMAT ist der erste Schritt zur Bestimmung des Registrierungswegs und der Einhaltung der argentinischen Vorschriften die Ermittlung der Klassifizierung des Medizinprodukts. In Argentinien werden Medizinprodukte je nach Risiko in vier (04) Klassen eingeteilt (Klasse I-IV).
| Medizinprodukteklasse | Kriterien |
|---|---|
| Klasse I | Geringes Risiko |
| Klasse II | Geringes bis mittleres Risiko |
| Klasse III | Hohes bis mittleres Risiko |
| Klasse IV | Hohes Risiko |
| IVD-Klasse | Kriterien |
|---|---|
| Klasse A | Diagnose von nicht-infektiösen oder nicht übertragbaren Krankheiten. |
| Klasse B | Diagnose von Infektionskrankheiten, außer denen der Klasse C. |
| Klasse C | Diagnose sexuell übertragbarer Infektionskrankheiten oder durch Blut oder dessen Derivate übertragener Krankheiten, sowie zur Bestimmung von Blutgruppen. |
| Klasse D | Zur Selbsttestung. |
Argentinischer Bevollmächtigter (AAR)
Der Registrierungsinhaber eines Medizinprodukts in Argentinien ist rechtlich für die Registrierung und Vermarktung des Geräts im Land verantwortlich. Dies kann der Hersteller des Geräts sein oder ein lokaler bevollmächtigter Vertreter (AAR) in Argentinien, der im Namen des Herstellers handelt.
Alle in Argentinien vermarkteten Medizinprodukte müssen bei der ANMAT registriert werden. Der Registrierungsprozess kann komplex und zeitaufwändig sein, daher wird ausländischen Herstellern oft empfohlen, einen AAR zu beauftragen, um sie zu unterstützen.
ANMAT Medizinprodukte-Registrierung
Der Registrierungsprozess für Medizinprodukte der ANMAT ähnelt den brasilianischen Notifizierungs- und Registrierungsprozessen, wobei der Umfang der für die Genehmigung erforderlichen Prüfung je nach Klassifizierung des Produkts (Klasse I, II, III und IV) zunimmt. Alle Hersteller von Medizinprodukten müssen auch die ANMAT-MDS einhalten, die Argentiniens Äquivalent zur BGMP ist und ebenfalls der ISO 13485:2016 entspricht.
Prozessablauf
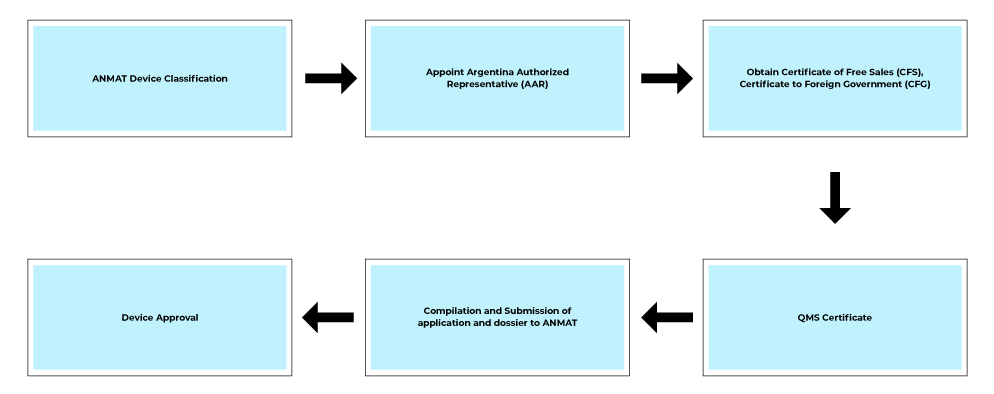
Dienstleistungen nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel –
- Änderungsmanagement nach der Zulassung – Änderungen an bestehenden Medizinproduktezulassungen, wie die Hinzufügung neuer Varianten, Zubehörteile und die Erweiterung um neue Anwendungsgebiete, unter anderem.
- Aufrechterhaltung von Zulassungen und Registrierungen durch fristgerechte Zahlung der Verwaltungs- und Registrierungsgebühren.
- Verlängerung von Lizenzen.
- Kommunikation zwischen ANMAT und dem Hersteller.
- Meldung unerwünschter Ereignisse.
- Importmanagement.
Freyr unterstützt Hersteller dabei, die Geräteklassifizierung als ersten Schritt zu identifizieren. Freyr hilft Kunden, den regulatorischen Weg zu finden und Zertifizierungen zu erhalten, indem es die damit verbundenen regulatorischen Hürden beseitigt. Mit bewährter Expertise bei der Einführung zahlreicher Geräte in der Region bietet Freyr End-to-End-Regulierungsdienstleistungen für Medizinprodukte.
Zusammenfassung
| Klasse der Medizinprodukte | Registrierungsweg (Meldung oder vollständige Registrierung) | Fristen der Gesundheitsbehörde | Gültigkeit der Registrierung (Jahre) |
|---|---|---|---|
| Geräte der Klasse I | Vollständige Registrierung | 4-6 Monate | 5 Jahre |
| Geräte der Klasse II | Vollständige Registrierung | 4-6 Monate | 5 Jahre |
| Klasse-III-Geräte | Vollständige Registrierung | 6-8 Monate | 5 Jahre |
| Geräte der Klasse IV | Vollständige Registrierung | 6-8 Monate | 5 Jahre |
*Bitte beachten Sie, dass Faktoren wie Bandbreitenbeschränkungen, regulatorische Aktualisierungen und andere Variablen zu Verlängerungen der Fristen der Gesundheitsbehörden führen können.
Freyr Expertise
- Dienstleistungen für Regulatory Intelligence Berichte.
- Dienstleistungen zur offiziellen Klassifizierung.
- Erstellung technischer Dokumente.
- Dienstleistungen zur Geräteregistrierung.
- Dienstleistungen als Autorisierter Vertreter in Argentinien (AAR).
- Importdienstleistungen.
- Betriebsgenehmigungen und Zulassungen.
- Übersetzungsdienstleistungen.
- Dienstleistungen für Kennzeichnung und Artwork.
- Dienstleistungen zur Identifizierung und Qualifizierung von Distributoren.
- Post-Market Surveillance.
- Dienstleistungen zur Lizenzverlängerung und -übertragung.
