Übersicht zur ägyptischen Medizinprodukte-Registrierung
Seit September 2018 ist die Registrierung von Medizinprodukten in Ägypten Pflicht. Die Medizinprodukteindustrie des Landes verzeichnete ein stetiges Wachstum und stellt einen attraktiven Markt für Hersteller und Händler dar. Mit einem Wert von 4,0 Milliarden US-Dollar im Jahr 2021 wird für den ägyptischen Markt für Medizinprodukte ein jährliches Wachstum (CAGR) von über 3 % von 2022 bis 2027 prognostiziert. Die Nachfrage nach Medizinprodukten in Ägypten wird angesichts der vergleichsweise geringen lokalen Produktion größtenteils durch Importe gedeckt. Bemerkenswerterweise ist der ägyptische Markt für Medizinprodukte der zweitgrößte in der Region Naher Osten und Nordafrika (MENA). Dieser Überblick beleuchtet wichtige Aspekte des ägyptischen Registrierungsprozesses und bietet Einblicke in den regulatorischen Rahmen und die Anforderungen, um innovative Medizinprodukte im ägyptischen Gesundheitssektor einzuführen.
Regulierungsbehörde: Egyptian Drug Authority (EDA)
Regulierung: Ägyptisches Medizinproduktegesetz Nr. 10 von 2003
Regulatorischer Weg: Produktregistrierung (Normal- und Schnellverfahren) und offizielle Klassifizierung
Lokaler bevollmächtigter Vertreter in Ägypten: Egyptian Registration Holder (ERH)
QMS-Anforderung: ISO 13485
Bewertung technischer Daten: Das Drug Policy and Planning Center (DPPC) und die Central Administration of Pharmaceutical Affairs (CAPA).
Gültigkeit der Lizenz: Zehn (10) Jahre
Einreichungsformat: Papier und Elektronisch
Übersetzung: Übersetzte Dokumente in Arabisch und Englisch
Geräteklassifizierung
In Ägypten richtet sich die Klassifizierung von Medizinprodukten nach dem europäischen Klassifizierungssystem, das Medizinprodukte nach ihrem Verwendungszweck und den potenziellen Risiken ihrer Anwendung einteilt. Hersteller sollten die korrekte Klassifizierung ihrer Produkte ermitteln, um die Einhaltung der regulatorischen Anforderungen sicherzustellen und die notwendigen Genehmigungen für die Vermarktung und den Vertrieb in Ägypten zu erhalten.
Medizinprodukteklassen
| Klasse | Risiko |
|---|---|
| Klasse I | Niedrig |
| Klasse II a | Niedrig bis Mittel |
| Klasse II b | Mittel-Hoch |
| Klasse III | Hoch |
Lokaler bevollmächtigter Vertreter in Ägypten
Medizinprodukteunternehmen mit Sitz außerhalb Ägyptens müssen einen lokalen Vertreter, den sogenannten „Egyptian Registration Holder (ERH)“, benennen, der die Einreichung von Registrierungsanträgen und Dossiers bei der EDA in ihrem Namen übernimmt. Der ERH fungiert als Bindeglied zwischen dem Hersteller und der Regulierungsbehörde, stellt die korrekte Erstellung und Einreichung aller erforderlichen Unterlagen sicher und überprüft, ob das Medizinprodukt die Sicherheits-, Qualitäts- und Wirksamkeitsstandards der EDA erfüllt. Darüber hinaus ist der ERH für die Aufbewahrung der Registrierungsdokumente, die Meldung von Vorkommnissen oder Rückrufen sowie die kontinuierliche Einhaltung aller geltenden Standards und Vorschriften während des gesamten Produktlebenszyklus verantwortlich. Der Egyptian Registration Holder (ERH) ist vollumfänglich für die Sicherstellung der Registrierung eines Medizinprodukts bei der EDA verantwortlich, insbesondere innerhalb der Zentralverwaltung für Medizinprodukte. Diese Rolle umfasst die Sicherstellung der Konformität des Produkts mit den regulatorischen Anforderungen der EDA für die Vermarktung und den Vertrieb in Ägypten.
Registrierung von Medizinprodukten
Die Erlangung einer Marktzulassung für ein Medizinprodukt in Ägypten umfasst mehrere Schritte, darunter die Erstellung der erforderlichen Dokumentation, die Einreichung des Antrags bei der EDA, die Einhaltung der Klassifizierungs- und Qualitätssystemanforderungen, die Ernennung eines ERH bei Bedarf und die Erfüllung der Post-Market-Verpflichtungen. Der Registrierungsprozess ist entscheidend, um zu gewährleisten, dass Medizinprodukte den vorgeschriebenen Sicherheits-, Qualitäts- und Wirksamkeitsstandards entsprechen, die von der ägyptischen Regulierungsbehörde festgelegt wurden. Die erforderliche Dokumentation kann je nach gewähltem Registrierungsweg variieren, umfasst aber im Allgemeinen Folgendes:
- CE-Zertifikat (falls zutreffend).
- Freiverkäuflichkeitsbescheinigung (CFS).
- ISO 13485 Zertifizierung.
- Konformitätserklärung (DOC).
Prozessablauf
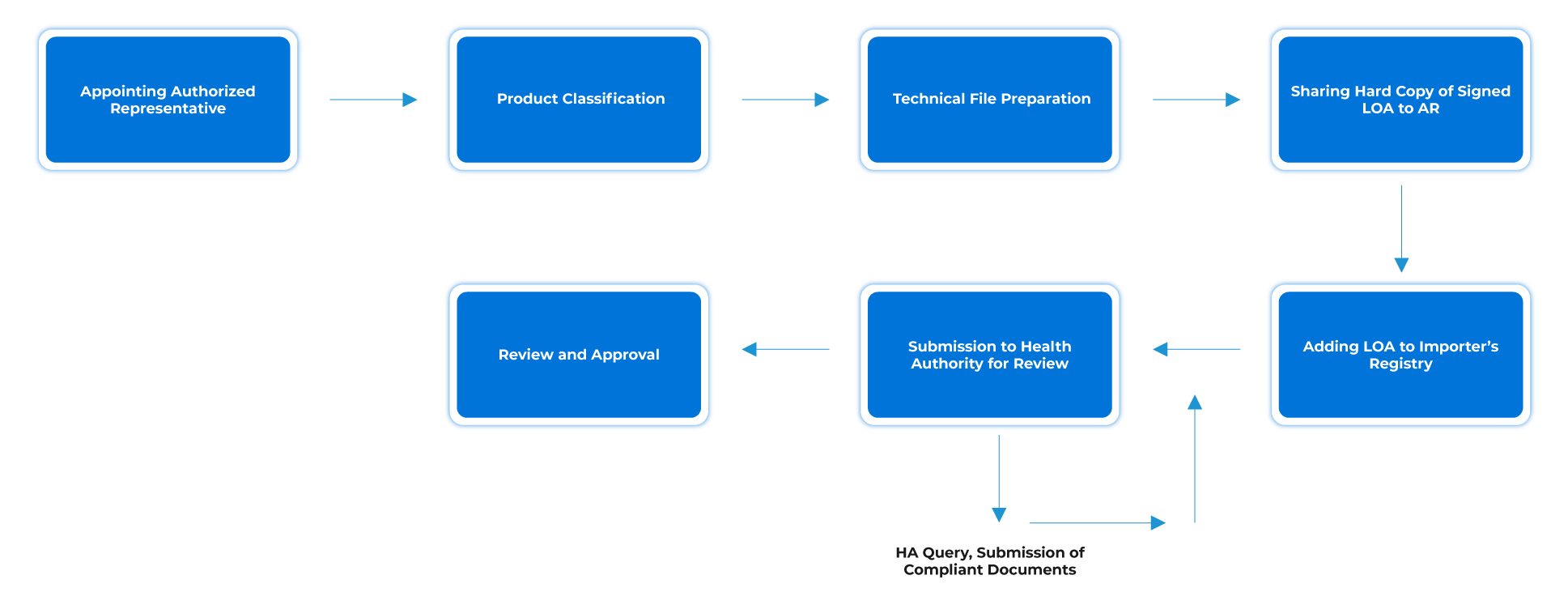
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr bietet ausländischen Herstellern umfassende Unterstützung bei der Verwaltung des gesamten Lebenszyklus von Medizinprodukten in Ägypten, einschließlich Aktivitäten nach der Zulassung:
- Verwaltung von Änderungen nach der Zulassung, die Anpassungen an bestehenden Medizinproduktezulassungen umfasst, zum Beispiel die Einführung neuer Varianten, Zubehörteile und Anwendungsgebiete.
- Wartung der ISO 13485:2016.
- CE-Zertifizierung.
- Als Vermittler zwischen der Benannten Stelle (NB) und dem Hersteller fungieren.
- Ein Vigilanzsystem ist eingerichtet, um die Sicherheit des Medizinprodukts zu überwachen, nachdem es die Marktzulassung erhalten hat.
- Regelmäßige Aktualisierungen bezüglich der Sicherheit und Wirksamkeit des Medizinprodukts sowie jegliche Änderungen des regulatorischen Status in anderen Rechtsräumen bereitstellen.
- Verlängerung der Marktzulassung nach einer bestimmten Frist, abhängig vom Gerätetyp und den Vorschriften.
Ein effektives Management der Post-Market Surveillance (PMS) in Ägypten erfordert ein geschicktes Navigieren durch die von der EDA festgelegten regulatorischen Rahmenbedingungen. Marktteilnehmer, die mit diesen komplexen Anforderungen zu kämpfen haben und keinen etablierten regulatorischen Partner besitzen, können die umfassenden regulatorischen Dienstleistungen von Freyr nutzen. Diese Dienstleistungen tragen zu einem reibungslosen Zulassungsprozess für Medizinprodukte in Ägypten bei und gewährleisten eine kontinuierliche Compliance mit der sich ständig weiterentwickelnden regulatorischen Landschaft und Marktdynamik.
Expertise bei der Medizinprodukte-Registrierung in Ägypten
- Regulatory Intelligence.
- Regulatory Due Diligence.
- Medizinprodukteklassifizierung.
- Geräteregistrierung.
- Ägyptischer Registrierungsinhaber.
- Übersetzungsunterstützung.
- Medizinisches Schreiben.
- Unterstützung bei der Kennzeichnung.
- Händleridentifizierung und -qualifizierung.
- Änderungsmanagement nach der Zulassung.
- Lizenzverlängerung und -übertragung.
- Zollabfertigung.

