
Übersicht zur Registrierung von Medizinprodukten in Taiwan
In Taiwan besteht eine wachsende Nachfrage nach Medizinprodukten. Die Taiwan Food & Drug Administration (TFDA) unter dem Ministerium für Gesundheit und Wohlfahrt (MOHW) reguliert Medizinprodukte durch das Arzneimittelgesetz (PAA). Ausländische Hersteller ohne physische Niederlassung in Taiwan benötigen eine Vertretung durch einen taiwanesischen Agenten als Voraussetzung für den taiwanesischen Registrierungsprozess für Medizinprodukte.
Aufsichtsbehörde: Taiwan Food and Drug Administration
Verordnung: Gesetz über pharmazeutische Angelegenheiten (PAA) & Verordnung zur Registrierung von Medizinprodukten
Bevollmächtigter Vertreter: Vertretung durch einen Taiwan-Beauftragten erforderlich
QMS-Anforderung: Qualitätssystemdokumentation (QSD) ISO 13485
Bewertung technischer Datena: Abteilung für Medizinprodukte & Kosmetika
Gültigkeit der Lizenz: QSD – 3 Jahre; Produktregistrierung – 5 Jahre
Kennzeichnungspflichten: Artikel 75, Gesetz über pharmazeutische Angelegenheiten
Einreichungsformat: Papier
Sprache: Englisch & Chinesisch
Klassifizierung von Medizinprodukten in Taiwan
Die TFDA klassifiziert Medizinprodukte in drei Risikoklassen: Klasse I für geringes Risiko, Klasse II für mittleres Risiko und Klasse III für hohes Risiko. Die Anforderung eines Referenzprodukts stellt eine Herausforderung für neuartige Geräte dar, um auf den Markt zu gelangen. Ein weiterer komplexer Aspekt ist der längere Verfahrenszeitraum für Geräte der Klassen II und III, die eine Dokumentation des Qualitätssystems erfordern. Alle importierten Medizinprodukte müssen ein Registrierungszertifikat von der TFDA erhalten.
| Geräteklasse | Risiko |
|---|---|
| Klasse I | Geringes Risiko |
| Klasse II | Mittleres Risiko |
| Klasse III | Hohes Risiko |
Vertretung durch einen Taiwan-Beauftragten
Ausländische Hersteller ohne physische Niederlassung in Taiwan müssen einen Taiwan-Beauftragten ernennen, um ihre Produkte in Taiwan vermarkten zu dürfen. Die Ernennung einer Drittorganisation als Taiwan-Beauftragten anstelle eines Vertriebspartners bietet die Flexibilität, mehrere Vertriebspartner für eine bessere Marktdurchdringung zu prüfen. Der Taiwan-Beauftragte muss eine in Taiwan ansässige juristische Person sein, die über eine Lizenz für den pharmazeutischen Vertrieb verfügt.
Registrierung von Medizinprodukten in Taiwan
Bevor ein Medizinprodukt in Taiwan verkauft werden kann, ist zusätzlich zur Registrierung des Medizinprodukts die Registrierung der Qualitätssystemdokumentation (QSD) für die Produktionsstätte erforderlich. Die QSD-Registrierung ist nur für Medizinprodukte der Klasse I (nicht steril) ausgesetzt. Eine QSD-Lizenz (erhalten nach Genehmigung der QSD-Registrierung) in Taiwan ähnelt der Guten Herstellungspraxis (GMP) für Medizinprodukte.
Die TFDA hat bekannt gegeben, dass Lizenzinhaber von Medizinprodukten der Klasse III ab dem 1. Juni 2022 verpflichtet sind, UDI und entsprechende Produktinformationen in die UDI-Datenbank (UDID) hochzuladen. Medizinproduktehersteller sind zudem verpflichtet, die UDI auf dem Produktetikett anzubringen. Darüber hinaus müssen Medizinprodukte der Klasse II ab dem 1. Juni 2023 die relevanten UDI-Vorschriften erfüllen.
Prozessablauf
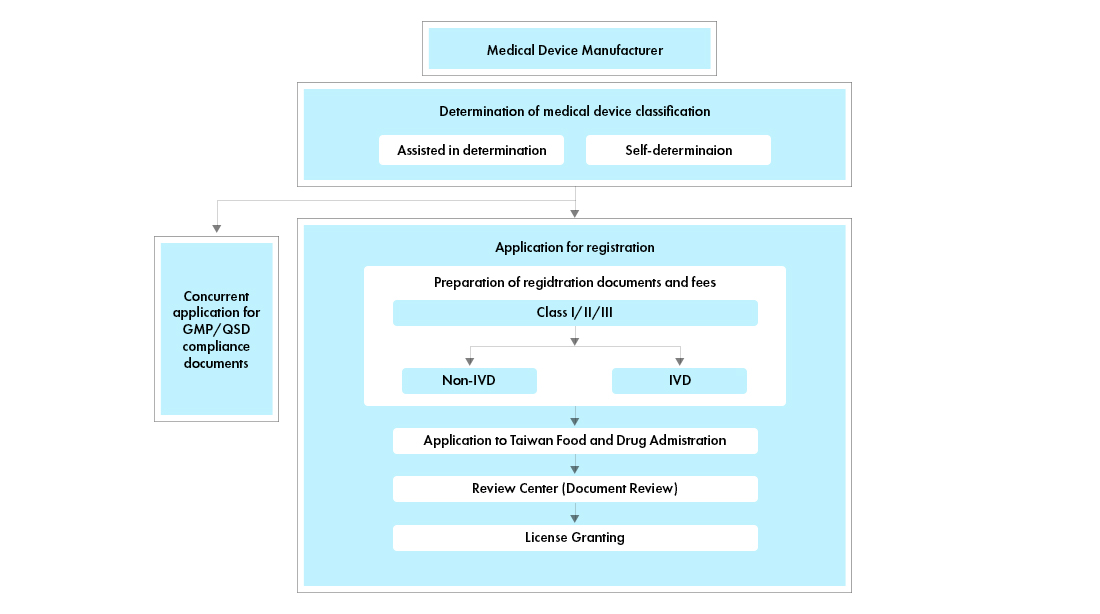
Lebenszyklusmanagement von Medizinprodukten nach der Zulassung
Freyr unterstützt ausländische Hersteller beim End-to-End Lebenszyklusmanagement von Medizinprodukten, einschließlich Aktivitäten nach der Zulassung, wie zum Beispiel:
- Änderungsmanagement nach Genehmigung – Änderungen an bestehenden Medizinprodukte-Zulassungen, wie z. B. die Hinzufügung neuer Varianten, Zubehörteile; die Hinzufügung neuer Anwendungsindikationen und anderes mehr.
- Aufrechterhaltung von Genehmigungen und Registrierungen durch fristgerechte Zahlung von Verwaltungs- und Registrierungsgebühren
- Verlängerung von Lizenzen
- Koordination zwischen der TFDA und dem Hersteller
- Importmanagement
Freyr ist spezialisiert auf die Erfüllung der regulatorischen Anforderungen für Medizinprodukte in Taiwan. Mit einem umfassenden Netzwerk hilft Freyr bei der Ernennung eines zuverlässigen lokalen Vertreters, dessen Präsenz während der gesamten Überwachung nach dem Inverkehrbringen von größter Bedeutung ist. Unsere Experten unterstützen auch bei der Auswahl eines geeigneten Referenzprodukts und bestehenden Zulassungen aus anderen Märkten, um den Markteintritt neuer Produkte zu unterstützen.
Zusammenfassung
| Geräteklasse | Risiko-/Klassifizierungskriterien | QMS | Produktregistrierung |
|---|---|---|---|
| Klasse I | Geringes Risiko | Ausgenommen (nicht-sterile Produkte der Klasse I) | Ja |
| Klasse II | Mittleres Risiko | QSD | Ja |
| Klasse III | Hohes Risiko | QSD | Ja |
Freyr Expertise
- Regulatorische Due-Diligence
- Offizielle Klassifizierung
- QSD-Zulassungen
- Registrierung von Medizinprodukten
- Rechtlicher Vertreter
- Kennzeichnungsunterstützung
- Übersetzungsunterstützung
- Identifizierung und Qualifizierung von Vertriebspartnern
- Marktüberwachung nach dem Inverkehrbringen
- Änderungsmanagement nach der Zulassung
- Lizenzverlängerung und -übertragung
- Einreichung und Koordination


