Zulassungsdienstleistungen für Arzneimittel in Chile – Überblick
Der chilenische Arzneimittelmarkt wird vom Instituto de Salud Pública de Chile (ISP) reguliert, das für die Zulassung, Registrierung und Überwachung von Arzneimitteln zuständig ist. Alle Arzneimittel müssen vor dem Verkauf registriert werden, um sicherzustellen, dass sie den in internationalen Richtlinien festgelegten Standards hinsichtlich Qualität, Sicherheit und Wirksamkeit entsprechen.
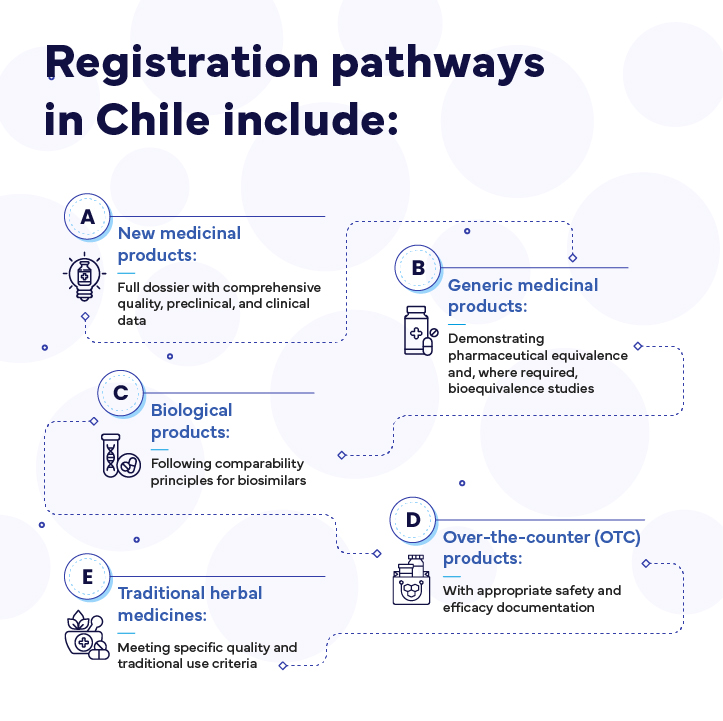
Zu den Zulassungsverfahren in Chile gehören:
Zu den wichtigsten Anforderungen zählen spanische Unterlagen, im Herkunftsland mit einer Apostille versehene Bescheinigungen, ein in Chile registrierter Inhaber sowie GMP-Konformitätsbescheinigungen. Für bestimmte Wirkstoffe, die vom ISP festgelegt werden, sind Bioäquivalenzstudien erforderlich.
Das regulatorische Umfeld erfordert Fachwissen in Bezug auf lokale Zulassungsverfahren, Dokumentation und Compliance. Ausländische Hersteller stehen vor komplexen administrativen Aufgaben und müssen gleichzeitig die Einhaltung der chilenischen Vorschriften zu Kennzeichnung, Pharmakovigilanz und Qualitätsstandards gewährleisten.
Freyr bietet Pharmaunternehmen, die eine Marktzulassung in Chile anstreben, umfassende Unterstützung in regulatorischen Fragen – von der strategischen Planung bis hin zum Management des Lebenszyklus nach der Zulassung.
Zulassungsdienstleistungen für Arzneimittel in Chile – Freyr Expertise
Registrierungsstrategie und Erstellung der Unterlagen
- Erstellung von Dossiers im CTD-Format für die Einreichung bei der ISP
- Bewertung des Zulassungsweges (Innovator, Generikum, Biosimilar)
- Regulierungsinformationen (RI) und Lückenanalyse
- Planung der Evidenz für Qualitäts-, präklinische und klinische Module
Vertretungsdienste vor Ort
- Dienstleistungen für Registrierungsinhaber mit Sitz in Chile
- Kontaktpflege zu Internetdienstanbietern und Verwaltung des offiziellen Schriftverkehrs
- Registrierung von Produktionsstätten und Dienstleistungen zur Einhaltung gesetzlicher Vorschriften
Dokumentation und administrative Unterstützung
- Verwaltung von Arzneimittelzertifikaten (CPP)
- Erstellung von GMP-Zertifikaten und Koordination der Apostille
- Übersetzung und Beglaubigung von behördlichen Dokumenten ins Spanische
- Erstellung und Beglaubigung von Vollmachten
Bioäquivalenz und Qualitätsdienstleistungen
- Planung und Überwachung von Bioäquivalenzstudien
- Erstellung von Begründungsunterlagen für Biowaiver
- Unterstützung bei der Validierung von Analysemethoden
- Entwicklung von Stabilitätsprotokollen und Datenauswertung
Einreichung und Lebenszyklusmanagement
- Elektronische Einreichung über ISP-Plattformen
- Bearbeitung von Anfragen und Mängelmanagement
- Änderungen nach der Zulassung (CMC, Kennzeichnung, administrative Änderungen usw.) und Ergänzungen
- Jährlicher Wartungs- und Erneuerungsservice
Compliance und Pharmakovigilanz
- Artwork der chilenischen Etikettierung und Artwork
- Einführung eines Pharmakovigilanz-Systems
- Verfahren zur Meldung unerwünschter Ereignisse (AE)
- Erstellung eines Risikomanagementplans (RMP)
Unser Standort in Chile
Av. Manquehue Nr. 151,
Büro 1205, Las Condes,
Chile

