MLR von Werbematerialien – Überblick
Erfolgreiche Produkteinführungen und ein effektiver Markteintritt für Arzneimittel oder Medizinprodukte hängen von der Synergie zwischen einer hochkompetenten Abteilung für Werbe- und Zulassungsangelegenheiten und einem soliden Prüfungsverfahren in den Bereichen Medizin, Recht und Zulassung (MLR) ab. Diese Synergie ist entscheidend für die vollständige Einhaltung der Vorschriften in Bezug auf Werbung, werbliche Kennzeichnung oder die Verbreitung nicht-werblicher Informationen im Bereich Medical Affairs.
Vermeidung irreführender Angaben, um die Patientensicherheit nicht zu gefährden, und Gewährleistung einer ethisch einwandfreien Verbreitung.
Minimieren Sie Risiken im Zusammenhang mit Verstößen, Mahnschreiben oder Strafen sowie Reputationsschäden.
Stellt sicher, dass Angaben zu Sicherheit, Wirksamkeit oder Leistungsfähigkeit des Produkts korrekt sind und durch wissenschaftliche Belege untermauert werden.
Übereinstimmung und Angleichung an die genehmigte Produktkennzeichnung und die Gebrauchsanweisung (IFU).
Einhaltung der von Aufsichtsbehörden festgelegten Richtlinien sowie der ethischen Verhaltenskodizes der Branche für verschiedene Länder und Regionen.
Bei Freyr bieten unsere Experten für Medizin und Zulassungsrecht mit ihrem beispiellosen klinischen und biomedizinischen Hintergrund, ihrer Kompetenz MLR sowie ihrer Erfahrung im Bereich Promotional Regulatory Affairs in über 120 Ländern rund um die Uhr Unterstützung, um die lückenlose Einhaltung der Vorschriften bei Ihren Markenwerbemaßnahmen, Anzeigen, Aufklärungskampagnen zu Krankheitsbildern oder markenunabhängigen Kampagnen sicherzustellen.
Dienste
- Bestätigung der Einhaltung länderspezifischer Richtlinien, die von Aufsichtsbehörden wie der FDA, EMA, EU MDR, MHRA, der TGA, HSA, PMDA, ANVISA, Health Canada und anderen festgelegt wurden.
- Bestätigung der Einhaltung länderspezifischer Richtlinien in Bezug auf Anti-Kickback-Gesetze und Branchen-Verhaltenskodizes wie FTC, PhRMA, EFPIA, ABPI, PAAB, TGA, Medicines New Zealand, ANVISA, ANAMED, IFPMA, AIFA, AEMPS, Mdeon und andere.
- Überprüfen Sie die korrekte Verwendung von Aussagen und Quellenangaben. Aussagen müssen durch relevante, geeignete Quellenangaben und wissenschaftliche Belege untermauert sein, und die Wirksamkeit oder Sicherheit darf nicht übertrieben dargestellt werden.
- Es ist darauf zu achten, dass bei der Darstellung der Risiken und Vorteile des Produkts, einschließlich etwaiger Nebenwirkungen oder Folgen der Anwendung, ein ausgewogenes Verhältnis gewahrt wird.
- Die Sprache, die Bildsprache und andere Elemente der Informationsdarstellung werden bewertet, um sicherzustellen, dass die Informationen für die Zielgruppen klar und präzise sind und keine irreführenden Angaben enthalten.
- Überprüfung der Übereinstimmung von Design- und Hintergrundelementen mit dem Inhalt, um Unstimmigkeiten zu vermeiden (z. B. Sicherstellung, dass Bilder von pädiatrischen Patientengruppen nicht in Zusammenhängen verwendet werden, in denen das Produkt nicht für diese Patientengruppe verschrieben wird).
- Richtigkeit der Marken- und Firmenzeichen, Dienstleistungsmarken sowie Konformitätsbescheinigungen für Geräte wie CE-Kennzeichnung, UKCA mark, CCC und andere.
- Bei Sitzungen der PRC als Fachexperten (SMEs) für regulatorische Angelegenheiten fungieren.
- Leitfaden für HA-Einreichungen, wie z. B. OPDP/APLP 2253 oder die HA-Prüfung von Werbematerialien.
- Einreichungen von Werbe- und Verkaufsförderungsmaterialien bei Gesundheitsbehörden, wie z. B.Form 2253 APLB Form 2253 der US FDA manuellen undFDA eCTD-Format.
Unser Team ist äußerst innovativ und in der Lage, Inhalte für jede Plattform und jeden Kanal zu entwickeln. Daher beschränken sich unsere Angebote und unser Fachwissen nicht auf die oben genannten Bereiche – wir können noch viel mehr!
- Überprüfen Sie die arzneimittelbezogenen Inhalte, einschließlich Indikationen, Dosierung, Anwendungshinweise und Wirkmechanismus, um deren Angemessenheit und Richtigkeit gemäß der zugelassenen Produktkennzeichnung, den Verschreibungsinformationen (PI), der Zusammenfassung der Merkmale des Arzneimittels ( SmPC, den Packungsbeilagen (PILs) und den Gebrauchsanweisungen (IFU) sicherzustellen, wobei diese durch geeignete klinische und wissenschaftliche Belege untermauert sein müssen.
- Bewertung der Übereinstimmung des Werbematerials mit aktuellen Behandlungsleitlinien und Versorgungsstandards innerhalb des spezifischen Therapiegebiets
- Anpassung der Prüfpunkte an die Therapiegebiete mit Leitlinien oder Vorschriften für Werbeaktivitäten, wie Onkologie oder seltene Krankheiten
- Sicherstellung eines „fairen Gleichgewichts“ zwischen der Darstellung von Risiken und Vorteilen im Werbematerial, wobei potenzielle Nachteile neben den Vorteilen genau widergespiegelt werden
- Klinische Studien und andere genaue, glaubwürdige wissenschaftliche Daten untermauern diese Behauptungen hinreichend.
- Stellen Sie sicher, dass die vergleichenden Aussagen zu anderen Produkten durch valide und zuverlässige Daten untermauert werden.
- Achten Sie darauf, dass medizinische Fachbegriffe und Synonyme sorgfältig ausgewählt werden, um eine klare Kommunikation zu gewährleisten.
- Stellen Sie sicher, dass die Materialien für die Zielgruppe geeignet sind (z. B. medizinisches Fachpersonal, Patienten, Pflegekräfte) und auf deren Verständnis und Bedürfnisse zugeschnitten sind.
- Arbeiten Sie mit funktionsübergreifenden Teams am länderbezogenen MLR (Global to Local) sowie an der aktuellen Szenariobewertung im Rahmen des Promotional Review Committee (PRC)-Prozesses zusammen, führen Sie Lückenanalysen durch und ermitteln Sie Bereiche, in denen Optimierungs- und Harmonisierungsbedarf besteht.
- Erstellung von Prozess-SOPs, Arbeitsanweisungen für MLR und KPIs zur Messung der Prozesseffizienz.
- Erfahrung in der Definition von MLR-Prozessabläufen für LCM-Systeme wie Veeva PromoMats MedComms.
- Unterstützung bei der MLR und dem PRC-Prozess für Anzeigen sowie werbliche und nicht-werbliche Materialien in LCM-Systemen wie Veeva PromoMats, Veeva MedComms, Pepperflow usw.
- Erstellung und Verteilung von Tagesordnungen an die Beteiligten, Teilnahme an Sitzungen des PRC sowie Protokollierung der Sitzungen und der vom PRC getroffenen Entscheidungen.
- Leiten Sie Werbe- und Informationsmaterialien zeitnah und nach Prioritäten an die Rezensenten weiter.
- Planung und Durchführung aller Besprechungen mit den Beteiligten zu Konzept, Vorabprüfung und Live-Überprüfung.
- Genehmigungen für die Überprüfung von Material nachverfolgen und sicherstellen, dass Änderungen korrekt umgesetzt werden.
- Stellt sicher, dass Werbe- und Promotionsmaterial die Kriterien für die Einreichung erfüllt.
MLR der Werbematerialien MLR
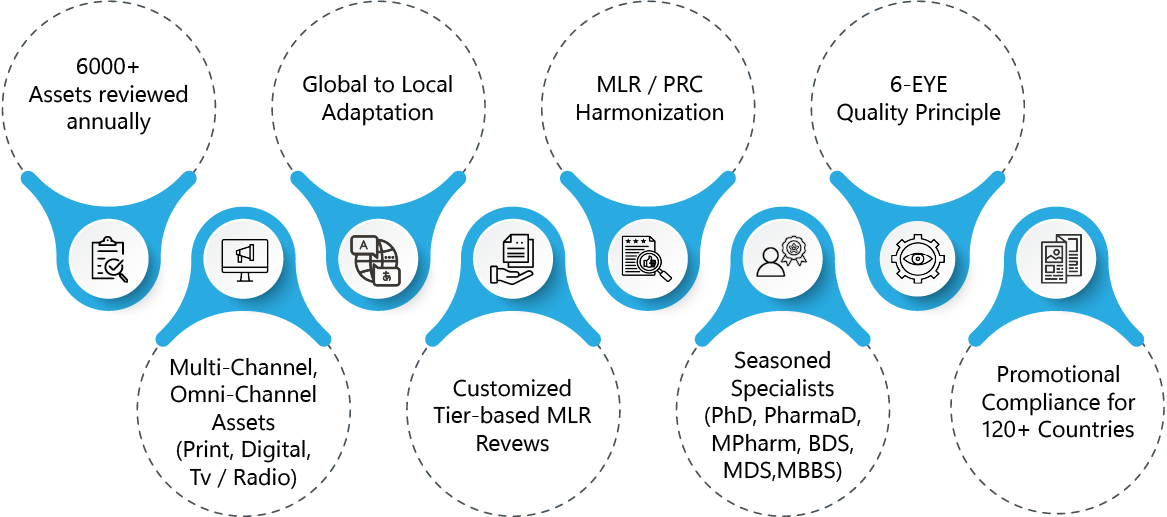
- Jährlich werden über 6000 Vermögenswerte auf MLR überprüft
- Erfahrung bei der Anpassung von Werbematerialien von der globalen auf die lokale Ebene sowie bei der Harmonisierung von MLR-Prozessen
- Das „6-Eye“-Qualitätsprinzip zur verbesserten Überprüfung der Einhaltung gesetzlicher Vorschriften, angepasst an die Komplexität des jeweiligen Therapiebereichs
- MLR – Fachkompetenz in einem breiten Spektrum an Werbe- und Nicht-Werbe-Materialien für verschiedene Kommunikationskanäle – Digital, Print, TV/Radio
- Maßgeschneiderte, auf der Komplexität der Vermögenswerte basierende, mehrstufige MLR
- Spezialisten für die Einhaltung von Werbevorschriften und MLR mit Branchenerfahrung und klinischem bzw. biomedizinischem Hintergrund (PharmaD, PhD, Mpharm, BDS, MDS, MBBS)
- Strategische, regionsspezifische Beratung zur Einhaltung der Vorschriften für Werbematerialien in über 120 Ländern.
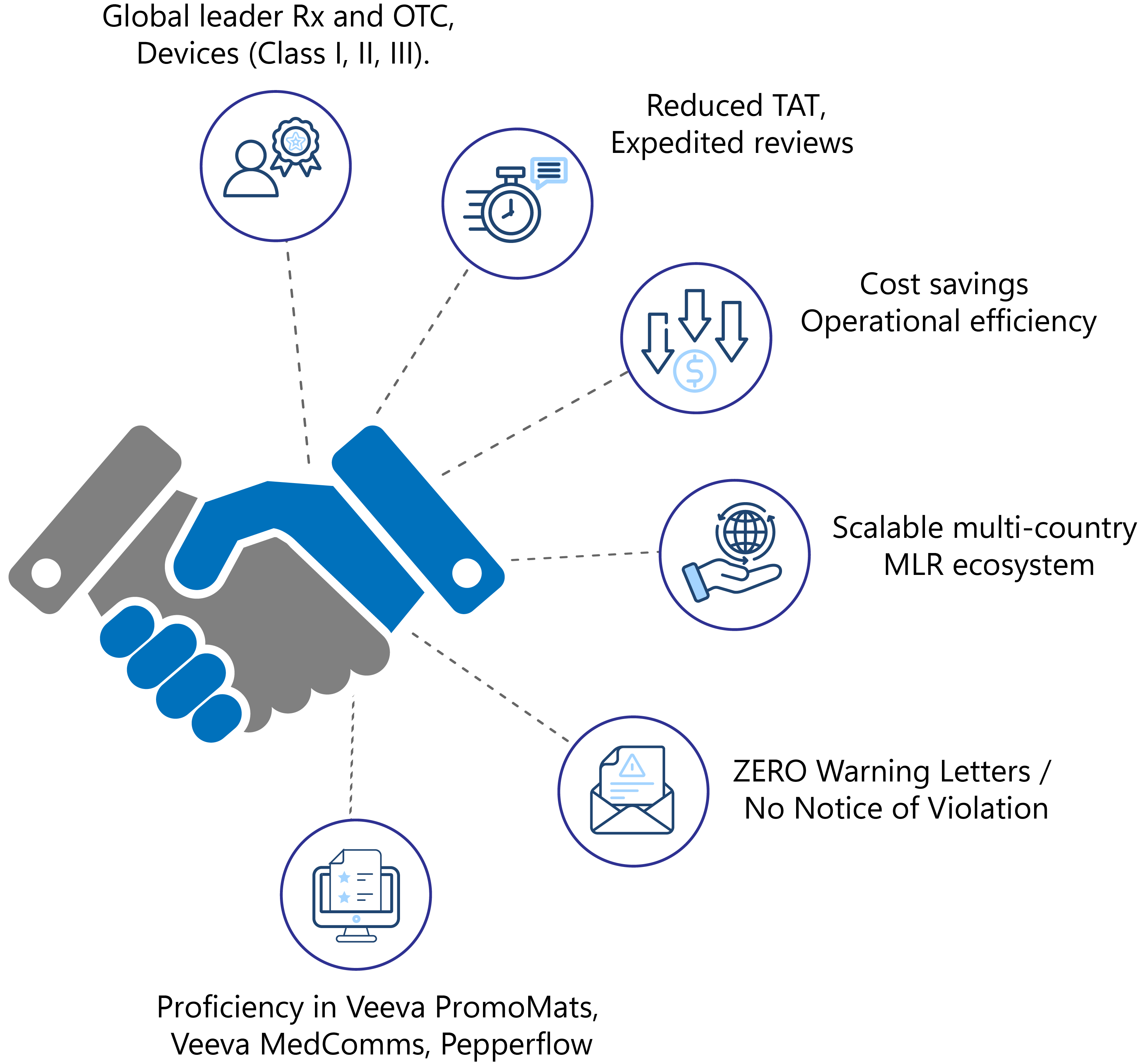
- Weltweit führend in den Bereichen Pharmazeutika, Biopharmazeutika (verschreibungspflichtige und OTC) sowie Medizinprodukte (Klasse I, II, III).
- Verkürzung der gesamten Durchlaufzeit für die Prüfung
- Reduzierte Durchlaufzeit durch beschleunigte Prüfungen zur Einhaltung von Fristen
- Erhebliche Kosteneinsparungen und verbesserte betriebliche Effizienz
- Skalierbares länderübergreifendes MLR-Ökosystem
- KEINE Abmahnungen/KEINE Mitteilungen über Verstöße
- Sicherer Umgang mit MLR -Systemen wie Veeva PromoMats, Veeva MedComms, Pepperflow usw.