Häufig gestellte Fragen
Regulatory Affairs (RA) in der Pharmaindustrie umfasst die Sicherstellung der Qualität, Sicherheit und Wirksamkeit von Arzneimitteln über deren gesamten Lebenszyklus hinweg. RA-Fachleute navigieren durch komplexe Anforderungen globaler Gesundheitsbehörden und gewährleisten die Einhaltung von Vorschriften von der Arzneimittelentdeckung bis zur Kommerzialisierung. Sie fungieren als Kommunikationsverbindung zwischen Pharmaunternehmen und weltweiten Zulassungsbehörden.
Der Hauptzweck der Regulierung in der Pharmaindustrie ist der Schutz der öffentlichen Gesundheit, indem sichergestellt wird, dass neue Medikamente sicher und wirksam sind, bevor sie auf den Markt kommen. Regulierungsbehörden setzen strenge Standards für Tests und Bewertungen durch, wodurch potenzielle Gesundheitsrisiken minimiert werden. Diese regulatorische Aufsicht schafft Vertrauen in die medizinischen Behandlungen, die der Öffentlichkeit zur Verfügung stehen.
Fachleute für Regulatory Affairs stellen sicher, dass pharmazeutische Produkte während ihres gesamten Lebenszyklus den regulatorischen Standards entsprechen. Sie sind an der Gestaltung klinischer Studien, der Marktzulassung und dem Management nach der Zulassung beteiligt, um die fortlaufende Einhaltung der Vorschriften zu gewährleisten und notwendige Produktänderungen zu erleichtern. Ihre Expertise hilft Unternehmen, sichere und wirksame Produkte effizient auf den Markt zu bringen.
Das Lebenszyklusmanagement in der Pharmaindustrie umfasst die Aufrechterhaltung der Lebensfähigkeit eines Produkts von der Entwicklung bis zur Nachzulassung. Es beinhaltet Strategien für die klinische Entwicklung, die Marktzulassung und die fortlaufende Einhaltung regulatorischer Standards. Ein effektives Lebenszyklusmanagement stellt sicher, dass das Produkt während seiner gesamten Marktpräsenz sicher und wirksam bleibt.
Die pharmazeutische Regulierung hat sich erheblich weiterentwickelt, von mittelalterlichen Arzneimittellisten bis hin zu modernen internationalen Harmonisierungsbemühungen. Wichtige Meilensteine sind der US Pure Food and Drugs Act von 1906 und die Gründung der International Conference on Harmonization (ICH) im Jahr 1990. Diese Entwicklungen haben die globalen Standards für Arzneimittelsicherheit und -wirksamkeit gestärkt.
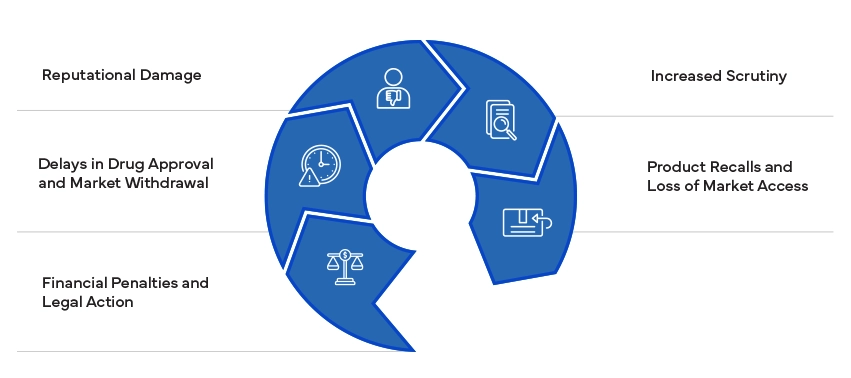
Die Nichteinhaltung regulatorischer Standards kann zu erheblichen Konsequenzen führen, darunter Geldstrafen, Rechtsstreitigkeiten und Produktrückrufe. Sie kann den Ruf eines Unternehmens schädigen und zu einer verstärkten Prüfung durch Regulierungsbehörden führen. Die Sicherstellung der Compliance ist unerlässlich, um diese Risiken zu vermeiden und den Marktzugang zu erhalten.
Freyr bietet umfassende regulatorische Lösungen und unterstützt Kunden von der frühen Entwicklungsphase bis zur Kommerzialisierung. Die Dienstleistungen umfassen die Erstellung von Dokumentationen für Gesundheitsbehörden, die Identifizierung regulatorischer Herausforderungen und die Beratung zu Post-Marketing-Strategien. Frey's Expertise hilft, die Produktentwicklung und Markteinführung zu beschleunigen.
Die globale regulatorische Harmonisierung zielt darauf ab, die Arzneimittelentwicklung und Registrierungsprozesse in verschiedenen Ländern zu optimieren. Sie minimiert Tierversuche und schützt die öffentliche Gesundheit, indem sie regulatorische Anforderungen international abstimmt. Diese Harmonisierung erleichtert die effiziente Einführung neuer Behandlungen auf globalen Märkten.
Zulassungsbehörden wie die FDA in den US und die EMA in der Europäischen Union setzen Standards durch, um die Sicherheit und Wirksamkeit von Arzneimitteln zu gewährleisten. Sie überwachen umfassende Test- und Bewertungsverfahren, bevor Arzneimittel auf den Markt gebracht werden können. Diese Behörden wägen den Bedarf an neuen Behandlungen mit der Minimierung potenzieller Gesundheitsrisiken ab.
Freyrs Global Regulatory intelligence Rahmen bietet aktuelle Informationen zu globalen Vorschriften und den Positionen der Gesundheitsbehörden. Dieser Rahmen wird in Kundenprojekte integriert, um den marktspezifischen Erfolg zu steigern. Er unterstützt die strategische Planung und die Einhaltung von Vorschriften in verschiedenen geografischen Regionen.