Pharma-Compliance-Audit- und Validierungsdienstleistungen
Nutzen Sie ein Jahrzehnt an Fachwissen mit unseren Dienstleistungen durch Compliance-Bewertungen, sorgfältige Audits und robuste Validierungsprozesse.
Themen entdecken
- Was ist Pharma-Compliance, Audit und Validierung?
- Welche Bedeutung haben Compliance, Audit und Validierung in der Pharmaindustrie?
- Wesentliche Herausforderungen im Bereich Compliance, Audit und Validierung.
- Was sind GxP-Audits?
- Fern-Audits verstehen
- Was ist Computer System Validation (CSV) und warum ist sie in der Pharmaindustrie so wichtig?
- Wie unterscheidet sich CSV von Computer System Assurance (CSA)?
- Welche Komponenten umfasst ein CSA-Programm?
- Wie trägt CSA zur Datenintegrität in der Pharmaindustrie bei?
- Welche Rolle spielt die Einhaltung gesetzlicher Vorschriften bei CSA?
- Wie hilft ein strategischer Partner für die Einhaltung gesetzlicher Vorschriften?
- Warum Freyr wählen?
- Unsere Dienstleistungen
Was ist Pharma-Compliance, Audit und Validierung?
Letzte Aktualisierung am: September 2024
Im pharmazeutischen Bereich sind Compliance-, Audit- und Validierungsprozesse unerlässlich, um die Einhaltung regulatorischer Standards, die Datenintegrität und die Herstellung sicherer, wirksamer Produkte zu gewährleisten. Compliance bedeutet die Abstimmung der Betriebsabläufe mit Branchenvorschriften und internen Richtlinien. Audits, als systematische Überprüfungen, verifizieren die Compliance, identifizieren Verbesserungsbereiche und mindern Risiken. Die Validierung gewährleistet, dass Systeme, Prozesse und Geräte die vordefinierten Anforderungen stets erfüllen.
Unternehmen suchen fachkundige Beratung, um sich nahtlos zu orientieren. Branchenführer bewältigen diese Prozesse gekonnt und gewährleisten die Einhaltung globaler Standards, ohne dabei die Wirksamkeit oder Sicherheit der Produkte zu beeinträchtigen. Im Zuge der Weiterentwicklung der Pharmabranche werden strategische Ansätze in den Bereichen Compliance, Audit und Validierung zu entscheidenden Faktoren für nachhaltigen Erfolg. Durch die Einhaltung dieser Prozesse erfüllen Unternehmen regulatorische Vorgaben und fördern eine Kultur der Exzellenz und Innovation in einer dynamischen und anspruchsvollen Branche.
Arbeiten Sie mit einem vertrauenswürdigen Partner zusammen, um strategische Beratung und maßgeschneiderte Lösungen zu erhalten, die Ihre pharmazeutischen Abläufe befähigen, in einem dynamischen regulatorischen Umfeld erfolgreich zu sein.

Welche Bedeutung haben Compliance, Audit und Validierung in der Pharmaindustrie?
Compliance, Audit und Validierung sind entscheidende Komponenten in der pharmazeutischen Industrie, die sicherstellen, dass Produkte sicher, wirksam und gemäß regulatorischen Standards hergestellt werden.
- Gewährleistet Produktsicherheit und -wirksamkeit: Die Einhaltung von Vorschriften stellt sicher, dass pharmazeutische Produkte strenge Sicherheits- und Wirksamkeitsstandards erfüllen, bevor sie auf den Markt kommen. Dies umfasst strenge Test- und Validierungsprozesse, um zu bestätigen, dass die Produkte wie vorgesehen funktionieren und keine Risiken für Patienten darstellen.
- Sicherstellung der Einhaltung regulatorischer Vorschriften: Regelmäßige Audits und Validierungen helfen Unternehmen, die komplexen und sich ständig ändernden Vorschriften der Gesundheitsbehörden einzuhalten. Dies umfasst die Einhaltung der Guten Herstellungspraxis (GMP), der Guten Klinischen Praxis (GCP) und anderer Industriestandards, wodurch das Risiko von regulatorischen Strafen und Produktrückrufen verringert wird.
- Verbessert die Qualitätssicherung: Validierungsprozesse, einschließlich der Validierung von Geräten und Systemen, stellen sicher, dass Herstellungs- und Testprozesse stets qualitativ hochwertige Produkte liefern. Audits überprüfen, ob diese Prozesse korrekt befolgt werden, was zu einer verbesserten Produktqualität und -zuverlässigkeit führt.
- Fördert den Marktzugang und stärkt das Ansehen: Wirksame Compliance- und Validierungsverfahren fördern den Marktzugang, indem sie die Einhaltung behördlicher Anforderungen nachweisen. Dies stärkt das Ansehen und die Glaubwürdigkeit des Unternehmens und schafft Vertrauen bei medizinischen Fachkräften, Patienten und Aufsichtsbehörden.
- Fördert kontinuierliche Verbesserung: Audits liefern Einblicke in Prozesseffizienzen und Verbesserungsbereiche, was zu einer besseren Qualitätskontrolle und operativen Praktiken führt. Diese fortlaufende Bewertung und Anpassung hilft, hohe Standards aufrechtzuerhalten und sich an Änderungen in Vorschriften und bewährten Branchenpraktiken anzupassen.
Wesentliche Herausforderungen im Bereich Compliance, Audit und Validierung.
Der Bereich Compliance, Audit und Validierung steht vor mehreren großen Herausforderungen, die die Fähigkeit pharmazeutischer Unternehmen beeinträchtigen können, regulatorische Anforderungen zu erfüllen und hohe Qualitäts- und Sicherheitsstandards aufrechtzuerhalten:
| Herausforderung | Beschreibung |
|---|---|
| Regulatorische Compliance | Pharmaunternehmen müssen strenge Vorschriften von Behörden wie der FDA und EMA einhalten, die eine rigorose Dokumentation und Qualitätskontrollmaßnahmen erfordern. Die Nichteinhaltung kann zu empfindlichen Strafen führen, einschließlich Bußgeldern und Produktrückrufen. |
| Zugangskontrolle und Sicherheit | Es ist entscheidend sicherzustellen, dass nur autorisiertes Personal Zugang zu sensiblen Bereichen und Informationen hat. Dies beinhaltet die Implementierung fortschrittlicher Zugangskontrollsysteme und die Aufrechterhaltung der Cybersicherheit gegen Bedrohungen, was komplex und kostspielig sein kann. |
| Computersystemvalidierung (CSV) | Die Validierung von Computersystemen, die in GxP-Umgebungen eingesetzt werden, ist unerlässlich, aber oft aufwendig und schlecht definiert. Der Prozess erfordert erhebliche Zeit und Ressourcen, insbesondere wenn ein Standardansatz wahllos angewendet wird. |
| Mitarbeiterschulung und -sensibilisierung | Kontinuierliche Schulungsprogramme sind notwendig, um sicherzustellen, dass Mitarbeiter die Compliance-Protokolle und deren Bedeutung verstehen. Unzureichende Schulungen können zu Nichteinhaltung und Fehlern in den Prozessen führen. |
| Dokumentation und Aktenführung | Die Pflege einer genauen und umfassenden Dokumentation ist für die Compliance unerlässlich. Unzureichende Dokumentation ist ein häufiges Problem, das zu regulatorischen Beanstandungen und Fehlern bei Audits führen kann. |
| Datenintegrität | Die Sicherstellung der Datenintegrität und -genauigkeit ist entscheidend, insbesondere bei der Verwaltung großer Informationsmengen. Herausforderungen sind unter anderem die manuelle Datenverarbeitung und der Bedarf an robusten Datenmanagementsystemen. |
| Lieferantenmanagement | Die Abhängigkeit von Drittanbietern für Software und Dienstleistungen erfordert eine gründliche Validierung und Compliance-Prüfung. Die Verwaltung dieser Beziehungen und die Sicherstellung, dass sie regulatorische Standards erfüllen, kann eine Herausforderung sein. |
| Technologische Komplexität | Die zunehmende Komplexität von Technologien, einschließlich KI und Cloud-based Systemen, stellt neue Validierungsherausforderungen dar und erfordert eine fortlaufende Anpassung an sich entwickelnde regulatorische Rahmenbedingungen. |
| Unzureichende Qualitätskontrolle | Viele Pharmaunternehmen haben Schwierigkeiten, hohe Qualitätsstandards über alle Prozesse hinweg aufrechtzuerhalten, was zu Kontamination, Kreuzkontamination und anderen Qualitätsproblemen führen kann. |
| Kontinuierliche Verbesserung und Überwachung | Regelmäßige Audits und Inspektionen sind unerlässlich, um Schwachstellen in Compliance-Systemen zu identifizieren. Viele Organisationen versäumen es jedoch, proaktive Maßnahmen zur kontinuierlichen Verbesserung umzusetzen. |
- Sich entwickelnde Vorschriften: Mit den sich schnell ändernden Vorschriften und Richtlinien in verschiedenen Regionen Schritt zu halten, kann eine Herausforderung sein. Pharmaunternehmen müssen ihre Compliance-Praktiken kontinuierlich aktualisieren, um neuen oder überarbeiteten regulatorischen Standards zu entsprechen, was erhebliche Ressourcen und Anpassungen erfordern kann.
- Komplexität globaler Standards: Die Navigation durch die vielfältigen und komplexen regulatorischen Anforderungen verschiedener Länder und Regionen erhöht die Herausforderung. Jede Gerichtsbarkeit kann ihre eigenen Regeln und Standards haben, was es schwierig macht, eine konsistente Compliance über globale Märkte hinweg zu erreichen.
- Datenintegrität und -sicherheit: Die Sicherstellung der Integrität und Sicherheit von Daten während der gesamten Compliance-, Audit- und Validierungsprozesse ist entscheidend. Unternehmen müssen robuste Systeme und Kontrollen implementieren, um sich vor Datenlecks, Manipulationen oder Ungenauigkeiten zu schützen, die schwerwiegende Folgen für die Produktzulassung und Patientensicherheit haben können.
- Ressourcenbeschränkungen: Begrenzte Ressourcen, einschließlich Zeit, Personal und Budget, können die Wirksamkeit von Compliance- und Audit-Aktivitäten beeinträchtigen. Unternehmen fällt es oft schwer, die Anforderungen der Compliance mit der Notwendigkeit abzuwägen, Ressourcen für andere kritische Geschäftsfunktionen bereitzustellen.
- Verwaltung von Dokumentation und Aufzeichnungen: Eine ordnungsgemäße Dokumentation und Aufbewahrung von Aufzeichnungen sind unerlässlich, um die Einhaltung von Vorschriften nachzuweisen und effektive Audits durchzuführen. Die Verwaltung großer Mengen an Dokumentation, die Sicherstellung ihrer Richtigkeit und die Aufrechterhaltung der Zugänglichkeit können jedoch eine Herausforderung darstellen, insbesondere in einem stark regulierten Umfeld.
- Integration neuer Technologien: Die Integration innovativer Technologien in bestehende Compliance- und Validierungsprozesse kann komplex sein. Während Technologien wie Automatisierung und KI (Künstliche Intelligenz) erhebliche Vorteile bieten, muss ihre Integration sorgfältig gehandhabt werden, um sicherzustellen, dass sie den regulatorischen Anforderungen entsprechen und keine neuen Risiken einführen.
- Schulung und Kompetenz: Es ist entscheidend, dass das Personal in Compliance-, Audit- und Validierungsprozessen ausreichend geschult und kompetent ist. Laufende Schulungsprogramme sind notwendig, um das Personal über regulatorische Änderungen und bewährte Verfahren auf dem Laufenden zu halten, was ressourcenintensiv sein kann.
- Behebung von Auditfeststellungen: Die effektive Behebung und Korrektur von Problemen, die bei Audits festgestellt werden, kann eine Herausforderung sein. Unternehmen müssen Korrektur- und Vorbeugemaßnahmen umgehend umsetzen und dabei sicherstellen, dass diese Maßnahmen den laufenden Betrieb nicht stören oder die Produktqualität beeinträchtigen.
- Balance zwischen Compliance und Innovation: Ein Gleichgewicht zwischen der Einhaltung strenger Vorschriften und dem Streben nach Innovation zu finden, kann schwierig sein. Unternehmen müssen sich in der regulatorischen Landschaft zurechtfinden und gleichzeitig neue Produkte und Technologien entwickeln und einführen.
- Sicherstellung der Konsistenz über alle Betriebsabläufe hinweg: Die Aufrechterhaltung der Konsistenz in Compliance-Praktiken und Validierungsprozessen über verschiedene Abteilungen, Standorte und Phasen des Produktlebenszyklus hinweg ist unerlässlich, aber herausfordernd. Unterschiede in den Praktiken können zu Nichteinhaltung und Qualitätsproblemen führen.
Was sind GxP-Audits?
Was ist ein unabhängiges GxP-Compliance-Audit und wer führt es durch?
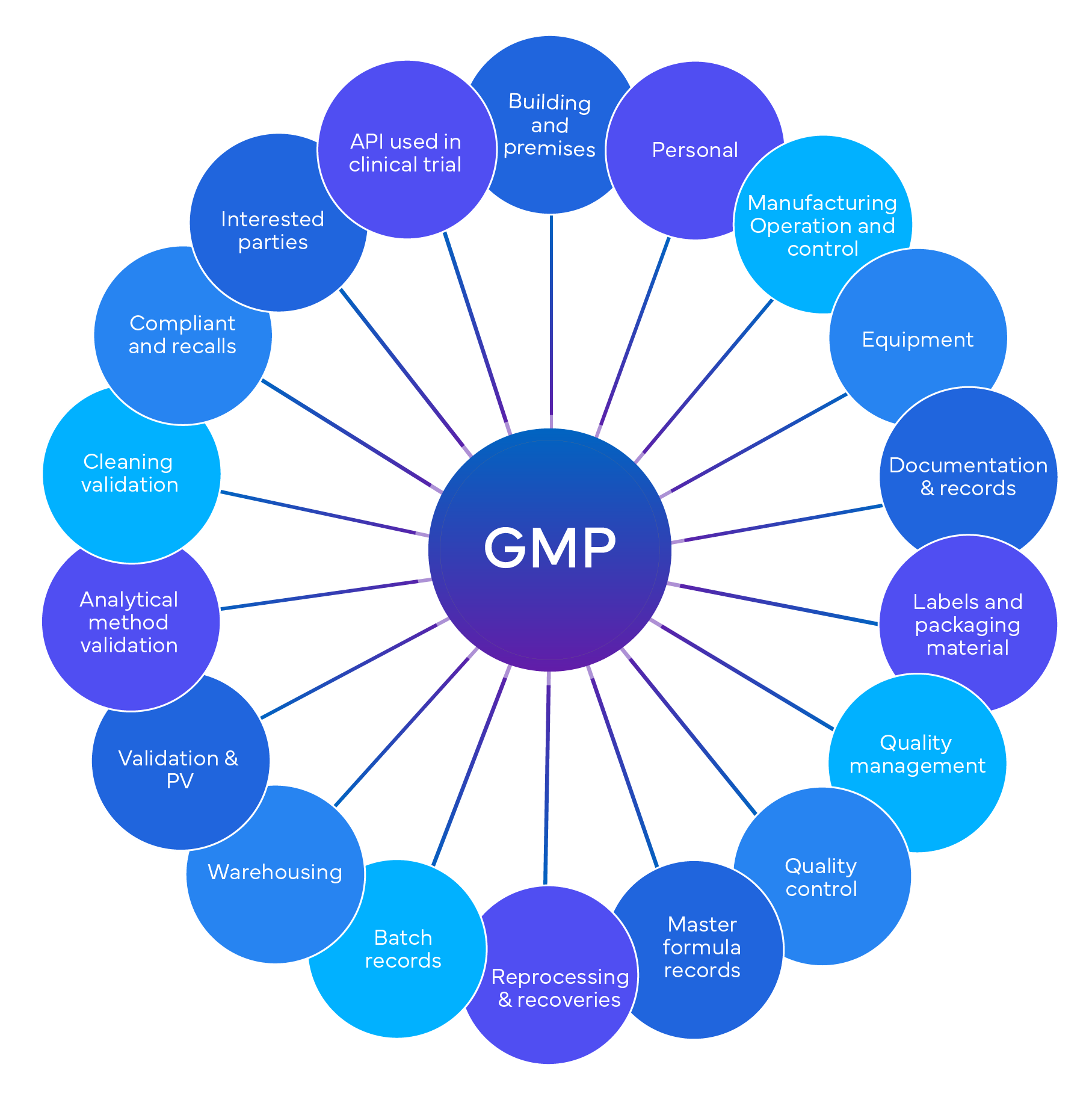
Ein GxP ist ein Verfahren, das entwickelt wurde, um sicherzustellen, dass Unternehmen vorgegebene Standards in Bezug auf Qualität, Sicherheit und die Einhaltung gesetzlicher Vorschriften einhalten. Es kann verschiedene Aspekte pharmazeutischer Produkte und Prozesse abdecken, wie beispielsweise die Gute Laborpraxis (GLP), die Gute klinische Praxis (GCP), die Gute Herstellungspraxis (GMP) und die Gute Pharmakovigilanzpraxis (GVP).
Im Rahmen des Audits wird die Einhaltung der geltenden Gesetze, Vorschriften, Richtlinien und Standardarbeitsanweisungen (SOPs) bewertet und es werden Lücken, Risiken und Verbesserungsmöglichkeiten ermittelt. Das Audit liefert zudem Empfehlungen und Korrekturmaßnahmen, um die festgestellten Mängel zu beheben und die Qualitätssysteme zu verbessern.
Die Vorteile eines GxP-Audits umfassen:
- Bereitstellung einer unvoreingenommenen und objektiven Bewertung der Qualitätssysteme und des Compliance-Niveaus.
- Stärkung des Vertrauens der Aufsichtsbehörden, Kunden, Lieferanten und anderer Interessengruppen.
- Verringerung der Wahrscheinlichkeit und Schwere von regulatorischen Inspektionen, Beobachtungen und Sanktionen.
- Verbesserung der Qualität, Sicherheit und Wirksamkeit von Produkten und Prozessen.
- Steigerung der Effizienz und Effektivität der Betriebsabläufe sowie Senkung von Kosten und Fehlern.
- Unterstützung der kontinuierlichen Verbesserung und Innovation von Produkten und Prozessen.
Ein GxP-Audit wird von einem qualifizierten und erfahrenen Auditor oder einem Team von Auditoren mit relevantem Wissen, Fähigkeiten und Qualifikationen in der pharmazeutischen Industrie und dem spezifischen GxP-Bereich durchgeführt. Der Auditor oder das Auditteam sollte unabhängig von dem zu auditierenden Unternehmen sein und die professionellen Standards und ethischen Grundsätze der Auditierung befolgen. Sie sollten auch geeignete Werkzeuge und Methoden zur Durchführung des Audits verwenden, wie z. B. Checklisten, Interviews, Beobachtungen, Dokumentenprüfungen, Stichproben, Tests usw. Freyr bietet End-to-End-Unterstützung bei GxP-Audits. Als Branchenführer werden unsere Experten Ihren Weg zur Compliance reibungslos gestalten.
Regulatorischer Rahmen für GxP-Audits
GxP-Konformität bezeichnet eine Reihe von Vorschriften, die verschiedene regulierte Branchen wie die Pharma-, Medizinprodukte-, Lebensmittel-, Getränke- und Biotechnologieindustrie betreffen. Das Hauptziel der GxP-Konformität ist es, die Produktqualität zu sichern und die öffentliche Sicherheit zu gewährleisten. Hier sind einige wichtige Punkte:
- Übersicht zur GxP-Konformität:
- GxP umfasst mehrere Standards, darunter die Gute Laborpraxis (GLP), die Gute Klinische Praxis (GCP), die Gute Herstellungspraxis (GMP) und die Gute Pharmakovigilanz-Praxis (GVP).
- Diese Standards stellen sicher, dass Produkte während ihres gesamten Lebenszyklus gründlich getestet, hergestellt und gehandhabt werden.
- Internationale Konferenz zur Harmonisierung (ICH):
- Die ICH stellt Leitlinien für die GxP-Konformität bereit.
- Der ICH Q7A Leitfaden zur Guten Herstellungspraxis befasst sich speziell mit den Herstellungspraktiken für aktive pharmazeutische Wirkstoffe (APIs).
- FDA-Inspektionen:
- Die US FDA (U.S. Food and Drug Administration) führt Inspektionen durch, um die Einhaltung der GxP-Vorschriften zu bewerten.
- Diese Inspektionen bewerten die Einhaltung spezifischer FDA-Vorschriften und -Richtlinien.
- Health Canada-Inspektionen:
- Health Canada, die Regulierungsbehörde in Kanada, führt auch Inspektionen durch, um die GxP-Konformität sicherzustellen.
- Diese Inspektionen konzentrieren sich auf verschiedene Aspekte, einschließlich Herstellung, Qualitätskontrolle und Vertrieb.
- Bewertungskriterien für GxP-Audits:
Die Compliance bei unabhängigen GxP-Audits wird typischerweise anhand einer Reihe von Kriterien bewertet, die Folgendes umfassen können:
- Regulatorische Anforderungen: Einhaltung spezifischer Vorschriften, Richtlinien und Gesetze, die für den GxP-Bereich gelten (z. B. FDA-Vorschriften, ICH-Richtlinien oder ISO-Standards).
- Qualitätssysteme: Bewertung von Qualitätsmanagementsystemen, Dokumentationspraktiken und Aufzeichnungen.
- Prozessvalidierung: Überprüfung, dass Prozesse validiert sind und vordefinierte Kriterien erfüllen.
- Schulung und Kompetenz: Bewertung der Schulung und Qualifikationen des Personals.
- Risikomanagement: Identifizierung und Minderung von Risiken in Bezug auf Produktqualität und -sicherheit.
Erfahren Sie, wie ein erfahrener Regulierungsexperte Sie dabei unterstützen kann, den passenden GxP-Auditrahmen für Ihre Anforderungen zu entwickeln und die weltweiten Vorschriften einzuhalten.
Vorteile der Durchführung von GxP-Compliance-Audits
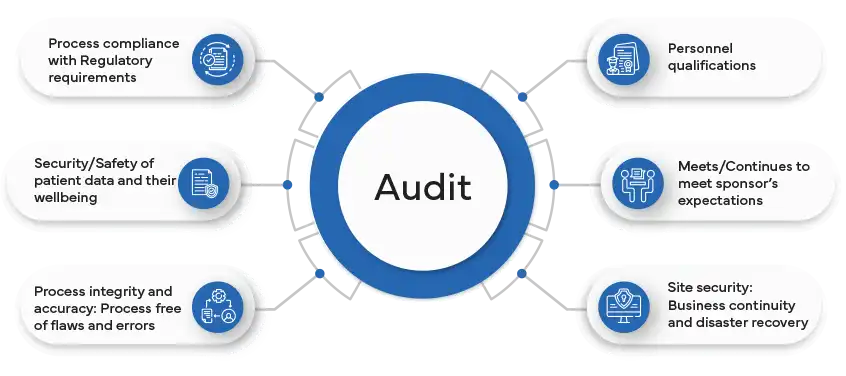
GxP-Audits bieten jeder Organisation zahlreiche Vorteile. Erstens ermöglichen sie eine unparteiische und unabhängige Bewertung von Risiken und der Einhaltung von Vorschriften innerhalb des Unternehmens. Dadurch können Firmen Bereiche der Nichteinhaltung oder potenzielle Risiken erkennen, die bei internen Audits möglicherweise übersehen wurden. Diese Audits sind entscheidend, um sicherzustellen, dass Unternehmen bestimmte Standards für Qualität, Sicherheit und die Einhaltung regulatorischer Anforderungen erfüllen.
| Aspekt | Beschreibung |
|---|---|
| Umfassende Überprüfung | Gründliche Bewertung durch einen qualifizierten Dritten zur Identifizierung von Bereichen der Nichteinhaltung. |
| Regulatorische Standards | Einhaltung der GxP-Standards (Gute-Praxis-Standards) wie GMP, GCP und GLP. |
| Maßgeschneiderter Umfang | Angepasster Audit-Umfang basierend auf spezifischen Produkten und Prozessen. |
| Qualifizierte Auditoren | Erfahrene Auditoren, vertraut mit Vorschriften. |
| Regulierungsrahmen | Folgt den ICH Q7A-, FDA- und Health Canada-Richtlinien. |
| Vorteile | Unabhängige Bewertungen, Risikoprävention, Qualitätssicherung und Skalierbarkeit. |
Hier sind einige wichtige Punkte zu GxP-Compliance-Audits:
- Umfassende Überprüfung: GxP-Audits umfassen einen gründlichen Überprüfungsprozess, der von einer qualifizierten Drittorganisation oder einem Berater durchgeführt wird. Ziel ist es, Bereiche der Nichteinhaltung innerhalb der Organisation zu identifizieren und Empfehlungen zur Verbesserung zu geben.
- Regulatorische Standards: Die bei diesen Audits überprüften Vorschriften werden durch GxP-Standards (gute Praktiken) definiert, wie Good Manufacturing Practices (GMP), Good Clinical Practices (GCP) und Good Laboratory Practices (GLP). Diese Standards stellen sicher, dass Produkte, Dienstleistungen und Prozesse stets die relevanten regulatorischen Anforderungen erfüllen.
- Maßgeschneiderter Umfang: Der Umfang eines unabhängigen Audits wird an die spezifischen Produkte und Prozesse der Organisation angepasst. Er kann Personalmanagement, Facility Management, Aufzeichnungen, Qualitätssicherung und -kontrolle, Produkt- und Prozessdesign sowie technische Operationen umfassen.
- Qualifizierte Auditoren: Das Audit muss von einem qualifizierten und erfahrenen Auditor durchgeführt werden, der mit den geltenden Vorschriften vertraut ist und über die notwendige Expertise verfügt, um die Verfahren und Prozesse der Organisation effektiv zu bewerten.
- Regulatorischer Rahmen: GxP-Audits folgen Rahmenwerken wie der International Conference on Harmonization (ICH) Q7A Good Manufacturing Practice Guidance, FDA-Inspektionen und Health Canada-Inspektionen. Diese Rahmenwerke bieten Leitlinien für grundlegende Anforderungen an Produktion, Qualitätssicherung, Distribution und andere kritische Aktivitäten im Zusammenhang mit der sicheren Produktherstellung.
- Vorteile: GxP-Audits bieten unparteiische Bewertungen, helfen, Nichteinhaltung zu verhindern, Qualitätsstandards aufrechtzuerhalten und Rechenschaftspflicht sicherzustellen. Das Outsourcing dieser Audits bietet Zugang zu Fachwissen, Objektivität, Kosteneffizienz und Skalierbarkeit, während Unternehmen sich auf ihre Kernkompetenzen konzentrieren können.
Wenn Sie nach GxP-Compliance-Lösungen suchen, ziehen Sie Freyr in Betracht. Wir sind spezialisiert auf regulatorische Compliance, Qualitätssicherung und Sicherheit in der gesamten Life-Sciences-Branche. Mit unserer Expertise können Sie die Einhaltung von GxP-Standards sicherstellen, Prozesse optimieren und qualitativ hochwertige Produkte und Dienstleistungen aufrechterhalten.
Tipps zur Vorbereitung Ihrer Organisation auf ein Audit
Die Vorbereitung Ihrer Organisation auf ein Audit ist ein strategischer Prozess, der eine sorgfältige Planung und einen proaktiven Ansatz erfordert. Stellen Sie zunächst sicher, dass alle Aufzeichnungen, Dokumentationen und relevanten Dateien organisiert und leicht zugänglich sind. Ein gut organisiertes Ablagesystem erleichtert einen reibungsloseren Auditprozess und wirkt sich positiv auf die Professionalität Ihrer Organisation aus.
Zweitens führen Sie ein internes Vorab-Audit durch, um potenzielle Problembereiche zu identifizieren. Diese Selbstbewertung ermöglicht es Ihnen, Probleme oder Abweichungen vor dem externen Audit zu beheben. Durch die proaktive Lösung von Problemen demonstrieren Sie Ihr Engagement für Compliance und Transparenz.
Drittens: Kommunizieren und arbeiten Sie effektiv mit dem Audit-Team zusammen. Stellen Sie die notwendigen Informationen, den Zugang zu relevantem Personal und ein förderliches Arbeitsumfeld bereit. Eine klare Kommunikation hilft, ein positives Verhältnis zu den Auditoren aufzubauen und fördert eine kooperative Atmosphäre während des Auditprozesses.
Schließlich stellen Sie sicher, dass Ihr Team gut geschult ist und den Auditprozess kennt. Klären Sie die Mitarbeiter über ihre Rollen, Verantwortlichkeiten und die Bedeutung der Compliance auf. Indem Sie eine Kultur der Vorbereitung und Zusammenarbeit etablieren, kann Ihr Unternehmen Audits mit Zuversicht und Professionalität meistern.
Fern-Audits verstehen
Was ist ein Remote-Audit in der pharmazeutischen Industrie und wie unterscheidet er sich von traditionellen Vor-Ort-Audits?
Ein Fernaudit in der pharmazeutischen Industrie ist eine umfassende Bewertung der Prozesse, Einrichtungen und Systeme eines Unternehmens, die von Aufsichtsbehörden oder Auditoren ohne physische Anwesenheit vor Ort durchgeführt wird. Dieses Audit wird durch digitale Kommunikationsmittel, Kollaborationssoftware und den Fernzugriff auf relevante Dokumente und Systeme ermöglicht. Es zielt darauf ab, die Einhaltung regulatorischer Standards sicherzustellen, Qualitätsmanagementsysteme zu bewerten und die Einhaltung der Guten Herstellungspraxis (GMP), der Guten klinischen Praxis (GCP) oder anderer geltender Vorschriften zu überprüfen.
Der Unterschied zwischen Remote- und traditionellen Vor-Ort-Audits liegt in der fehlenden physischen Präsenz während eines Remote-Audits. Anstatt die Räumlichkeiten des Unternehmens zu besuchen, verlassen sich Auditoren auf virtuelle Interaktionen, elektronische Dokumentation und Fernzugriff auf Systeme. Dieser Ansatz bietet Flexibilität und Effizienz, wodurch Audits unabhängig von geografischen Entfernungen und Reisebeschränkungen stattfinden können. Herausforderungen wie die eingeschränkte direkte Beobachtung von Einrichtungen und potenzielle Cybersicherheitsbedenken müssen jedoch angegangen werden, um die Effektivität von Remote-Audits zu gewährleisten.
Trotz der Unterschiede bleiben die Ziele sowohl von Remote- als auch von traditionellen Audits gleich: die Compliance zu verifizieren, Verbesserungsbereiche zu identifizieren und die Qualität und Sicherheit pharmazeutischer Produkte sicherzustellen. Die Wahl zwischen Remote- und Vor-Ort-Audits hängt von Faktoren wie der Art des Audits, den regulatorischen Anforderungen und den Fähigkeiten des Unternehmens ab, eine gründliche Bewertung mittels Remote-Methoden zu ermöglichen.
Freyr nutzt seine jahrzehntelange Expertise, um unübertroffene regulatorische Lösungen anzubieten und die Einhaltung von Vorschriften sowie den Erfolg in der dynamischen Pharmabranche sicherzustellen.
Entdecken Sie mit uns regulatorische Exzellenz – wir sind Ihr strategischer Partner für erfolgreiche Compliance in der sich ständig wandelnden Pharmaindustrie. Sprechen Sie uns an, um regulatorische Komplexitäten mühelos zu meistern.
Welche Herausforderungen können bei Remote-Audits auftreten und wie werden sie angegangen, um gründliche Bewertungen zu gewährleisten?
Bei Remote-Audits können verschiedene Herausforderungen auftreten, aber Organisationen können Maßnahmen ergreifen, um diese anzugehen und gründliche Bewertungen sicherzustellen. Hier sind einige zentrale Herausforderungen und ihre potenziellen Lösungen:
- Aufbau wichtiger Beziehungen zu Audit-Stakeholdern:
- Herausforderung: Remote-Arbeit kann den Aufbau starker Beziehungen zu Audit-Stakeholdern behindern.
- Lösung: Regelmäßige virtuelle Meetings, offene Kommunikation und aktives Engagement können helfen, Beziehungen aufzubauen und zu pflegen. Nutzen Sie Videoanrufe, um eine persönliche Verbindung herzustellen.
- Investition in Technologie für virtuelle Arbeit:
- Herausforderung: Remote-Audits sind stark von Technologie abhängig, und unzureichende Tools können die Effizienz beeinträchtigen.
- Lösung: Investieren Sie in robuste Audit-Management-Software, sichere Kommunikationsplattformen und Kollaborationstools. Stellen Sie sicher, dass Auditoren die notwendige Hard- und Software besitzen.
- Mitarbeiterentwicklung und Förderung einer positiven Unternehmenskultur aus der Ferne:
- Herausforderung: Remote-Arbeit kann zu Isolation führen und die berufliche Entwicklung behindern.
- Lösung: Bieten Sie virtuelle Schulungen, Mentoring und Möglichkeiten zur Kompetenzentwicklung an. Fördern Sie eine positive Kultur durch Teambuilding-Aktivitäten, Anerkennung und regelmäßige Gespräche.
- Entwicklung einer zielgerichteten und anpassungsfähigen Denkweise:
- Herausforderung: Remote-Auditoren müssen sich an veränderte Umstände anpassen und konzentriert bleiben.
- Lösung: Fördern Sie Flexibilität, Anpassungsfähigkeit und eine wachstumsorientierte Denkweise. Schulen Sie Auditoren darin, unerwartete Situationen zu bewältigen und ihren Ansatz bei Bedarf anzupassen.
Freyr ist ein vertrauenswürdiger Partner für regulatorische Compliance und Sicherheitslösungen in der Biowissenschaftsbranche. Mit fundiertem Fachwissen, innovativer Technologie und globaler Präsenz unterstützt Freyr Unternehmen dabei, komplexe regulatorische Rahmenbedingungen nahtlos zu bewältigen. Entdecken Sie unsere Dienstleistungen und kontaktieren Sie uns noch heute, um Ihre Compliance-Reise zu optimieren.
Wie kann Freyr Sie bei Ihren Remote-Audits optimal unterstützen?
Freyr verfügt über jahrzehntelange Expertise und ist führend bei der Durchführung nahtloser Remote-Audits für die Pharmaindustrie. Durch den Einsatz fortschrittlicher Technologien und ein tiefgreifendes Verständnis der regulatorischen Anforderungen gewährleistet Freyr einen gründlichen und effizienten Auditprozess, der Herausforderungen wie begrenzte physische Präsenz und Cybersicherheitsbedenken berücksichtigt.
Unser engagiertes Team von Regulierungsexperten ist versiert im Einsatz innovativer digitaler Lösungen und gewährleistet eine umfassende virtuelle Bewertung Ihrer Prozesse, Einrichtungen und Dokumentation. Unsere nachgewiesene Erfolgsbilanz bei Remote-Audits spiegelt unser Engagement wider, zuverlässige und effektive regulatorische Lösungen zu liefern, die auf die sich entwickelnden Bedürfnisse der Pharmalandschaft zugeschnitten sind. Mit Freyr gewinnen Sie einen vertrauenswürdigen Partner, der die Feinheiten von Remote-Audits versteht und einen proaktiven und kollaborativen Ansatz verfolgt, um Ihre Compliance-Reise zu optimieren.
Was ist Computer System Validation (CSV) und warum ist sie in der Pharmaindustrie so wichtig?
Computer System Validierung (CSV) ist ein kritischer Prozess in der pharmazeutischen Industrie, der die Integrität, Zuverlässigkeit und Compliance von computergestützten Systemen für verschiedene Zwecke gewährleistet. Lassen Sie uns die Details beleuchten:
- Definition und Zweck:
- CSV ist der dokumentierte Prozess, der sicherstellt, dass ein computergestütztes System Informationen oder Daten liefert, die vordefinierten Anforderungen entsprechen.
- Sein Hauptzweck ist es, zu validieren und zu verifizieren, dass Computersysteme konsistent wie beabsichtigt funktionieren und die Datenintegrität, Zuverlässigkeit und Sicherheit gewährleisten.
- Bedeutung in der Pharmabranche:
- Regulatorische Compliance: Die Pharmaindustrie unterliegt strengen Vorschriften (wie der Guten Herstellungspraxis oder GMP), um Produktqualität, Sicherheit und Wirksamkeit zu gewährleisten.
- Datenintegrität: Genaue und zuverlässige Daten sind entscheidend für die Arzneimittelentwicklung, klinische Studien, Herstellung und den Vertrieb.
- Risikominderung: CSV hilft dabei, Risiken im Zusammenhang mit Computersystemen zu erkennen und zu mindern, wodurch Fehler, Datenverlust und die Nichteinhaltung von Vorschriften verhindert werden.
- Patientensicherheit: Ordnungsgemäß validierte Systeme tragen zur Sicherheit der Patienten bei, indem sie eine gleichbleibende Qualität und die Einhaltung von Standards gewährleisten.
- Wichtige Aspekte von CSV:
- Anforderungsdefinition: Systemanforderungen, Funktionalitäten und Benutzererwartungen klar definieren.
- Design und Konfiguration: Das System gemäß den Spezifikationen entwickeln und konfigurieren.
- Test und Qualifizierung: Umfassende Tests (einschließlich Unit-Tests, Integrationstests und Benutzerakzeptanztests) zur Überprüfung der Systemleistung.
- Dokumentation: Umfassende Dokumentation über den gesamten Systemlebenszyklus hinweg pflegen.
- Änderungsmanagement: Änderungen am System verwalten und sicherstellen, dass dessen Integrität nicht beeinträchtigt wird.
- Herausforderungen, die durch CSV bewältigt werden:
- Datenintegrität: Unbefugten Zugriff, Datenkorruption oder -manipulation verhindern.
- Systemsicherheit: Vor Cyberbedrohungen und unbefugten Änderungen schützen.
- Audit-Trail: Einen unveränderlichen elektronischen Datenpfad für regulatorische Audits pflegen.
- Validierungspflege: Die Validierung regelmäßig überprüfen und aktualisieren, um sie an Systemänderungen anzupassen.
Worin unterscheidet sich CSV von Computer System Assurance (CSA)?
Computer System Validation (CSV) und Computer System Assurance (CSA) sind unterschiedliche Ansätze, um die Integrität und Konformität computergestützter Systeme in der pharmazeutischen Industrie sicherzustellen. CSV, eine langjährige Praxis, konzentriert sich hauptsächlich auf die Validierungsphase im Lebenszyklus eines Systems und stellt sicher, dass Softwaresysteme durch vordefinierte Protokolle die regulatorischen Anforderungen erfüllen. CSA hingegen verfolgt einen umfassenderen und dynamischeren Ansatz, der den gesamten Lebenszyklus eines computergestützten Systems abdeckt, von der Entwicklung und Implementierung über den operativen Einsatz bis zur endgültigen Außerbetriebnahme.
CSV begegnet dem Bedarf an strengen Validierungsprozessen und betont risikobasierte Ansätze zur Identifizierung und Minderung potenzieller Probleme. Die pharmazeutische Landschaft entwickelt sich jedoch weiter, was die Entstehung von CSA als umfassendere Strategie vorantreibt. CSA erweitert seinen Fokus über die Validierung hinaus, indem es agile Methoden anpasst und eine kontinuierliche Überwachung über den gesamten Lebenszyklus eines Systems integriert. Diese ganzheitliche Perspektive ermöglicht es Organisationen, Risiken proaktiv zu managen, insbesondere in den Bereichen Cybersicherheit und Datenintegrität, und stimmt mit dem wachsenden Fokus der Branche auf Technologie- und Datensicherheit überein.
Die Anpassungsfähigkeit von CSA ist in einem sich rasch wandelnden regulatorischen Umfeld von großem Wert. Während CSV an traditionellen Validierungsverfahren festhält, orientiert sich CSA an den sich wandelnden Erwartungen der Aufsichtsbehörden. Es geht über regelmäßige Revalidierungsmaßnahmen hinaus und umfasst kontinuierliche Überwachung, Echtzeit-Datenanalyse sowie proaktive Risikomanagementstrategien, um eine dauerhafte Compliance und optimale Leistung sicherzustellen. Da die Pharmaindustrie den digitalen Wandel vorantreibt, ist das Verständnis der Unterschiede zwischen CSV und CSA für Unternehmen, die in Bezug auf regulatorische Compliance und Systemintegrität die Nase vorn behalten wollen, unerlässlich.
In diesem Zusammenhang ist Freyr mit seiner umfassenden Erfahrung und Expertise bestens gerüstet, um Pharmaunternehmen durch die Feinheiten von sowohl CSV als auch CSA zu führen und maßgeschneiderte Lösungen anzubieten, die den sich entwickelnden Anforderungen der regulatorischen Compliance und des technologischen Fortschritts gerecht werden.
Welche Komponenten umfasst ein CSA-Programm?
Computer Software Assurance (CSA) ist ein moderner Ansatz, der die Zuverlässigkeit, Sicherheit und Konformität in computergestützten Systemen verbessert. Lassen Sie uns seine Komponenten und langfristigen Vorteile erkunden:
- Risikobasierter Ansatz:
- Komponente: CSA konzentriert sich auf Risikobewertung und -management.
- Bedeutung: Die Identifizierung kritischer Bereiche hilft, Validierungsbemühungen effektiv zu verteilen.
- Unskriptierte Tests:
- Komponente: CSA umfasst unskriptierte Tests, die über traditionelle skriptbasierte Testfälle hinausgehen.
- Bedeutung: Unskriptierte Tests ahmen reale Szenarien nach und decken verborgene Probleme auf.
- Kontinuierliche Leistungsüberwachung:
- Komponente: CSA beinhaltet eine kontinuierliche Überwachung der Systemleistung.
- Bedeutung: Das frühzeitige Erkennen von Anomalien verhindert Systemausfälle und Probleme mit der Datenintegrität.
- Datenaufsicht:
- Komponente: CSA legt Wert auf Datenqualität und -integrität.
- Bedeutung: Stellt genaue Daten für Entscheidungsfindung und Konformität sicher.
- Externe Validierungsaktivitäten:
- Komponente: CSA arbeitet mit Softwareanbietern für externe Validierung zusammen.
- Bedeutung: Unabhängige Validierung schafft Vertrauen und reduziert Voreingenommenheit.
- Übergang von CSV zu CSA:
- Erste Schritte:
- CSA-Prinzipien verstehen
- Bestehende Systeme auf Risiken bewerten
- Kritische Funktionalitäten priorisieren
- Vorteile:
- Reduzierter Validierungsaufwand
- Agile Reaktion auf Änderungen
- Verbesserte Systemzuverlässigkeit
- Erste Schritte:
- Langfristige Systemzuverlässigkeit:
- CSA gewährleistet:
- Anpassungsfähigkeit: Systeme entwickeln sich weiter, ohne die Zuverlässigkeit zu beeinträchtigen.
- Sicherheit: Schutz vor Cyberbedrohungen.
- Compliance: Kontinuierliche Ausrichtung an Vorschriften.
- Qualität: Konsistente Daten- und Produktqualität.
- CSA gewährleistet:
Wie trägt CSA zur Datenintegrität in der Pharmaindustrie bei?
CSA wahrt die Datenintegrität in der pharmazeutischen Industrie, indem es Genauigkeit, Konsistenz und Datenzuverlässigkeit über den gesamten Lebenszyklus eines Systems hinweg sicherstellt. Im Gegensatz zu traditionellen Ansätzen verfolgt CSA eine ganzheitliche Strategie, die über die Validierung hinausgeht und potenzielle Herausforderungen und Abweichungen, die im Laufe der Zeit auftreten können, aktiv angeht.
Ein Beitrag von CSA zur Datenintegrität liegt in seinen kontinuierlichen Überwachungsfunktionen. Anstatt sich ausschließlich auf periodische Validierungsbemühungen zu verlassen, umfasst CSA Echtzeit-Datenanalysen und proaktive Risikomanagementmaßnahmen. Dieser Ansatz ermöglicht es Organisationen, potenzielle Datenabweichungen zu erkennen und zu beheben, wodurch verhindert wird, dass sich Ungenauigkeiten im Laufe der Zeit ansammeln. CSAs Betonung eines dynamischen und anpassungsfähigen Lebenszyklusmodells stellt sicher, dass die Datenintegrität ein ständiger Schwerpunkt bleibt und den regulatorischen Erwartungen entspricht.
Um Datenabweichungen im Laufe der Zeit zu verhindern, integriert CSA mehrere strategische Maßnahmen. Erstens setzt es robuste Änderungskontrollprozesse ein, die alle Änderungen an computergestützten Systemen oder Prozessen, die die Datenintegrität beeinträchtigen könnten, sorgfältig dokumentieren. Regelmäßige Systemprüfungen und -bewertungen werden durchgeführt, um potenzielle Probleme zu identifizieren und zu beheben, bevor sie eskalieren. Darüber hinaus betont CSA die Bedeutung von Schulungs- und Sensibilisierungsprogrammen für Benutzer, um sicherzustellen, dass das Personal die Bedeutung der Aufrechterhaltung der Datenintegrität versteht und bewährte Verfahren einhält.
Zusammenfassend lässt sich sagen, dass sich der proaktive und umfassende Ansatz von CSA zur Datenintegrität als strategische Lösung in der pharmazeutischen Industrie abhebt. Durch die Einbeziehung kontinuierlicher Überwachung, Risikomanagement und strenger Änderungskontrollmaßnahmen wahrt CSA die Datenintegrität und stellt sicher, dass Pharmaunternehmen gut darauf vorbereitet sind, die sich entwickelnde Landschaft der regulatorischen Erwartungen zu meistern. Da Organisationen bestrebt sind, die höchsten Standards bei der Datenintegrität einzuhalten, erweist sich CSA als wichtiger Verbündeter auf ihrem Weg, im Einklang mit Branchentrends und regulatorischen Fortschritten.
Für Organisationen, die Unterstützung bei der Implementierung effektiver CSA-Strategien suchen, ist Freyr ein zuverlässiger Partner, der maßgeschneiderte Lösungen anbietet, um die einzigartigen Herausforderungen der Pharmalandschaft zu bewältigen.
Welche Rolle spielt die Einhaltung gesetzlicher Vorschriften bei CSA?
Die Einhaltung regulatorischer Vorschriften ist ein Eckpfeiler von CSA und stellt sicher, dass Pharmaunternehmen die sich entwickelnden Standards und Richtlinien über den gesamten Lebenszyklus eines Systems hinweg einhalten. Im Gegensatz zum traditionellen Fokus der Computer System Validierung (CSV) betont CSA die kontinuierliche Compliance und Anpassungsfähigkeit an sich ändernde regulatorische Rahmenbedingungen. Wenn Unternehmen von CSV zu CSA übergehen, wird es entscheidend, über sich entwickelnde Vorschriften auf dem Laufenden zu bleiben.
Im Kontext von CSA umfasst die Einhaltung regulatorischer Vorschriften die Abstimmung computergestützter Systeme mit globalen und lokalen regulatorischen Anforderungen von der Entwicklung über den operativen Einsatz bis zur endgültigen Außerbetriebnahme. CSA betont die fortlaufende Compliance anstelle einer periodischen Validierung, wodurch ein proaktiver Ansatz zur schnellen Bewältigung potenzieller regulatorischer Änderungen gefördert wird. Diese strategische Ausrichtung stellt sicher, dass Pharmaunternehmen gut darauf vorbereitet sind, regulatorische Erwartungen zu erfüllen und so Datenintegrität, Patientensicherheit und die allgemeine Systemzuverlässigkeit zu gewährleisten.

Regelmäßiger Austausch mit Aufsichtsbehörden, die Teilnahme an Branchenforen und das Abonnieren von Fachpublikationen bieten wertvolle Einblicke in sich entwickelnde Standards. Die Nutzung des Fachwissens von regulatorischen Beratern und die kontinuierliche Schulung des Personals, das an CSA-Prozessen beteiligt ist, stärken das regulatorische Bewusstsein zusätzlich. Die Zusammenarbeit mit regulatorischen Partnern, wie Freyr Solutions, ermöglicht einen proaktiven Ansatz, der den Zugang zu aktuellen regulatorischen Informationen und maßgeschneiderten Lösungen gewährleistet, um den Übergang reibungslos zu gestalten.
Die Einhaltung regulatorischer Vorschriften in CSA ist eine dynamische und fortlaufende Verpflichtung, die sich an der Verlagerung der Branche hin zu Anpassungsfähigkeit und kontinuierlicher Verbesserung orientiert. Informiert zu bleiben, proaktiv zu handeln und mit regulatorischen Experten zusammenzuarbeiten, ist entscheidend für Unternehmen, die von CSV zu CSA übergehen, um eine reibungslose und konforme Entwicklung in der sich ständig verändernden pharmazeutischen Landschaft zu ermöglichen.
Als vertrauenswürdiger regulatorischer Partner bietet Freyr die notwendige Unterstützung und Expertise, um Unternehmen durch diesen Übergang zu führen und regulatorische Exzellenz sowie Compliance im Zeitalter von CSA zu gewährleisten.
Wie hilft ein strategischer Partner für die Einhaltung gesetzlicher Vorschriften?
Ein strategischer Partner für regulatorische Compliance spielt eine entscheidende Rolle, um sicherzustellen, dass Pharmaunternehmen regulatorische Anforderungen erfüllen und hohe Qualitätsstandards aufrechterhalten. So können sie helfen:
- Expertenberatung: Ein strategischer Partner bietet fachkundige Beratung bei der Navigation durch komplexe und sich entwickelnde Vorschriften in verschiedenen Regionen. Sie bieten Einblicke in die neuesten regulatorischen Änderungen und helfen Unternehmen, ihre Praktiken anzupassen und die Compliance aufrechtzuerhalten.
- Optimierte Prozesse: Sie helfen, Compliance-Prozesse durch die Implementierung bewährter Verfahren und effizienter Arbeitsabläufe zu optimieren. Dazu gehört die Entwicklung robuster Systeme für Dokumentation, Auditing und Validierung, die Reduzierung des Verwaltungsaufwands und die Verbesserung der Gesamteffizienz.
- Risikominderung: Durch die Identifizierung potenzieller Compliance-Risiken und Schwachstellen hilft ein strategischer Partner, Risiken zu mindern, bevor sie zu Problemen werden. Sie führen gründliche Audits und Bewertungen durch, um sicherzustellen, dass alle Prozesse konform sind und eventuelle Lücken proaktiv geschlossen werden.
- Schulung und Unterstützung: Sie bieten Schulungen und Unterstützung an, um sicherzustellen, dass die Mitarbeiter gut über regulatorische Anforderungen und bewährte Verfahren informiert sind. Dies trägt zum Aufbau interner Kompetenzen bei und stellt sicher, dass alle an Compliance-Aktivitäten Beteiligten mit den aktuellen Standards vertraut sind.
- Technologieintegration: Ein strategischer Partner unterstützt bei der Integration innovativer Technologien, wie Automatisierung und KI, in Compliance-Prozesse. Sie stellen sicher, dass diese Technologien effektiv und in Übereinstimmung mit den regulatorischen Anforderungen implementiert werden, wodurch die Datenintegrität und Prozesseffizienz verbessert werden.
- Dokumentation und Aufzeichnungen: Sie verwalten die Erstellung, Organisation und Pflege wichtiger Compliance-Dokumentationen. Dies stellt sicher, dass alle Aufzeichnungen genau, vollständig und für Audits und Inspektionen leicht zugänglich sind.
- Regulatorische Einreichungen und Genehmigungen: Sie übernehmen die Vorbereitung und Einreichung regulatorischer Dokumente und Anträge. Dazu gehört die Sicherstellung, dass die Einreichungen alle notwendigen Anforderungen erfüllen, und die Verwaltung der Kommunikation mit den Regulierungsbehörden, um zeitnahe Genehmigungen zu erleichtern.
- Korrektur- und Präventivmaßnahmen: Ein strategischer Partner unterstützt die Entwicklung und Implementierung von Korrektur- und Präventivmaßnahmen als Reaktion auf Auditfeststellungen oder Compliance-Probleme. Sie tragen dazu bei, dass diese Maßnahmen wirksam sind und den laufenden Betrieb nicht stören.
- Globale Compliance-Strategie: Sie entwickeln und implementieren Strategien zur Erreichung globaler Compliance, die die vielfältigen regulatorischen Anforderungen verschiedener Märkte berücksichtigen. Dies stellt sicher, dass Produkte alle notwendigen Standards für den internationalen Vertrieb und die Nutzung erfüllen.
- Laufende Überwachung: Sie bieten laufende Überwachung und Unterstützung, um Unternehmen über regulatorische Aktualisierungen oder Änderungen auf dem Laufenden zu halten. Dieser proaktive Ansatz hilft Unternehmen, compliant zu bleiben und sich an neue Vorschriften anzupassen, sobald diese entstehen.
Warum Freyr wählen?
Mehr als zehn Jahre Exzellenz in der regulatorischen Compliance.
Umfassendes Spektrum an Compliance, Audits und Validierung.
Fachwissen in verschiedenen Branchen und Regionen.
Nutzt innovative Werkzeuge für präzise Ergebnisse.
Qualifizierte Fachkräfte mit fundiertem Branchenwissen.
Erfolgreiche Bewältigung komplexer Compliance-Herausforderungen.
Häufig gestellte Fragen
Pharmazeutische Compliance bedeutet die Einhaltung von Gesetzen, Vorschriften und Richtlinien, die die Pharmaindustrie regeln. Sie stellt sicher, dass Unternehmen ihre Abläufe an Industriestandards anpassen, wodurch die Produktsicherheit und -wirksamkeit gewährleistet und gleichzeitig die Datenintegrität gewahrt wird.
Der Zweck eines Audits ist es, die Einhaltung regulatorischer Standards und interner Richtlinien eines Unternehmens systematisch zu bewerten. Audits helfen dabei, Verbesserungspotenziale zu erkennen, Risiken zu mindern und sicherzustellen, dass die Prozesse effektiv sind, um sichere und konforme pharmazeutische Produkte herzustellen.
Validierung im pharmazeutischen Bereich ist der Prozess, der bestätigt, dass Systeme, Prozesse und Geräte stets vordefinierte Anforderungen erfüllen. Sie ist unerlässlich, um die Einhaltung regulatorischer Standards zu gewährleisten und die Qualität und Sicherheit pharmazeutischer Produkte über ihren gesamten Lebenszyklus hinweg aufrechtzuerhalten.
Diese Prozesse sind entscheidend, um die Produktsicherheit und -wirksamkeit zu gewährleisten, die Einhaltung regulatorischer Vorschriften aufrechtzuerhalten, die Qualitätssicherung zu verbessern, den Marktzugang zu unterstützen und eine kontinuierliche Verbesserung zu ermöglichen. Sie helfen Unternehmen, strenge Standards zu erfüllen und Vertrauen bei den Stakeholdern aufzubauen.
Zu den Herausforderungen gehören die Navigation durch sich ständig ändernde Vorschriften, die Gewährleistung der Datenintegrität, die Verwaltung von Ressourcenengpässen und die Aufrechterhaltung einer ordnungsgemäßen Dokumentation. Zusätzlich können die Integration innovativer Technologien und die Sicherstellung der Mitarbeiterkompetenz die Compliance-Bemühungen erschweren.
GxP-Audits sind Bewertungen, die sicherstellen sollen, dass die Standards der Guten Praktiken (GxP) eingehalten werden. Dazu gehören die Gute Herstellungspraxis (GMP), die Gute Klinische Praxis (GCP) und die Gute Laborpraxis (GLP). Diese Audits helfen dabei, Lücken in der Einhaltung zu identifizieren und die Qualitätssysteme zu verbessern.
Ein unabhängiges GxP-Compliance-Audit ist eine objektive Bewertung der Einhaltung von Qualitäts- und Regulierungsstandards eines Unternehmens. Durchgeführt von qualifizierten Auditoren, identifiziert es Risiken und Verbesserungspotenziale, wodurch die Compliance und Produktsicherheit verbessert werden.
GxP-Audits bieten unparteiische Bewertungen, verbessern die Einhaltung regulatorischer Vorschriften und zeigen Bereiche für betriebliche Verbesserungen auf. Sie tragen dazu bei, hohe Qualitätsstandards zu wahren und Vertrauen bei Aufsichtsbehörden und Kunden aufzubauen.
CSV stellt sicher, dass computergestützte Systeme, die in der Pharmazie eingesetzt werden, stets zuverlässige Daten liefern und regulatorische Anforderungen erfüllen. Dies ist entscheidend für die Aufrechterhaltung der Datenintegrität, die Risikominderung und die Gewährleistung der Patientensicherheit über den gesamten Produktlebenszyklus hinweg.
CSV konzentriert sich darauf, zu validieren, dass ein System regulatorische Anforderungen erfüllt und wie beabsichtigt funktioniert, während CSA einen breiteren Ansatz umfasst, der die kontinuierliche Sicherstellung der Systemleistung und Compliance über seinen gesamten Lebenszyklus hinweg einschließt.














