BIMO steht für Bioresearch Monitoring, ein Programm für Vor-Ort-Inspektionen und Datenprüfungen zur Überwachung aller Aspekte der Durchführung und Berichterstattung von durch die US Food and Drug Administration (FDA) regulierter Forschung. Das Programm wurde 1977 ins Leben gerufen, nachdem der Bedarf an der Prüfung klinischer Forschungsstandorte festgestellt wurde. Das Hauptziel dieses Programms ist es, die Qualität und Integrität der eingereichten Daten für neue Produktzulassungen und Marketinganträge sicherzustellen. Darüber hinaus schützt dieses Programm auch die Rechte und das Wohlergehen von menschlichen und tierischen Probanden, die an der FDA-regulierten Forschung beteiligt sind.
Die Hauptziele des BIMO-Programms
Jährlich werden über 1000 Inspektionen durchgeführt. Die Hauptziele, die im Rahmen des BIMO-Programms abgedeckt werden, sind:
- Audit klinischer Daten
- Überprüfung laufender klinischer Studien
- Überprüfung nicht-klinischer Labore
- Inspektion von Institutional Review Boards (IRB)
Welche Produkte fallen in den Geltungsbereich des BIMO-Audits?
BIMO ist anwendbar für Arzneimittel, Biologika, Medizinprodukte, Lebensmittel, Tabakprodukte und Tierarzneimittel. Das Compliance-Programm wird von den sechs (06) Produktzentren der FDA überwacht: Center for Biologics Evaluation and Research (CBER), Center for Devices and Radiological Health (CDRH), Center for Drug Evaluation and Research (CDER), Center for Food Safety and Applied Nutrition (CFSAN), Center for Tobacco Products (CTP) und Center for Veterinary Medicine (CVM).
Welche Unternehmen unterliegen dem BIMO-Audit?
Sowohl inländische als auch internationale Unternehmen, die eine der unten genannten Aktivitäten durchführen oder unter diese fallen, unterliegen den Anforderungen des Bioresearch Monitoring –
- Nicht-klinische Prüflabore für die Einhaltung der Guten Laborpraxis (GLP)
- Klinische Prüfer für die Einhaltung der Guten Klinischen Praxis (GCP)
- Sponsoren
- Vertragsforschungsorganisationen (CROs)
- Klinische Prüfmonitore
- Einrichtungen für In-vivo-Bioäquivalenz
- Institutional Review Boards (IRBs)
Welche Compliance-Programme fallen unter das BIMO-Programm?
Die US FDA kann jederzeit ein BIMO-Audit durch die sieben (07) Multi-Center-Compliance-Programme durchführen. Diese sieben Multi-Center-Compliance-Programme werden umgesetzt durch –
- Inspektion von klinischen Prüfärzten (CI) und Sponsor-Prüfärzten (SI)
- Inspektion von Institutional Review Boards (IRB)
- Inspektion von Auftragsforschungsinstituten/Sponsoren/Monitoren (CRO/S/M)
- Inspektion der Guten Laborpraxis (GLP)
- Bioäquivalenz-Bioverfügbarkeits-Inspektion (BEQ)
- Inspektion der Meldung unerwünschter Arzneimittelwirkungen nach dem Inverkehrbringen (PADE)
- Inspektion der Meldung von Risikobewertungs-, Minderungs- und Strategieplänen (REMS)
Jedes dieser Programme skizziert einen detaillierten Umfang der Überprüfung oder Inspektion, die durchgeführt werden muss, um die Einhaltung der FDA-Vorschriften zu gewährleisten.
Welche Vorschriften sind für das BIMO-Audit anwendbar?
Die Vorschriften – 21 CFR 50 – Schutz menschlicher Probanden, 21 CFR 54 – Finanzielle Offenlegung, 21 CFR 56 – IRBs, 21 CFR 58 – Gute Laborpraxis für nicht-klinische Labore, 21 CFR 809 – In-vitro-Diagnostika und 21 CFR 812 – Ausnahmegenehmigung für Prüfprodukte – sind für das BIMO-Audit anwendbar.
Wie viele Audits werden jährlich im Rahmen des BIMO-Programms durchgeführt?
Die Anzahl der von der US FDA durchgeführten BIMO-Audits variiert jedes Jahr. In den letzten Jahren ist die Anzahl der Vor-Ort-Inspektionen aufgrund des Ausbruchs der COVID-19-Pandemie zurückgegangen, und die FDA musste alle Vor-Ort-Überwachungen der klinischen Studien aussetzen. Es wurden nur spezifische kritische und entscheidende klinische Studien überwacht.
Die „Remote Regulatory Assessments“ (RRAs) wurden während der COVID-19-Pandemie eingeführt, um regulierte Forschung aus der Ferne zu überwachen. RRAs werden über Videokonferenzen durchgeführt und sind eine freiwillige Initiative zur Fernbewertung von Daten und Prozessen. Dabei ist jedoch zu beachten, dass RRAs kein Äquivalent oder eine Alternative zur Vor-Ort-Inspektion sind, sondern lediglich ein Verfahren, das sich aufgrund der COVID-19-Pandemie entwickelt hat.
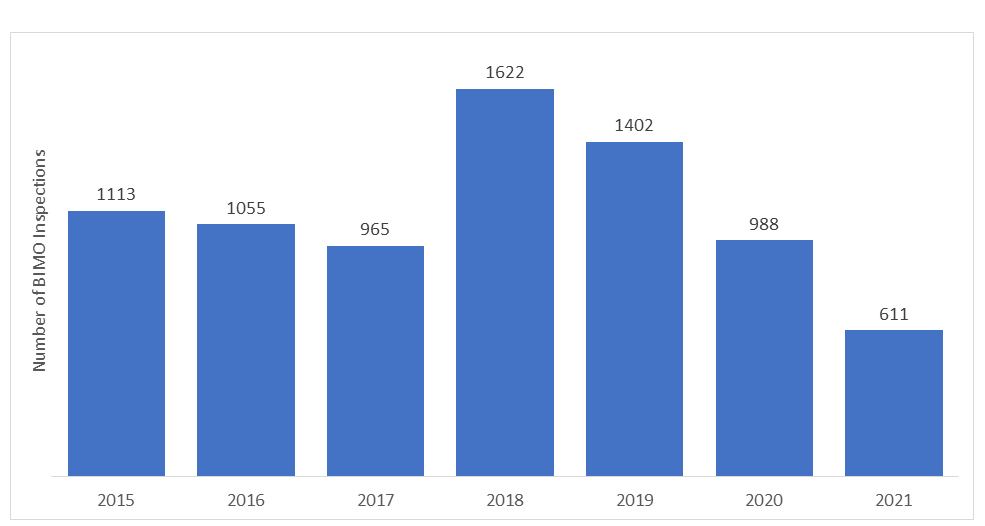
*Die dargestellten Daten für die Jahre 2020 und 2021 enthalten keine RRA-Inspektionen.
Wie viele Remote Regulatory Assessments (RRAs) wurden während der COVID-19-Pandemie im Rahmen des BIMO-Programms durchgeführt?
Im Jahr 2021 nahm die Einführung von RRA-Inspektionen in allen Programmen erheblich zu. Im April 2021 veröffentlichte die FDA ein Leitliniendokument mit dem Titel „Remote Interactive Evaluations of Drug Manufacturing and Bioresearch Monitoring Facilities During the COVID-19 Public Health Emergency Guidance for Industry“, das umfassende Informationen über den Prozess der FDA zur Durchführung von RRAs bereitstellt.
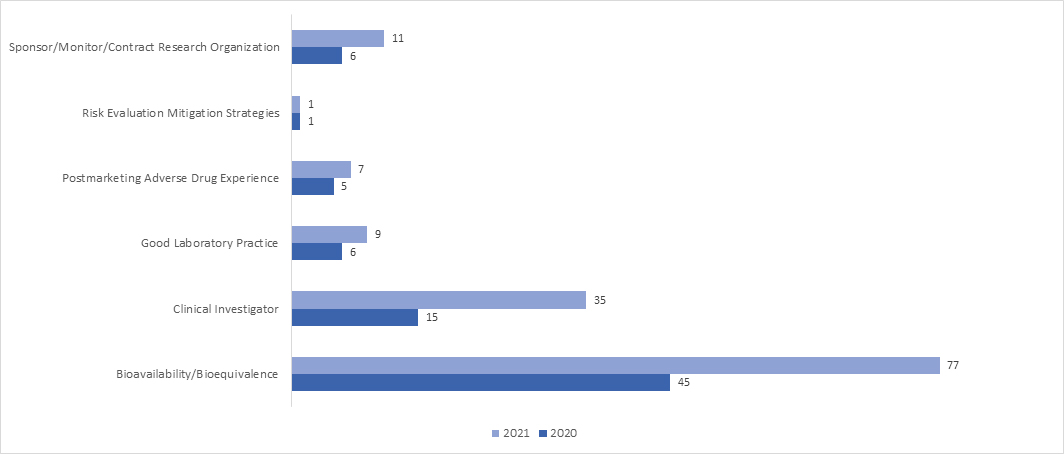
Was sind die möglichen Ergebnisse eines BIMO-Audits?
Während des BIMO-Audits kann die US FDA basierend auf der Einhaltung der Vorschriften eine der unten aufgeführten Maßnahmen ergreifen –
1. No Action Indicated (NAI)
NAI ist anwendbar, wenn der FDA-Feldinspektor keine beanstandungswürdige Praxis oder nur geringfügige Probleme festgestellt hat, für die weitere Maßnahmen nicht gerechtfertigt sind.
2. Voluntary Action Indicated (VAI)
VAI ist anwendbar, wenn bedenkliche Praktiken festgestellt wurden, die jedoch nicht gravierend sind.
3. Official Action Indicated (OAI)
OAI ist anwendbar, wenn bedenkliche Praktiken festgestellt wurden, die die Datenintegrität und/oder die Rechte menschlicher Probanden beeinträchtigen.
Was sind die häufigsten Nichtkonformitäten, die bei einem BIMO-Audit festgestellt werden?
Einige der häufigsten Nichtkonformitäten, die während des BIMO-Audits festgestellt werden, sind –
- Mangelhafte Aufzeichnungen
- Mängel in Bezug auf den Prüfplan
- Nichteinhaltung der Vorschriften
- Mangelhafte Überwachung der Protokolle
- Unzureichender Schutz der Probanden
- Unzureichende Rechenschaftspflicht für das zu untersuchende Produkt.
Das BIMO-Audit ist entscheidend für jeden Entwickler oder Hersteller neuartiger Medizinprodukte und Technologien, der plant, sein Produkt auf dem US-Markt einzuführen. Die Einhaltung der Vorschriften und Richtlinien, um die beschriebenen Fallstricke zu vermeiden, ist sehr wichtig.
Benötigen Sie Unterstützung bei BIMO-Audit-Inspektionen? Kontaktieren Sie Freyr. Bleiben Sie informiert. Bleiben Sie konform.