Przegląd rejestracji wyrobów medycznych w Kolumbii
Kolumbia stwarza ogromne możliwości dla firm produkujących wyroby medyczne, a jej system opieki zdrowotnej jest znany z zaangażowania w bezpieczeństwo pacjentów i jakość usług medycznych, i reguluje wyroby medyczne za pośrednictwem INVIMA (Krajowego Instytutu Nadzoru nad Żywnością i Lekami). INVIMA jest organem operacyjnym odpowiedzialnym za rejestrację wyrobów medycznych w Kolumbii.

Organ regulacyjny: INVIMA (Narodowy Instytut Nadzoru nad Żywnością i Lekami)
Regulacja: Dekret 4725/2005
Ścieżka regulacyjna: Rejestracja wyrobów
Autoryzowany Przedstawiciel: Przedstawiciel prawny w Kolumbii
Wymaganie QMS: ISO 13485:2016 / MDSAP
Ocena Danych Technicznych: INVIMA
Wymogi dotyczące oznakowania: Dokumenty oznakowania muszą być w języku hiszpańskim
Ważność licencji: 10 lat
Format przedłożenia: Elektroniczny
Klasyfikacja wyrobów medycznych w Kolumbii
| Klasyfikacja wyrobów medycznych | |
|---|---|
| Klasa I (Najniższe ryzyko) | |
| Klasa IIa | |
| Klasa IIb | |
| Klasa III (Najwyższe ryzyko) | |
Przedstawiciel prawny w Kolumbii
Aby zostać Przedstawicielem Prawnym w Kolumbii, należy posiadać obywatelstwo kolumbijskie lub niezbędne uprawnienia prawne do zamieszkania i pracy w kraju jako cudzoziemiec. Przedstawiciel Prawny może pomagać i zarządzać wszystkimi procedurami rejestracyjnymi w Kolumbii, działając jako łącznik między firmą a INVIMA, lokalnym organem regulacyjnym.
Rejestracja wyrobów medycznych w Kolumbii
Wyroby medyczne i IVD podlegają procedurze rejestracji, dlatego wyrób medyczny musi być zarejestrowany w INVIMA, aby mógł być wprowadzony do obrotu w Kolumbii.
Aby wprowadzić wyrób medyczny na rynek w Kolumbii, wymagane jest uzyskanie Certyfikatu Wolnej Sprzedaży (CFS) lub Certyfikatu dla Rządu Zagranicznego (CFG) wydanego przez odpowiednią agencję regulacyjną w kraju pochodzenia lub uznanym kraju referencyjnym (np. Kanada, Japonia, Australia, Unia Europejska i US). Certyfikat Wolnej Sprzedaży lub Certyfikat dla Rządu Zagranicznego służy jako dowód, że wyrób medyczny spełnia niezbędne normy bezpieczeństwa i jakości do sprzedaży w Kolumbii.
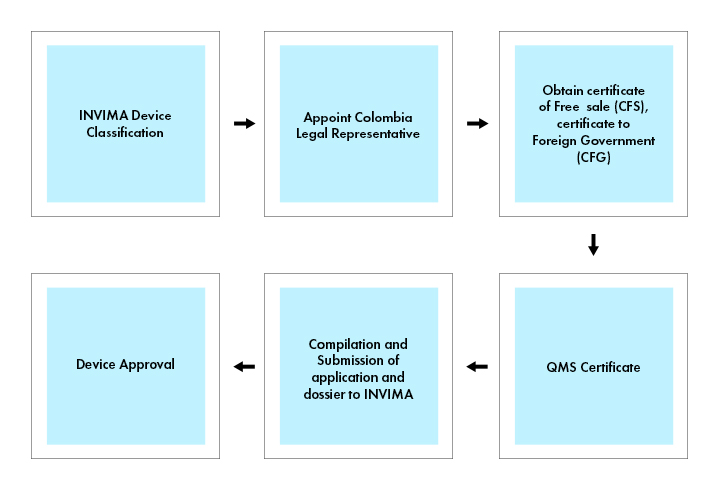
Przebieg procesu
Zarządzanie cyklem życia urządzenia po zatwierdzeniu
Freyr wspiera zagranicznych producentów w zarządzaniu cyklem życia wyrobów medycznych End-to-End, w tym w działaniach po zatwierdzeniu, takich jak:
- Zarządzanie zmianami po zatwierdzeniu – modyfikacje istniejących zatwierdzeń wyrobów medycznych, takie jak dodanie nowych wariantów, akcesoriów; dodanie nowych wskazań do stosowania i inne
- Utrzymywanie zatwierdzeń i rejestracji poprzez terminowe uiszczanie opłat administracyjnych i rejestracyjnych
- Odnowienie licencji
- Pośrednictwo między INVIMA a producentem
Podsumowanie
| Klasyfikacja wyrobów medycznych | Nowe licencje i odnowienia | ||
|---|---|---|---|
| Nowa rejestracja | Zmiana | Odnowienie | |
| Klasa I | 4–6 miesięcy | 2-3 miesiące | 4–6 miesięcy |
| Klasa IIa | 4–6 miesięcy | 2-3 miesiące | 4–6 miesięcy |
| Klasa IIb | 4–6 miesięcy | 2-3 miesiące | 4–6 miesięcy |
| Klasa III | 4–6 miesięcy | 2-3 miesiące | 4–6 miesięcy |
| Opłaty rejestracyjne | |||||
|---|---|---|---|---|---|
| Nowe licencje i odnowienia | Modyfikacje techniczne. | Zmiany administracyjne | |||
| Klasa I i Klasa IIa | Klasa IIb i Klasa III | Klasa I i Klasa IIa | Klasa IIb i Klasa III | Klasa I i Klasa IIa | Klasa IIb i Klasa III |
| $ 690,00 | $ 776,00 | $ 196,00 | $ 196,00 | $ 153,00 | $ 153,01 |
Ekspertyza Freyr
- Należyta staranność regulacyjna
- Oficjalna Klasyfikacja
- Rejestracja wyrobów
- Posiadacz rejestracji w Kolumbii
- Wsparcie w zakresie etykietowania
- Wsparcie tłumaczeniowe
- Identyfikacja i kwalifikacja dystrybutora
- Nadzór po wprowadzeniu do obrotu
- Zarządzanie zmianami po zatwierdzeniu
- Odnowienie i przeniesienie licencji
- Złożenie dokumentów i kontakt z INVIMA