Usługi w zakresie zgodności, audytu i walidacji – Przegląd
Czy spełniasz wymogi? To pytanie, na które trudno odpowiedzieć każdej firmie z branży farmaceutycznej, biotechnologicznej, genomicznej, chemicznej, producentom urządzeń medycznych oraz podmiotom zajmującym się zarządzaniem łańcuchem dostaw. Organizacje te muszą spełniać rygorystyczne wymagania dotyczące jakości, bezpieczeństwa i zgodności z przepisami w każdym regionie, w którym dystrybuowane są ich produkty. Obecny trend w zarządzaniu zgodnością z przepisami zmierza w kierunku globalnej harmonizacji jakości i bezpieczeństwa, kładąc nacisk na solidne praktyki. Niezależnie od tego, czy jesteś producentem, czy dostawcą, ekspansja rynkowa, ciągłe doskonalenie i zadowolenie klientów zależą głównie od standardów jakości Twojej firmy. Centrum Doskonałości (CoE) ds. zgodności z przepisami, audytu i walidacji firmy Freyr może pomóc w tych działaniach, oferując profesjonalne usługi w zakresie zgodności, audytu i walidacji dla branży farmaceutycznej, wyroby medyczne, produktów konsumenckich i opieki zdrowotnej, takie jak cGMP (aktualne dobre praktyki produkcyjne), GCP dobre praktyki kliniczne), GDP dobre praktyki dystrybucyjne), Dobrej Praktyki Laboratoryjnej (GLP), GPVP Dobrej monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny walidacji systemów komputerowych GxP (CSV). Nasz zespół doradców ds. zgodności farmaceutycznej zapewnia rozwiązania dostosowane do Twoich indywidualnych wyzwań w zakresie zgodności.
Freyr świadczy usługi w zakresie zgodności z przepisami, audytu i walidacji, które obejmują ocenę Państwa wymagań oraz proponowanie rozwiązań dla procesów biznesowych mających na celu zapewnienie satysfakcji klientów. Dzięki naszym strategiom przygotowywania raportów z audytu zgodności oraz zapewniania gotowości dostarczamy raporty dotyczące zgodności i audytu (analiza luk), zawierające propozycje działań korygujących i zapobiegawczych (CAPA), które pozwalają uniknąć potencjalnych uwag typu 483 oraz zastrzeżeń organów regulacyjnych w wyniku audytu zgodności. Doradztwo firmy Freyr w zakresie zgodności farmaceutycznej obejmuje również doradztwo w zakresie zgodności automatyzacji farmaceutycznej, zapewniając, że zautomatyzowane systemy spełniają zmieniające się oczekiwania organów regulacyjnych. Nasze kompleksowe podejście do zarządzania zgodnością gwarantuje, że każdy etap cyklu życia procesu jest monitorowany i optymalizowany pod kątem zgodności z przepisami.
Świadczymy usługi w zakresie zgodności z przepisami i walidacji, aby zapewnić, że wszystkie Państwa procesy i produkty są zgodne z obowiązującymi wymogami dotyczącymi jakości, bezpieczeństwa informacji oraz audytów zgodności z przepisami, takimi jak (między innymi):
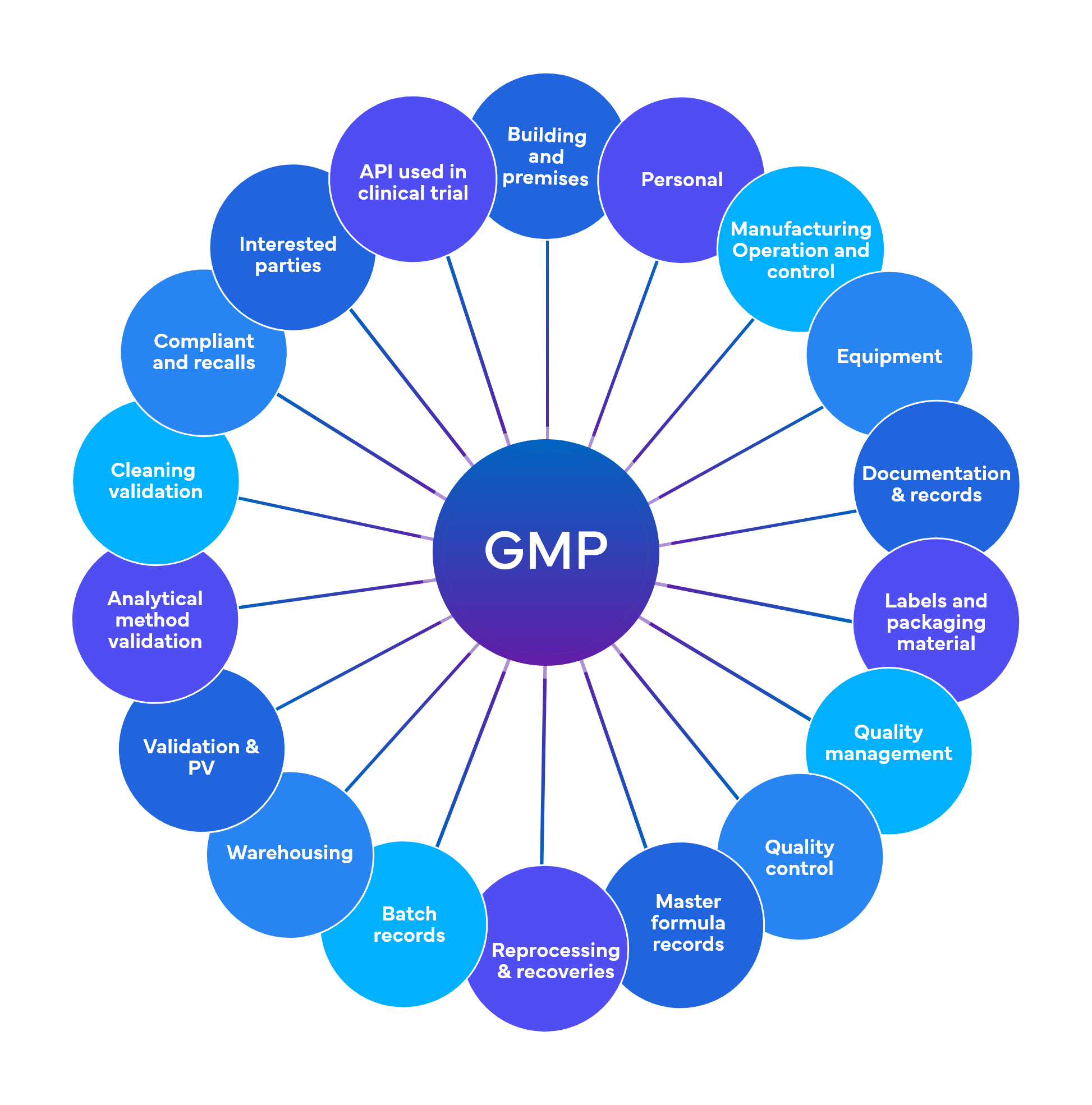
Freyr przeprowadza około 700 wstępnych kontroli, rozłożonych na 18-19 obszarów funkcjonalnych GMP.
Zgodność, Audyt i Walidacja Freyr
Usługi w zakresie zgodności, audytu i walidacji
Jakość i zgodność regulacyjna – Obecne Dobre Praktyki Wytwarzania (cGMP)
- ISO / IEC 17025: 2017 – Ogólne wymagania dotyczące kompetencji laboratoriów badawczych i wzorcujących
- OECD (Organizacja Współpracy Gospodarczej i Rozwoju) - Wytyczne Dobrej Praktyki Laboratoryjnej
- Przewodnik EURACHEM / CITAC: Przewodnik po jakości w chemii analitycznej – Pomoc w akredytacji, wydanie 3 (2016), powinien być przestrzegany w procedurach analitycznych
- 21 CFR 58: Dobra Praktyka Laboratoryjna dla nieklinicznych badań laboratoryjnych
- Przewodnik po brytyjskich przepisach GLP, luty 2000 (opracowany przez GLPMA)
- Podręcznik WHO dotyczący Dobrej Praktyki Laboratoryjnej (GLP): Praktyki jakościowe w regulowanych nieklinicznych badaniach i rozwoju
- Health Canada: Ukończony dokument wytycznych – Dane z nieklinicznych badań laboratoryjnych wspierające wnioski i zgłoszenia dotyczące produktów leczniczych: Zgodność z Dobrą Praktyką Laboratoryjną
- Standardy OSHA (Occupational Safety and Health Administration)
- Obowiązujące wytyczne ICH
Dobra Praktyka Laboratoryjna
- ISO / IEC 17025: 2017 – Ogólne wymagania dotyczące kompetencji laboratoriów badawczych i wzorcujących
- OECD (Organizacja Współpracy Gospodarczej i Rozwoju) - Wytyczne Dobrej Praktyki Laboratoryjnej
- Przewodnik EURACHEM / CITAC: Przewodnik po jakości w chemii analitycznej – Pomoc w akredytacji, wydanie 3 (2016), powinien być przestrzegany w procedurach analitycznych
- 21 CFR 58: Dobra Praktyka Laboratoryjna dla nieklinicznych badań laboratoryjnych
- Przewodnik po brytyjskich przepisach GLP, luty 2000 (opracowany przez GLPMA)
- Podręcznik WHO dotyczący Dobrej Praktyki Laboratoryjnej (GLP): Praktyki jakościowe w regulowanych nieklinicznych badaniach i rozwoju
- Health Canada: Ukończony dokument wytycznych – Dane z nieklinicznych badań laboratoryjnych wspierające wnioski i zgłoszenia dotyczące produktów leczniczych: Zgodność z Dobrą Praktyką Laboratoryjną
- Standardy OSHA (Occupational Safety and Health Administration)
- Obowiązujące wytyczne ICH
Dobra Praktyka Kliniczna (GCP) i Dobra Praktyka monitorowania bezpieczeństwa stosowania produktów leczniczych (GVP)
- Ujednolicone Trójstronne Wytyczne ICH: Wytyczne Dobrej Praktyki Klinicznej - E6
- Specyfikacja Indywidualnego Raportu Bezpieczeństwa Przypadku (ICSR) E2B(R3) i powiązane pliki
- Okresowy Raport z Oceny Korzyści i Ryzyka (PBRER) E2C(R2)
- Inne obowiązujące wytyczne ICH
- Wytyczne dotyczące Dobrych Praktyk monitorowania bezpieczeństwa stosowania produktów leczniczych (GVP) – Moduły
- Wymogi FDA dotyczące zgłaszania bezpieczeństwa dla wniosków IND i badań BA/BE
- Raportowanie bezpieczeństwa po wprowadzeniu do obrotu dla produktów leczniczych stosowanych u ludzi i produktów biologicznych, w tym szczepionek
- Regionalne specyfikacje wdrożeniowe FDA dla raportowania ICH E2B(R3) do Systemu Zgłaszania Zdarzeń Niepożądanych FDA (FAERS).
- Przygotowywanie zgłoszeń w formacie elektronicznym – niepilne indywidualne raporty bezpieczeństwa (ICSR) po wprowadzeniu do obrotu, pytania i odpowiedzi techniczne
- End-to-End Planowanie monitorowania bezpieczeństwa stosowania produktów leczniczych
Bezpieczeństwo Informacji, Prywatność Danych i Walidacja Systemów Komputerowych (CSV)
- ISO 27001: 2013 Technika informatyczna – Techniki bezpieczeństwa – System zarządzania bezpieczeństwem informacji – Wymagania
- ISO 27002: 2013 Technika informatyczna – Techniki bezpieczeństwa – Kodeks postępowania w zarządzaniu bezpieczeństwem informacji
- USFDA 21 CFR Part 11: Zapisy elektroniczne; Podpisy elektroniczne – Zakres i zastosowanie
- Przewodnik UE GMP, Załącznik 11
- Japońskie wytyczne ERES, powiadomienie nr 0401022
- GAMP 5: Podejście oparte na ryzyku do zgodnych z GxP systemów skomputeryzowanych
- USFDA – Wytyczne walidacji oprogramowania
- Obowiązujące wytyczne ICH QSEM
- Planowanie i tworzenie SOP oraz kontrola zakładów produkcyjnych
- Zintegrowany model procesu
- Utrzymuj wizerunek marki
- Usługi oceny ryzyka
- Całkowite oszczędności kosztów
- Wdrożyć skuteczne i zgodne z przepisami procesy biznesowe
- Ustanawianie strategii walidacji i kwalifikacji
- Ekspertyza w zakresie zgodności regulacyjnej i audytowej
- Profesjonalni audytorzy zgodności
Nasze podejście do doradztwa w zakresie jakości i zgodności z przepisami ma na celu dostarczanie praktycznych wskazówek i zapewnienie trwałych usprawnień, wspierając Państwa firmę w dążeniu do doskonałości operacyjnej i osiągnięciu sukcesu w zakresie zgodności z przepisami.



 Usługi w zakresie zgodności i audytu
Usługi w zakresie zgodności i audytu










