Usługi etykietowania klinicznego – Przegląd
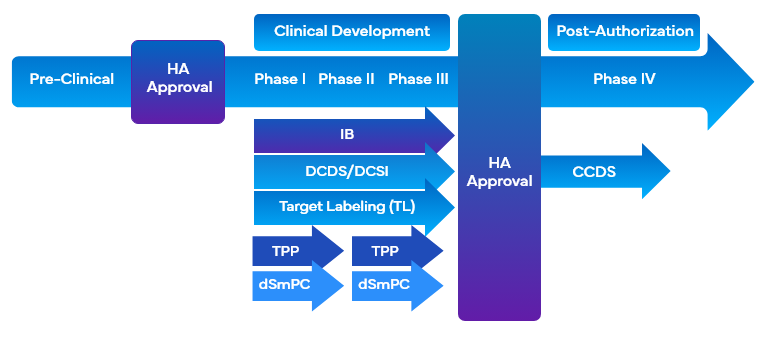
W trakcie opracowywania leków firmy korzystają z szeregu narzędzi związanych z oznakowaniem klinicznym, które wykorzystują oznakowanie docelowe w celu usprawnienia tego procesu. Narzędzia te pozwalają jednocześnie dostosować pożądane cele w zakresie oznakowania marketingowego i oznakowania badań klinicznych do przebiegu opracowywania programu lub projektu badania oraz ułatwiają sporządzenie przeglądu klinicznego (CO). Niektóre z narzędzi do oznakowania klinicznego, które wykorzystują oznakowanie docelowe podczas opracowywania leków, to:
- Investigator Brochure (IB)
- Etykietowanie docelowe (TL)/Profil docelowy.
- Karta danych podstawowych rozwoju (DCDS)
- Opracowanie podstawowych informacji o bezpieczeństwie (DCSI)
- Docelowy profil produktu FDA (TPP)
Ważne jest, aby firmy stosowały modułowe podejście podczas gromadzenia informacji o bezpieczeństwie i skuteczności dla różnych rodzajów etykiet klinicznych w celu uzupełnienia wymagań dotyczących etykietowania klinicznego. Pozwoliłoby to skutecznie wspierać badaczy i sponsorów poprzez prezentowanie i aktualizowanie ukierunkowanej i dedykowanej sekcji DCSI, którą można wygodnie umieścić w różnych kategoriach klinicznych.
Ponadto, DCSI jest uwzględnione w Podstawowych Informacjach o Bezpieczeństwie Firmy (CCSI), które stanowią podstawę dla pierwszej Podstawowej Karty Danych Firmy (CCDS) i są wykorzystywane do wprowadzenia produktu na rynek. Wymagane jest również sporządzenie szczegółowego CO, obejmującego zakres i kluczowe kwestie w programie rozwoju klinicznego leku, aby wesprzeć dokumentację dla oceniających.
Usługi etykietowania klinicznego Freyr
Usługi etykietowania klinicznego
Tworzenie i przegląd Broszury Badacza (IB)
Firma Freyr posiada bogate doświadczenie w tworzeniu, redagowaniu i weryfikacji protokołów badań klinicznych (IB) dla różnych programów badań klinicznych realizowanych na zlecenie naszych klientów. IB to najnowsza forma dokumentacji mająca na celu dostarczenie badaczowi lub lekarzowi prowadzącemu istotnych informacji dotyczących leku/interwencji. Ich celem jest przekazanie badaczom i innym osobom zaangażowanym w badanie informacji niezbędnych do zrozumienia uzasadnienia wielu kluczowych elementów protokołu oraz zapewnienia zgodności z nimi. Obejmują one dawkę, częstotliwość/odstępy między dawkami, metody podawania oraz procedury monitorowania bezpieczeństwa. IB informacje przedkliniczne i kliniczne dotyczące badanego leku.

Podczas pracy nad IB, eksperci Freyr w dziedzinie etykietowania klinicznego przedstawiają informacje w zwięzłej, prostej, obiektywnej i wyważonej formie. Te same cechy można wziąć pod uwagę również podczas tłumaczenia dokumentów. Oprócz tworzenia IB, Freyr wspiera również coroczny przegląd IB i pracuje nad rewizjami w razie potrzeby, zgodnie ze standardowymi procedurami ustalonymi przez klientów i sponsorów.
Opracowanie etykietowania docelowego (TL)/profilu docelowego
Opracowanie i przegląd DCDS i DCSI
Freyr posiada udowodnione doświadczenie w tworzeniu wysokiej jakości arkuszy danych rozwojowych (DCDS). DCDS to pośrednia etykieta podstawowa, kluczowa w pozyskiwaniu treści dla pierwszych krajowych etykiet (takich jak USPI, SmPC itp.). DCDS/DCSI jest przygotowywany na podstawie etykiety docelowej i zapewnia zintegrowane bezpieczeństwo i skuteczność interwencji lub leku. DCDS/DCSI pomaga badaczom i sponsorom poprzez prezentowanie i aktualizowanie ukierunkowanych i dedykowanych sekcji DCDS, które można wygodnie umieścić w IB. DCSI ułatwia rozwój CCSI, który później stanowi integralną część Podstawowego Arkusza Danych Firmy (CCDS).
Opracowanie i przegląd profilu produktu docelowego FDA (TPP) oraz projektu SmPC UE (dSmPC)
Profil docelowego produktu (TPP)/projekt charakterystyki produktu leczniczego (dSmPC) to rodzaj etykiety klinicznej, która ułatwia dialog między firmami farmaceutycznymi a organami ds. zdrowia. TPP jest wykorzystywany w całym procesie opracowywania leku, począwszy od fazy poprzedzającej złożenie wniosku o dopuszczenie nowego leku do badań klinicznych (IND) oraz samej fazy składania wniosku o dopuszczenie nowego leku do badań klinicznych (IND), aż po programy poprodukcyjne, w celu uzyskania nowych wskazań lub wprowadzenia innych istotnych zmian w etykietach badań klinicznych. Firmy farmaceutyczne określają koncepcje etykietowania, które są celami programu rozwoju leku, w formie TPP. TPP zawiera oświadczenie dotyczące ogólnego zamierzenia programu rozwoju leku oraz informacje o leku na konkretnym etapie rozwoju. Jako strategiczny partner w zakresie regulacji, firma Freyr posiada doświadczenie w przygotowywaniu TPP dla US dSmPC dla Unii Europejskiej.
- Zasoby z dogłębną wiedzą regulacyjną w zakresie pakowania klinicznego i etykietowania
- Ekspertyza w skutecznym zarządzaniu globalnym i regionalnym etykietowaniem leków dla klientów z branży farmaceutycznej z listy Fortune w US, Europie, regionie APAC, MENA itd.
- Globalna ekspertyza regulacyjna we wspieraniu organizacji z branży nauk przyrodniczych, tj. producentów farmaceutycznych, biotechnologicznych i żywieniowych
- Wysoce wykwalifikowani autorzy tekstów medycznych posiadający bogate doświadczenie w etykietowaniu regulacyjnym
- Dogłębna i aktualna wiedza na temat zmian w globalnych przepisach dotyczących etykietowania leków wprowadzonych przez różne organy ds. zdrowia, takie jak US FDA, EMA, TGA itp.
- Dedykowany zespół ds. zgodności monitorujący status wdrożenia podstawowej i firmowej podstawowej karty danych (CDS/CCDS) w etykietach regionalnych
- Ekspertyza w zakresie etykietowania badań klinicznych i usług etykietowania klinicznego.
- Wysoce doświadczeni specjaliści ds. etykietowania produktów farmaceutycznych, biotechnologicznych i żywieniowych









